硼氢化钠(NaBH4)为白色粉末,容易吸水潮解,可溶于异丙胺(熔点:-101℃,沸点:33℃),在干空气中稳定,在湿空气中分解,是无机合成和有机合成中常用的选择性还原剂。某研究小组采用偏硼酸钠(NaBO2)为主要原料制备NaBH4,其流程如下:
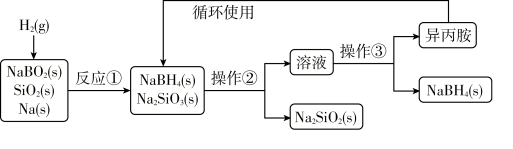
下列说法不正确的是

下列说法不正确的是
| A.实验室中取用少量钠需要用到的实验用品有镊子、滤纸、玻璃片和小刀 |
| B.操作②、操作③分别是过滤与蒸发结晶 |
| C.反应①加料之前需将反应器加热至100℃以上并通入氩气 |
| D.反应①中消耗的H2与Na的物质的量之比为1∶2 |
更新时间:2019-09-06 16:31:47
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】化学实验设计和操作须十分重视安全和环保问题。下列关于实验问题处理正确的是
| A.做CO还原CuO时,应先加热再通入CO,以免浪费CO和污染空气 |
| B.稀释浓硫酸时,将浓硫酸沿器壁缓慢加入水中,边加边搅拌,以免液体过热引起外溅 |
| C.蒸馏时加热一段时间,发现忘记加沸石,应迅速补加沸石并继续加热 |
| D.做CO还原CuO实验须检验CO纯度,最简单的方法是排空气法收集一试管气体,点燃气体,听爆鸣声 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验操作或实验设计正确的是
| A | B | C | D |
 |  |  |  |
| 验证铁钉的析氢腐蚀 | 验证1-溴丙烷发生消去反应 | 熔化 固体 固体 | 收集 气体 气体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】高纯碳酸锰在电子工业中有着重要的应用,湿法浸出软锰矿(主要成分为MnO2,含有少量Fe、Al、Mg等杂质元素)制备高纯碳酸锰的流程如下:其中除杂过程包括:①向浸出液中加入一定量的试剂X,调节浸出液的pH为3.5~5.5;②再加入一定量的软锰矿和双氧水,过滤;③…下列说法正确的是(已知室温下:Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3.0×10-34,Ksp[Fe(OH)3]=4.0×10-38。)


| A.浸出时加入植物粉的作用是作为还原剂 |
| B.除杂过程中调节浸出液的pH为3.5~5.5可完全除去Fe、Al、Mg等杂质 |
| C.试剂X可以是MnO、MnO2、MnCO3等物质 |
| D.为提高沉淀MnCO3步骤的速率可以持续升高温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】重铬酸钠在工业生产上具有广泛用途。一种以铬铁矿(含FeCr2O4及少量Al2O3、SiO2等)为原料制备Na2Cr2O7的工艺流程如下:
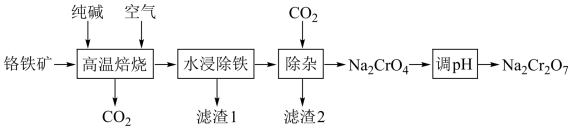
已知滤渣1为Fe2O3。下列说法错误的是

已知滤渣1为Fe2O3。下列说法错误的是
| A.流程中可循环使用的物质有CO2 |
| B.滤渣2的成分是Al(OH)3和H2SiO3 |
| C.“调pH”是向溶液中加NaOH使pH增大,促进氧化还原反应进行 |
D.“高温焙烧"发生的主要反应为4FeCr2O4+7O2+8Na2CO3 2Fe2O3+8Na2CrO4+8CO2 2Fe2O3+8Na2CrO4+8CO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的特殊情况,下列反应中属于这种情况的是①过量的锌与18mol/L硫酸溶液反应 ②过量的氢气与少量的氮气在催化剂存在下充分反应 ③过量的MnO2 与浓盐酸反应 ④过量铜与浓硫酸反应 ⑤过量稀硝酸与铁反应;⑥过量的水与一定量的氯气反应;⑦常温下,过量的浓硫酸与铝反应
| A.②③④⑥⑦ | B.②③⑤⑦ | C.①③⑦ | D.①②③④⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在一定条件下,向Al2O3和过量C粉的混合物中通入纯净的氯气,可制得易水解的AlCl3,反应的化学方程式为Al2O3+3Cl2+3C 2AlCl3+3CO,实验装置如图所示。下列说法错误的是
2AlCl3+3CO,实验装置如图所示。下列说法错误的是

 2AlCl3+3CO,实验装置如图所示。下列说法错误的是
2AlCl3+3CO,实验装置如图所示。下列说法错误的是
A.装置a中反应的化学方程式为:MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O MnCl2+Cl2↑+2H2O |
| B.装置b、c中盛装的分别是饱和食盐水和浓硫酸 |
| C.装置d、e之间应添加一个干燥装置 |
| D.此实验的尾气,除氯气外都可直接排放到大气中 |
您最近一年使用:0次




