KClO3和浓盐酸在一定温度下反应会生成红黄色的易爆物二氧化氯。
(1)请完成该过程的化学方程式并配平。
____ KClO3+___ HCl(浓)===____ KCl+____ ClO2↑+____ Cl2↑+___ ( )
(2)浓盐酸在反应中显示出来的性质是__ (填写编号)。
①氧化性 ②还原性 ③酸性 ④碱性
(3)若反应生成0.1molCl2,则转移的电子数为__ 。
(4)ClO2具有很强的氧化性。因此,常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)1kgClO2相当于___ kgCl2。(提示:Cl2和ClO2在消毒过程中均变为Cl-)
(1)请完成该过程的化学方程式并配平。
(2)浓盐酸在反应中显示出来的性质是
①氧化性 ②还原性 ③酸性 ④碱性
(3)若反应生成0.1molCl2,则转移的电子数为
(4)ClO2具有很强的氧化性。因此,常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)1kgClO2相当于
19-20高一·全国·课时练习 查看更多[2]
更新时间:2019-09-26 17:23:00
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】汽车的方向盘和前排乘客座位前的仪表板内都有折叠安全气囊,该安全气囊中含有叠氮化钠( )、硝酸钾(
)、硝酸钾( )、二氧化硅(
)、二氧化硅( )粉等。完成下列填空:
)粉等。完成下列填空:
(1)关于 ,下列分析正确的是_______。
,下列分析正确的是_______。
(2)行驶的汽车发生有足够强度的意外碰撞时,碰撞传感器将激活特定的电路,放电使 迅速分解,生成Na并放出
迅速分解,生成Na并放出 ,写出
,写出 分解的化学方程式
分解的化学方程式_______ 。
(3)生成的Na与 发生二次反应:
发生二次反应: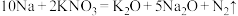 ,标出上式的单线桥:
,标出上式的单线桥:_______ ,其中生成2个氮气分子时,转移_______ 个电子,该反应的还原剂与氧化剂的个数比为_______ 。
 )、硝酸钾(
)、硝酸钾( )、二氧化硅(
)、二氧化硅( )粉等。完成下列填空:
)粉等。完成下列填空:(1)关于
 ,下列分析正确的是_______。
,下列分析正确的是_______。A. 电离需要通电 电离需要通电 |
B. 的焰色反应为蓝色 的焰色反应为蓝色 |
C.熔融状态的 中含自由移动的 中含自由移动的 和 和 |
D.固态 不导电,因其中不含 不导电,因其中不含 和 和 |
 迅速分解,生成Na并放出
迅速分解,生成Na并放出 ,写出
,写出 分解的化学方程式
分解的化学方程式(3)生成的Na与
 发生二次反应:
发生二次反应: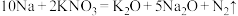 ,标出上式的单线桥:
,标出上式的单线桥:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧化还原反应在生产、生活和生命活动中起着十分重要的作用。例如,饮用水处理和污水净化问题中就广泛应用了氧化还原反应的原理。
I.高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为: 。
。
(1)在 中,
中, 的化合价为
的化合价为___________ 价;上述反应中,每生成 ,有
,有___________  电子转移。
电子转移。
(2)制备 的另外一种方法是在碱性条件下用
的另外一种方法是在碱性条件下用 和
和 反应,请写出相关的离子方程式:
反应,请写出相关的离子方程式:___________ 。
Ⅱ.含氯消毒剂在自来水净化过程中也起到了重要作用。
(3)很多自来水厂用氯气来杀菌、消毒,实验室不能用自来水配制硝酸银溶液,用离子方程式表示其原因___________ 。
(4)亚氯酸钠 是一种高效的漂白剂和氧化剂,其制备方法如下:
是一种高效的漂白剂和氧化剂,其制备方法如下: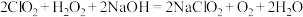 ,从上述反应中可知氧化性较强的是
,从上述反应中可知氧化性较强的是___________ (填“二氧化氯”或“氧气”)。
(5)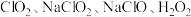 都常被用作消毒剂,上述物质消毒效率最高的是___________(填序号)。(已知:消毒效率是以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)
都常被用作消毒剂,上述物质消毒效率最高的是___________(填序号)。(已知:消毒效率是以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)
I.高铁酸钠
 是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为: 。
。(1)在
 中,
中, 的化合价为
的化合价为 ,有
,有 电子转移。
电子转移。(2)制备
 的另外一种方法是在碱性条件下用
的另外一种方法是在碱性条件下用 和
和 反应,请写出相关的离子方程式:
反应,请写出相关的离子方程式:Ⅱ.含氯消毒剂在自来水净化过程中也起到了重要作用。
(3)很多自来水厂用氯气来杀菌、消毒,实验室不能用自来水配制硝酸银溶液,用离子方程式表示其原因
(4)亚氯酸钠
 是一种高效的漂白剂和氧化剂,其制备方法如下:
是一种高效的漂白剂和氧化剂,其制备方法如下: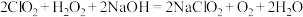 ,从上述反应中可知氧化性较强的是
,从上述反应中可知氧化性较强的是(5)
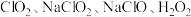 都常被用作消毒剂,上述物质消毒效率最高的是___________(填序号)。(已知:消毒效率是以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)
都常被用作消毒剂,上述物质消毒效率最高的是___________(填序号)。(已知:消毒效率是以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)A. | B. | C. | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】铝是一种重要金属:
(1)生产中曾用铝热反应(铝与铁的氧化物反应生成氧化铝和铁)焊接钢轨,则铝与磁性氧化铁发生反应的化学方程式为________________________ 。该反应中氧化剂是_______ ,还原剂是______ ,要得到1mol金属铁,需要铝的质量_____ g。
(2) 铝与NaOH溶液反应的离子方程式为:_________________ 。在同温同压下,等质量铝投入足量盐酸和NaOH溶液中,产生气体的体积之比为___ 。
(1)生产中曾用铝热反应(铝与铁的氧化物反应生成氧化铝和铁)焊接钢轨,则铝与磁性氧化铁发生反应的化学方程式为
(2) 铝与NaOH溶液反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】实验室用含有绿矾杂质的硫酸铜粗产品(含绿矾及不溶性杂质)制备纯净的胆矾,设计的实验步骤如下图所示。

已知溶液中A中加入H2O2,发生反应的离子方程式为___________ ,溶液B中加入NaOH溶液调到pH=4的目的是___________ ,操作Ⅰ是___________ ,操作Ⅱ是___________ 。

已知溶液中A中加入H2O2,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电化学脱硫技术是一种温和的净化技术,其基本原理为利用阳极反应产生的羟基自由基(·OH,氧元素为-1价)将燃煤中的含硫物质氧化除去,其装置示意图如图所示。
(1)将煤打成煤浆加入电解槽的目的是________ 。
(2)阳极的电极反应式为________ 。
(3)补全用羟基自由基除去煤中二硫化亚铁(FeS2)的反应的离子方程式:FeS2 +·OH =Fe3+ + SO42- + H2O +___ 。
(4)利用上述装置对某含FeS2的煤样品进行电解脱硫,测得一定时间内随溶液起始pH的改变脱硫率(溶于水中的硫元素质量占煤样中硫元素总质量的百分比)的变化如下图所示。
pH大于1.5后脱硫率下降的可能原因有:随着pH的升高,反应物的氧化性或还原性降低;________ 。

(1)将煤打成煤浆加入电解槽的目的是
(2)阳极的电极反应式为
(3)补全用羟基自由基除去煤中二硫化亚铁(FeS2)的反应的离子方程式:FeS2 +·OH =Fe3+ + SO42- + H2O +
(4)利用上述装置对某含FeS2的煤样品进行电解脱硫,测得一定时间内随溶液起始pH的改变脱硫率(溶于水中的硫元素质量占煤样中硫元素总质量的百分比)的变化如下图所示。

pH大于1.5后脱硫率下降的可能原因有:随着pH的升高,反应物的氧化性或还原性降低;
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
3FeS2+8O2 6SO2+Fe3O4,有3 molFeS2参加反应,转移
6SO2+Fe3O4,有3 molFeS2参加反应,转移_______ mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为_________ ;从腐蚀废液回收得到金属铜,还需要的试剂是_______________ 。
(3)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是____________________________
(4)钢铁的电化腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向___________________ 。
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
3FeS2+8O2
 6SO2+Fe3O4,有3 molFeS2参加反应,转移
6SO2+Fe3O4,有3 molFeS2参加反应,转移(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为
(3)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是
(4)钢铁的电化腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】阅读下面一段材料并回答问题。
(1) 中铁元素的化合价为
中铁元素的化合价为___________ 。
(2)制备 需要在
需要在___________ (填“酸性”、“碱性”或“中性”)环境中进行。
(3)下列关于 的说法中,
的说法中,不正确 的是___________ 。
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快、安全性好、无异味
(4)将 与水反应的化学方程式补充完整
与水反应的化学方程式补充完整___________ 。

| 高铁酸钾使用说明书 【化学式】  【性状】暗紫色具有金属光泽的粉末,无臭无味。 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着  减小,稳定性下降,与水反应放出氧气。 减小,稳定性下降,与水反应放出氧气。 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 与水反应还能产生具有强吸附性的 与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用。 胶体,可除去水中细微的悬浮物,有净水作用。【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理。 【用量】消毒净化  水投放 水投放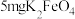 即可达到卫生标准。 即可达到卫生标准。…… |
 中铁元素的化合价为
中铁元素的化合价为(2)制备
 需要在
需要在(3)下列关于
 的说法中,
的说法中,a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快、安全性好、无异味
(4)将
 与水反应的化学方程式补充完整
与水反应的化学方程式补充完整
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】H2O2是在医疗、化工方面应用广泛的化学试剂。
(1)Na2O2、CaO2以及BaO2都可与酸作用生成过氧化氢,实验室通过上述某种过氧化物与适量稀硫酸作用,过滤后即可制得较纯净的H2O2溶液,则应选择的过氧化物是________ ;
(2)实验室可用H2O2与次氯酸钠反应制氧气,其中还原剂是__________ ,写出该反应的化学方程式____________________________ ,生成0.5mol氧气,转移电子_______ mol;
(3)用酸性高锰酸钾溶液滴定法可测定双氧水中H2O2的含量:
H2O2+KMnO4+H2SO4→MnSO4+K2SO4+O2↑+H2O,若滴定中消耗0.50mol/L的高锰酸钾溶液40.00ml,则此双氧水溶液中溶质的质量为____________ g。
(1)Na2O2、CaO2以及BaO2都可与酸作用生成过氧化氢,实验室通过上述某种过氧化物与适量稀硫酸作用,过滤后即可制得较纯净的H2O2溶液,则应选择的过氧化物是
(2)实验室可用H2O2与次氯酸钠反应制氧气,其中还原剂是
(3)用酸性高锰酸钾溶液滴定法可测定双氧水中H2O2的含量:
H2O2+KMnO4+H2SO4→MnSO4+K2SO4+O2↑+H2O,若滴定中消耗0.50mol/L的高锰酸钾溶液40.00ml,则此双氧水溶液中溶质的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知实验室制取氯气的反应原理为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,据此回答下列问题:
MnCl2+Cl2↑+2H2O,据此回答下列问题:
(1)该反应中氧化剂是__________ (填化学式)。
(2)用双线桥法表示电子转移的方向和数目:_______
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(3)有一种“地康法”制取氯气的反应原理如图所示:

①反应Ⅰ的离子方程式为________ 。
②工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟(为NH4Cl固体生成,同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式_________ 。
 MnCl2+Cl2↑+2H2O,据此回答下列问题:
MnCl2+Cl2↑+2H2O,据此回答下列问题:(1)该反应中氧化剂是
(2)用双线桥法表示电子转移的方向和数目:
MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O(3)有一种“地康法”制取氯气的反应原理如图所示:

①反应Ⅰ的离子方程式为
②工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟(为NH4Cl固体生成,同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式
您最近一年使用:0次



