有以下物质:
①石墨;②铝;③酒精;④氨水;⑤二氧化碳;⑥碳酸氢钠固体;⑦氯化铁溶液;⑧纯醋酸;⑨氧化钠固体;⑩氯化氢气体。
(1)其中能导电的是___ ;属于非电解质的是___ ;属于强电解质的是___ ;属于弱电解质的是___ 。
(2)写出物质⑥溶于水的电离方程式:____ 。
(3)写出物质⑥和⑧在水中反应的离子方程式:___ 。
(4)配制溶液⑦时通常将⑦先溶于___ ,然后再加水稀释,通过增加溶液中__ 的浓度以防止其发生水解。
(5)浓度、体积相同的⑧和⑩的溶液,加入相同形状且足量的Zn粒,反应速率快的是___ (填化学式);pH值、体积相同的⑧和⑩的溶液时,产生气体的量多的是___ 。(填化学式)
①石墨;②铝;③酒精;④氨水;⑤二氧化碳;⑥碳酸氢钠固体;⑦氯化铁溶液;⑧纯醋酸;⑨氧化钠固体;⑩氯化氢气体。
(1)其中能导电的是
(2)写出物质⑥溶于水的电离方程式:
(3)写出物质⑥和⑧在水中反应的离子方程式:
(4)配制溶液⑦时通常将⑦先溶于
(5)浓度、体积相同的⑧和⑩的溶液,加入相同形状且足量的Zn粒,反应速率快的是
更新时间:2019-09-29 21:40:30
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】25℃时部分弱电解质的电离常数如下表:
(1)①25℃时,pH相等的HCN、 、
、 物质的量浓度从大到小的顺序是
物质的量浓度从大到小的顺序是_______ 。
②下列反应方程式正确的是_______ 。
A.少量的 通入到NaClO溶液中:
通入到NaClO溶液中: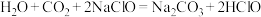
B.往 溶液中滴加少量
溶液中滴加少量 :
:
C.往 溶液中滴加过量HCN:
溶液中滴加过量HCN: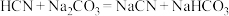
D.往 溶液中滴加HClO:
溶液中滴加HClO:
(2)25℃时,氨水与 的混合溶液
的混合溶液 ,该溶液中
,该溶液中 :
:
___________ 。
(3)请设计实验证明, 溶液中存在
溶液中存在 的电离平衡:
的电离平衡:_______ 。
| 物质 | HCN |  | HClO |  |  |
| 电离常数 | 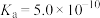 |  |  |   |  |
 、
、 物质的量浓度从大到小的顺序是
物质的量浓度从大到小的顺序是②下列反应方程式正确的是
A.少量的
 通入到NaClO溶液中:
通入到NaClO溶液中: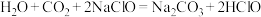
B.往
 溶液中滴加少量
溶液中滴加少量 :
:
C.往
 溶液中滴加过量HCN:
溶液中滴加过量HCN: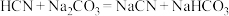
D.往
 溶液中滴加HClO:
溶液中滴加HClO:
(2)25℃时,氨水与
 的混合溶液
的混合溶液 ,该溶液中
,该溶液中 :
:
(3)请设计实验证明,
 溶液中存在
溶液中存在 的电离平衡:
的电离平衡:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】回答下列问题
(1)在体积都为1 L,pH都等于2的盐酸和醋酸溶液中,投入0.65 g锌粒,则如图所示符合客观事实的是___________
(2)25℃时,pH=2的盐酸和醋酸各1mL分别加水稀释,pH随溶液体积变化的曲线如下图所示。请回答如下问题
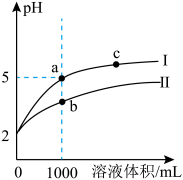
①曲线___________ (填“Ⅰ”或“Ⅱ”)代表盐酸的稀释过程
②a溶液的导电性比c溶液的导电性___________ (填“强”或“弱”)
③将a、b两溶液加热至30℃,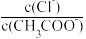
___________ (填“变大”、“变小”或“不变”)
④设稀释前的醋酸电离度为0.1%,醋酸的电离常数Ka=___________ 。
(1)在体积都为1 L,pH都等于2的盐酸和醋酸溶液中,投入0.65 g锌粒,则如图所示符合客观事实的是___________
A.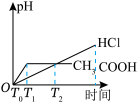 | B. |
C. | D. |

①曲线
②a溶液的导电性比c溶液的导电性
③将a、b两溶液加热至30℃,
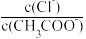
④设稀释前的醋酸电离度为0.1%,醋酸的电离常数Ka=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】请根据题目要求回答以下问题:
(1)CuSO4·5H2O的摩尔质量是__________ ; 0.1mol CH4含有的氢原子数为_____ ; 0.2 mol·L-1的 AlCl3溶液中Cl-的物质的量浓度是__________ 。
(2)现有以下物质:①NaCl ②氯水③醋酸 ④HCl ⑤酒精(C2H5OH)⑥CaCO3⑦Ba(OH)2属于强电解质的是__________ ,属于弱电解质的是____ 。(填序号),写出Ba(OH)2的电离方程式_________ .
(1)CuSO4·5H2O的摩尔质量是
(2)现有以下物质:①NaCl ②氯水③醋酸 ④HCl ⑤酒精(C2H5OH)⑥CaCO3⑦Ba(OH)2属于强电解质的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】下列物质能导电的是______ ;属于强电解质的是______ ;属于弱电解质的是____ ;属于非电解质的是______ .(填写字母)
a.铜丝 b.石墨 c.NaCl d.盐酸 e.蔗糖 f.CO2 g.Na2O h.冰醋酸 i.碳酸氢铵 j.氢氧化铝 k.氯气 m.BaSO4
a.铜丝 b.石墨 c.NaCl d.盐酸 e.蔗糖 f.CO2 g.Na2O h.冰醋酸 i.碳酸氢铵 j.氢氧化铝 k.氯气 m.BaSO4
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】I.物质的分离提纯操作包括:过滤、蒸馏、萃取、分液、结晶(重结晶)、盐析、渗析等,选择合适的操作名称填空:
(1)除去Ca(OH)2 溶液中悬浮的 CaCO3______
(2)从碘水中提取碘___
(3)用自来水制取蒸馏水_______________
(4)分离植物油和水_________
(5)除去KNO3晶体中混有的少量NaCl________ 。
II.今有10种物质:①Al ②稀硝酸 ③乙酸 ④液氨 ⑤CO2 ⑥NaCl ⑦BaSO4 ⑧Na2CO3 ⑨酒精 ⑩Al2O3
(1)属于电解质的是________
(2)属于非电解质的是________
(3)属于强电解质的是____________
(4)属于弱电解质的是________
(5)熔融状态下能导电的电解质是________
(1)除去Ca(OH)2 溶液中悬浮的 CaCO3
(2)从碘水中提取碘
(3)用自来水制取蒸馏水
(4)分离植物油和水
(5)除去KNO3晶体中混有的少量NaCl
II.今有10种物质:①Al ②稀硝酸 ③乙酸 ④液氨 ⑤CO2 ⑥NaCl ⑦BaSO4 ⑧Na2CO3 ⑨酒精 ⑩Al2O3
(1)属于电解质的是
(2)属于非电解质的是
(3)属于强电解质的是
(4)属于弱电解质的是
(5)熔融状态下能导电的电解质是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】现有以下物质:①NaCl晶体 ②盐酸 ③CaCO3固体 ④熔融KCl ⑤蔗糖 ⑥铜⑦CO2 ⑧冰醋酸 ⑨KOH固体 ⑩液氨
(1)以上物质中能导电的是___________________________ 。(填序号,下同)
(2)以上物质中属于电解质的是_____________________ ,强电解质的是_____________________ ,属于弱电解质的是__________________ ,属于非电解质的是___________________________ 。
(1)以上物质中能导电的是
(2)以上物质中属于电解质的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】常温下,等体积、等pH的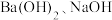 和
和 三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为
三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为 ,则三者的大小关系为
,则三者的大小关系为________ 。
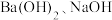 和
和 三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为
三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为 ,则三者的大小关系为
,则三者的大小关系为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】有pH均为2的盐酸、硫酸、醋酸三瓶溶液:
(1)设三种溶液的物质的量浓度依次为c1、c2、c3,则其关系是__________ (用“>、<、=”表示,下同)。
(2)取同体积的三种酸溶液分别加入足量的锌粉,反应开始放出H2的速率依次为a1、a2、a3,则其关系是_____________ ;反应过程中放出H2的速率依次为b1、b2、b3,则其关系是_________________
(3)完全中和体积和物质的量浓度均相同的三份NaOH溶液时,需三种酸的体积依次为V1、V2、V3,则其关系是________________ 。
(1)设三种溶液的物质的量浓度依次为c1、c2、c3,则其关系是
(2)取同体积的三种酸溶液分别加入足量的锌粉,反应开始放出H2的速率依次为a1、a2、a3,则其关系是
(3)完全中和体积和物质的量浓度均相同的三份NaOH溶液时,需三种酸的体积依次为V1、V2、V3,则其关系是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】根据所学知识回答问题
(1)25 ℃时,HF的Ka=6.4×10-4,则此温度下0.1 mol·L-1HF溶液的c(H+)为___________ mol·L-1。
(2)25 ℃时,a mol·L-1 CH3COOH溶液的pH=b,用含a和b的代数式表示CH3COOH的电离平衡常数Ka=___________ 。
(3)硒酸(H2SeO4)在水溶液中的电离如下:H2SeO4=H++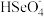 ,
,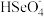
 H++
H++ ,K2=1.0×10-2(25 ℃)。
,K2=1.0×10-2(25 ℃)。
①向H2SeO4溶液中滴加少量氨水,该反应的离子方程式为___________ 。
②已知H2CO3的电离平衡常数Ka1=4.4×10-7,Ka2=4.7×10-11,则KHCO3和KHSeO4两溶液混合反应的离子方程式为___________ 。
(4)已知25 ℃时,Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13.现在该温度下将20 mL 0.1 mol·L-1 CH3COOH溶液和20 mL 0.1 mol·L-1 HSCN溶液分别与20 mL 0.1 mol·L-1 NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图所示,反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是______________________ 。
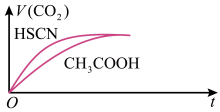
(5)已知25 ℃时,几种弱酸的电离平衡常数如下:HCOOH:Ka=1.77×10-4,HCN:Ka=4.9×10-10,H2CO3:Ka1=4.4×10-7,Ka2=4.7×10-11,则以下反应不能自发进行的是___________ (填字母)。
a.HCOOH+NaCN=HCOONa+HCN
b.NaHCO3+NaCN=Na2CO3+HCN
c.NaCN+H2O+CO2=HCN+NaHCO3
d.2HCOOH+ =2HCOO-+H2O+CO2↑
=2HCOO-+H2O+CO2↑
e.H2O+CO2+2CN-=2HCN+
(1)25 ℃时,HF的Ka=6.4×10-4,则此温度下0.1 mol·L-1HF溶液的c(H+)为
(2)25 ℃时,a mol·L-1 CH3COOH溶液的pH=b,用含a和b的代数式表示CH3COOH的电离平衡常数Ka=
(3)硒酸(H2SeO4)在水溶液中的电离如下:H2SeO4=H++
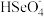 ,
,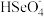
 H++
H++ ,K2=1.0×10-2(25 ℃)。
,K2=1.0×10-2(25 ℃)。①向H2SeO4溶液中滴加少量氨水,该反应的离子方程式为
②已知H2CO3的电离平衡常数Ka1=4.4×10-7,Ka2=4.7×10-11,则KHCO3和KHSeO4两溶液混合反应的离子方程式为
(4)已知25 ℃时,Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13.现在该温度下将20 mL 0.1 mol·L-1 CH3COOH溶液和20 mL 0.1 mol·L-1 HSCN溶液分别与20 mL 0.1 mol·L-1 NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图所示,反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是
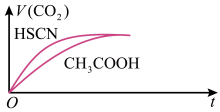
(5)已知25 ℃时,几种弱酸的电离平衡常数如下:HCOOH:Ka=1.77×10-4,HCN:Ka=4.9×10-10,H2CO3:Ka1=4.4×10-7,Ka2=4.7×10-11,则以下反应不能自发进行的是
a.HCOOH+NaCN=HCOONa+HCN
b.NaHCO3+NaCN=Na2CO3+HCN
c.NaCN+H2O+CO2=HCN+NaHCO3
d.2HCOOH+
 =2HCOO-+H2O+CO2↑
=2HCOO-+H2O+CO2↑e.H2O+CO2+2CN-=2HCN+

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】根据要求完成下列内容
(1)配制FeCl3溶液,为了防止发生水解,应加少量的____ ;
(2)配制Fe2(SO4)3溶液,为了防止发生水解,应加入少量的____ 。
(1)配制FeCl3溶液,为了防止发生水解,应加少量的
(2)配制Fe2(SO4)3溶液,为了防止发生水解,应加入少量的
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)氯化铁水解的离子方程式为_________________________________ ,实验室配制氯化铁溶液时,常将氯化铁先溶于浓盐酸,然后再加水稀释,其目的是_________________________ 。
(2)若向氯化铁溶液中加入碳酸钙粉末,碳酸钙逐渐逐渐溶解,并产生无色气体的离子方程式为________ ,溶液中同时有红褐色沉淀生成,其原因是______________ 。
(2)若向氯化铁溶液中加入碳酸钙粉末,碳酸钙逐渐逐渐溶解,并产生无色气体的离子方程式为
您最近一年使用:0次



