配平(1)(2);用双线桥法表示(3)(4)氧化还原反应的电子转移。
(1)( ) KI+( ) KIO3+( ) H2SO4—( ) I2+( ) K2SO4+( ) H2O
(2)( ) Cu2S + ( ) HNO3 — ( ) Cu(NO3)2 + ( ) H2SO4 + ( ) NO2↑+( ) H2O
(3)MnO2+4HCl(浓)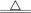 MnCl2+C12↑+2H2O
MnCl2+C12↑+2H2O______
(4)3S+6KOH=K2SO3+2K2S+3H2O_______
(1)
(2)
(3)MnO2+4HCl(浓)
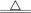 MnCl2+C12↑+2H2O
MnCl2+C12↑+2H2O(4)3S+6KOH=K2SO3+2K2S+3H2O
19-20高一上·河北承德·阶段练习 查看更多[2]
更新时间:2019-10-01 18:36:36
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】已知KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表述为2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
(1)请分析该反应中电子转移的情况(用双线桥表示)______ 。
(2)浓盐酸在反应中显示出来的性质是____ (填序号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)若标准状况下产生4.48LCl2,被氧化的盐酸的物质的量为___ mol,转移电子的物质的量_____ mol。
(1)请分析该反应中电子转移的情况(用双线桥表示)
(2)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)若标准状况下产生4.48LCl2,被氧化的盐酸的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据反应 8NH3 + 3Cl2 = N2 + 6NH4Cl,回答下列问题:
①用双线桥法标出该反应中电子转移的方向和数目:_____ .
②该反应中_____ 元素被还原,_____ 元素被氧化.
③氧化剂和还原剂的物质的量之比为_____ .
④在该反应中,若有 3mol 电子发生转移,在标准状况下,可生成N2的体积为_____ L.
①用双线桥法标出该反应中电子转移的方向和数目:
②该反应中
③氧化剂和还原剂的物质的量之比为
④在该反应中,若有 3mol 电子发生转移,在标准状况下,可生成N2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】高铁酸钾( 极易溶于水)是常见的水处理剂,其原理如图所示。
极易溶于水)是常见的水处理剂,其原理如图所示。
(1) 中铁元素的化合价为
中铁元素的化合价为___________ 价。
(2)过程①中活细菌表现了___________ (填“氧化”或“还原”)性。
(3)净水利用了 胶体聚沉作用,请写出
胶体聚沉作用,请写出 胶体制备化学方程式
胶体制备化学方程式___________ 。
(4)根据上述原理分析,作水处理剂时, 的作用有
的作用有___________ 和净水剂。
(5)还可用干法制备高铁酸钠,主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,(Na2O2中氧元素为-1价)该反应中还原剂是___________ 。(填化学式)
(6)已知铁与水蒸气发生如下反应: ,请用单线桥法表示电子转移的方向和数目:
,请用单线桥法表示电子转移的方向和数目:___________ ;该反应的还原产物是___________ 。
 极易溶于水)是常见的水处理剂,其原理如图所示。
极易溶于水)是常见的水处理剂,其原理如图所示。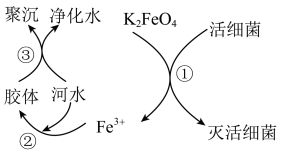
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)过程①中活细菌表现了
(3)净水利用了
 胶体聚沉作用,请写出
胶体聚沉作用,请写出 胶体制备化学方程式
胶体制备化学方程式(4)根据上述原理分析,作水处理剂时,
 的作用有
的作用有(5)还可用干法制备高铁酸钠,主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,(Na2O2中氧元素为-1价)该反应中还原剂是
(6)已知铁与水蒸气发生如下反应:
 ,请用单线桥法表示电子转移的方向和数目:
,请用单线桥法表示电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】2021年是国际化学年十周年,中国的宣传口号是“化学一我们的生活,我们的未来”。下列为生产生活中一些常见的化学反应。
(1)反应2Al+Fe2O3 2Fe+Al2O3可用于野外焊接钢轨。
2Fe+Al2O3可用于野外焊接钢轨。
①该反应属于四种基本反应类型中的_____ 。
②该反应中,发生氧化反应的是_____ (填化学式,下同),还原产物是_____ 。
(2)ClO2是世卫组织确认的A级新型高效消毒剂,其安全性远高于氯气。一种制备方法为2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O,其中氧化剂与还原剂的物质的量之比为_____ 。ClO2在杀菌消毒过程中会产生副产物亚氯酸盐( ),需将其转化为Cl-除去。下列试剂中可将
),需将其转化为Cl-除去。下列试剂中可将 ,转化为Cl-的是
,转化为Cl-的是_____ (填序号)。
A.FeSO4 B.O2 C.KMnO4 D.SO2
(3)小苏打(NaHCO3)可作为食品制作过程中的膨松剂。
①往饱和Na2CO3溶液中通入_____ (填化学式),过滤、干燥可得到NaHCO3。
②小苏打受热发生分解,产生的气体使面包松软,该反应的化学方程式为_____ 。
(1)反应2Al+Fe2O3
 2Fe+Al2O3可用于野外焊接钢轨。
2Fe+Al2O3可用于野外焊接钢轨。①该反应属于四种基本反应类型中的
②该反应中,发生氧化反应的是
(2)ClO2是世卫组织确认的A级新型高效消毒剂,其安全性远高于氯气。一种制备方法为2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O,其中氧化剂与还原剂的物质的量之比为
 ),需将其转化为Cl-除去。下列试剂中可将
),需将其转化为Cl-除去。下列试剂中可将 ,转化为Cl-的是
,转化为Cl-的是A.FeSO4 B.O2 C.KMnO4 D.SO2
(3)小苏打(NaHCO3)可作为食品制作过程中的膨松剂。
①往饱和Na2CO3溶液中通入
②小苏打受热发生分解,产生的气体使面包松软,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物,试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是( ) (填字母)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:________________________ 。
(3)Fe与过量稀硫酸反应可以制取FeSO4,若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是( ) (填字母)
A.Cl2 B.Fe C.H2O2 D.HNO3
请写离子方程式________________________ 。
(4)FeSO4可用于制备高铁酸钾(K2FeO4),写出在碱性条件下用FeSO4与NaClO反应制高铁酸钾的离子方程式:___________________ 。
①该反应中的还原剂是___________________ ,
②当有38g的FeSO4反应转移的电子数目为___________________ 。
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:
(3)Fe与过量稀硫酸反应可以制取FeSO4,若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
A.Cl2 B.Fe C.H2O2 D.HNO3
请写离子方程式
(4)FeSO4可用于制备高铁酸钾(K2FeO4),写出在碱性条件下用FeSO4与NaClO反应制高铁酸钾的离子方程式:
①该反应中的还原剂是
②当有38g的FeSO4反应转移的电子数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知反应4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3。
(1)在该反应中氧化剂是___ ,还原剂是___ ,1摩尔氧气完全参与反应,转移电子数目___ 。
(2)用双线桥标出该反应的电子转移方向及数目_____________ ,4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3。
(3)该反应中氧化剂与氧化产物的氧化性由强到弱的关系是__________ 。
(4)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3 + C+S = K2S + 2NO2↑ + CO2↑。其中被还原的元素是____ ,被氧化的元素是____ ,氧化剂是___ ,还原剂是____ ,氧化产物是____ ,还原产物是_______ 。
(1)在该反应中氧化剂是
(2)用双线桥标出该反应的电子转移方向及数目
(3)该反应中氧化剂与氧化产物的氧化性由强到弱的关系是
(4)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3 + C+S = K2S + 2NO2↑ + CO2↑。其中被还原的元素是
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐1】海水中含有非常丰富的化学资,从海水中可提取多种化工原料。下图是某工厂对海水资综合利用的示意图。

试回答下列问题:
(1)我国政府规定食用盐中必须加入一定量的KIO3(碘酸钾),其中碘元素的化合价为___________ 价。
(2)为除去粗盐中的Ca2+、Mg2+、SO 及泥沙,方法是将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量的氢氧化钠溶液;③加适量的盐酸;④加过量的碳酸钠溶液;⑤加过量的氯化钡溶液,合理的操作顺序是
及泥沙,方法是将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量的氢氧化钠溶液;③加适量的盐酸;④加过量的碳酸钠溶液;⑤加过量的氯化钡溶液,合理的操作顺序是___________ ①③(填序号)。
(3)写出电解饱和食盐水的化学方程式___________ ,当转移0.2mol电子时,阴阳两极生成的气体体积之和是___________ (标准状况下)。
(4)以海边贝壳为原料可以制取石灰乳,贝壳的主要化学成分为___________ (写化学式)。
(5)目前,世界上生产的镁有60%自海水,由“母液”制“镁”的过程中,发生了___________ 个复分解反应(填数目)。
(6)电解氯化镁所得的氯气,除用于生产盐酸外,还可以用于制取漂白粉,漂白粉的有效成分是___________ (写化学式)。
(7)溴主要以Br-形式存在于海水中,提取食盐后剩下的母液(也叫卤水)中,Br-的浓度较大,工业上 制备的Br2的操作步骤为:一定条件下,将Cl2通入卤水中,生成Br2,利用热空气将Br2吹出,Br2可用热空气吹出,其原因是___________ 。

试回答下列问题:
(1)我国政府规定食用盐中必须加入一定量的KIO3(碘酸钾),其中碘元素的化合价为
(2)为除去粗盐中的Ca2+、Mg2+、SO
 及泥沙,方法是将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量的氢氧化钠溶液;③加适量的盐酸;④加过量的碳酸钠溶液;⑤加过量的氯化钡溶液,合理的操作顺序是
及泥沙,方法是将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量的氢氧化钠溶液;③加适量的盐酸;④加过量的碳酸钠溶液;⑤加过量的氯化钡溶液,合理的操作顺序是(3)写出电解饱和食盐水的化学方程式
(4)以海边贝壳为原料可以制取石灰乳,贝壳的主要化学成分为
(5)目前,世界上生产的镁有60%自海水,由“母液”制“镁”的过程中,发生了
(6)电解氯化镁所得的氯气,除用于生产盐酸外,还可以用于制取漂白粉,漂白粉的有效成分是
(7)溴主要以Br-形式存在于海水中,提取食盐后剩下的母液(也叫卤水)中,Br-的浓度较大,工业上 制备的Br2的操作步骤为:一定条件下,将Cl2通入卤水中,生成Br2,利用热空气将Br2吹出,Br2可用热空气吹出,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】NaCN超标的电镀废水可用两段氧化法处理:
(1)NaCN与NaClO反应,生成NaOCN和NaCl
(2)NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
(1)第一次氧化时,溶液的pH应调节为_____ (选填“酸性”、“碱性”或“中性”);原因是__________ 。
(2)写出第二次氧化时发生反应的离子方程式_____________________ 。
(3)处理100 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO___ g(实际用量应为理论值的4倍),才能使NaCN含量低于0.5 mg/L,达到排放标准。
(4)(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成_________ 、__________ 和H2O。
(1)NaCN与NaClO反应,生成NaOCN和NaCl
(2)NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
(1)第一次氧化时,溶液的pH应调节为
(2)写出第二次氧化时发生反应的离子方程式
(3)处理100 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO
(4)(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成
您最近一年使用:0次
【推荐3】危化仓库中往往存有钠、钾、硫、白磷(P4)、硝酸铵和氰化钠(NaCN)等危险品。请回答下列问题:
(1)NH4NO3为爆炸物,在某温度下按下式进行分解:5NH4NO3=4N2↑+2HNO3+9H2O,则被氧化和被还原的氮元素质量之比为_____________ ;
(2)硫酸铜溶液是白磷引起中毒的一种解毒剂,1lP4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4,若6molH3PO4生成,则被CuSO4氧化的P4的物质的量为______________ mol;
(3)NaCN属于剧毒物质,有一种处理方法其原理为:CN-与S2O32-反应生成两种离子,一种与Fe3+可生成红色弱电解质,另一种与H+作用产生能使品红溶液腿色的刺激性气体,写出离子反应方程式:__________________ 。处理CN一还常用的一种方法是:用ClO一氧化处理生成CNO一,反应的离子方程式如下;aCN-+bClO-+ 2cOH一=dCNO-+eN2↑+fCO32-+bCl-+cH2O;上述化学方程式可能的配平化学计量数有多组,回答下列问题:
①方程式中e:f的值为_________ (填字母);
A.1 B.1/2 C.2 D.不能确定
②若d=e=l,则b=_________ 。
(1)NH4NO3为爆炸物,在某温度下按下式进行分解:5NH4NO3=4N2↑+2HNO3+9H2O,则被氧化和被还原的氮元素质量之比为
(2)硫酸铜溶液是白磷引起中毒的一种解毒剂,1lP4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4,若6molH3PO4生成,则被CuSO4氧化的P4的物质的量为
(3)NaCN属于剧毒物质,有一种处理方法其原理为:CN-与S2O32-反应生成两种离子,一种与Fe3+可生成红色弱电解质,另一种与H+作用产生能使品红溶液腿色的刺激性气体,写出离子反应方程式:
①方程式中e:f的值为
A.1 B.1/2 C.2 D.不能确定
②若d=e=l,则b=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】白色固体A,熔点182℃,摩尔质量76.12g∙mol-1,可代替氰化物用于提炼金的新工艺。A的合成方法有:
i.142°C下加热硫氰酸铵;
ii.CS2与氨反应;
iii.CaCN2和(NH4)2S水溶液反应(放出氨气)。
常温下,A在水溶液中可发生异构化反应,部分转化成B.酸性溶液中,A在氧化剂(如Fe3+、H2O2和O2)存在下能溶解金,形成取sp杂化的Au(I)配合物。
(1)画出A的结构式_______ 。
(2)分别写出合成A的方法ii、iii中化学反应的方程式______ 、________ 。
(3)画出B的结构式_______ 。
(4)写出A在硫酸铁存在下溶解金的离子方程式________ 。
(5)A和Au(I)形成的配合物中配位原子是________ 。
(6)在提炼金时,A可被氧化成C:2A→C+2e-;C能提高金的溶解速率。画出C的结构式______ 。写出C和Au反应的方程式_________ 。
i.142°C下加热硫氰酸铵;
ii.CS2与氨反应;
iii.CaCN2和(NH4)2S水溶液反应(放出氨气)。
常温下,A在水溶液中可发生异构化反应,部分转化成B.酸性溶液中,A在氧化剂(如Fe3+、H2O2和O2)存在下能溶解金,形成取sp杂化的Au(I)配合物。
(1)画出A的结构式
(2)分别写出合成A的方法ii、iii中化学反应的方程式
(3)画出B的结构式
(4)写出A在硫酸铁存在下溶解金的离子方程式
(5)A和Au(I)形成的配合物中配位原子是
(6)在提炼金时,A可被氧化成C:2A→C+2e-;C能提高金的溶解速率。画出C的结构式
您最近一年使用:0次
【推荐2】酸性KMnO4、H2O2、Fe(NO3)3是重要的氧化剂,用所学知识回答问题:
(1)3H2SO4+2KMnO4+5H2O2===K2SO4+2MnSO4+5O2↑+8H2O,当有6 mol H2SO4参加反应,有________ mol还原剂被氧化。
(2)在稀硫酸中,KMnO4与H2C2O4反应的离子方程式为__________________________
(3)Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,再变为棕黄色,溶液先变为浅绿色的离子方程式是_______________ ,再变为棕黄色的原因是_______________
(1)3H2SO4+2KMnO4+5H2O2===K2SO4+2MnSO4+5O2↑+8H2O,当有6 mol H2SO4参加反应,有
(2)在稀硫酸中,KMnO4与H2C2O4反应的离子方程式为
(3)Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,再变为棕黄色,溶液先变为浅绿色的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】二氧化硫是造成大气污染的主要有害气体之一,二氧化硫尾气处理的方法之一是采用钠一钙联合处理法。
第一步:用NaOH溶液吸收SO2。2NaOH+SO2=Na2SO3+H2O
第二步:将所得的Na2SO3溶液与生石灰反应。Na2SO3+CaO+ H2O=CaSO3↓+2NaOH
完成下列填空:
(1)在上述两步反应所涉及的短周期元素中,原子半径由小到大的顺序是_______ (用元素符号填写)。
(2)氧和硫属于同族元素,写出一个能比较氧元素和硫元素非金属性强弱的化学反应方程式:_______________________________________ 。
(3)NaOH的电子式为______________ 。
(4)若在第一步吸收SO2后得到的NaOH和Na2SO3混合溶液中,加入少许溴水,振荡后溶液变为无色,生成Na2SO4和NaBr。写出发生反应的化学方程式______________ 。
(5)钠一钙联合处理法的优点有________________ 。(任写一点即可)
第一步:用NaOH溶液吸收SO2。2NaOH+SO2=Na2SO3+H2O
第二步:将所得的Na2SO3溶液与生石灰反应。Na2SO3+CaO+ H2O=CaSO3↓+2NaOH
完成下列填空:
(1)在上述两步反应所涉及的短周期元素中,原子半径由小到大的顺序是
(2)氧和硫属于同族元素,写出一个能比较氧元素和硫元素非金属性强弱的化学反应方程式:
(3)NaOH的电子式为
(4)若在第一步吸收SO2后得到的NaOH和Na2SO3混合溶液中,加入少许溴水,振荡后溶液变为无色,生成Na2SO4和NaBr。写出发生反应的化学方程式
(5)钠一钙联合处理法的优点有
您最近一年使用:0次



