二氧化硫是造成大气污染的主要有害气体之一,二氧化硫尾气处理的方法之一是采用钠一钙联合处理法。
第一步:用NaOH溶液吸收SO2。2NaOH+SO2=Na2SO3+H2O
第二步:将所得的Na2SO3溶液与生石灰反应。Na2SO3+CaO+ H2O=CaSO3↓+2NaOH
完成下列填空:
(1)在上述两步反应所涉及的短周期元素中,原子半径由小到大的顺序是_______ (用元素符号填写)。
(2)氧和硫属于同族元素,写出一个能比较氧元素和硫元素非金属性强弱的化学反应方程式:_______________________________________ 。
(3)NaOH的电子式为______________ 。
(4)若在第一步吸收SO2后得到的NaOH和Na2SO3混合溶液中,加入少许溴水,振荡后溶液变为无色,生成Na2SO4和NaBr。写出发生反应的化学方程式______________ 。
(5)钠一钙联合处理法的优点有________________ 。(任写一点即可)
第一步:用NaOH溶液吸收SO2。2NaOH+SO2=Na2SO3+H2O
第二步:将所得的Na2SO3溶液与生石灰反应。Na2SO3+CaO+ H2O=CaSO3↓+2NaOH
完成下列填空:
(1)在上述两步反应所涉及的短周期元素中,原子半径由小到大的顺序是
(2)氧和硫属于同族元素,写出一个能比较氧元素和硫元素非金属性强弱的化学反应方程式:
(3)NaOH的电子式为
(4)若在第一步吸收SO2后得到的NaOH和Na2SO3混合溶液中,加入少许溴水,振荡后溶液变为无色,生成Na2SO4和NaBr。写出发生反应的化学方程式
(5)钠一钙联合处理法的优点有
更新时间:2018-07-20 12:06:37
|
相似题推荐
【推荐1】下图为铁元素的价类二维图,其中箭头表示部分物质间的转化关系(条件略去)。
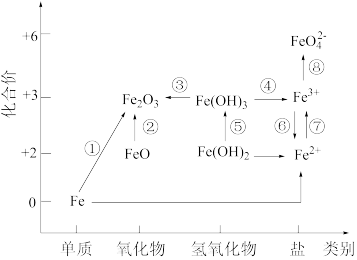
回答下列问题:
(1)工业上冶炼铁的主要方法是_______(填标号)。
(2)在潮湿的空气里,钢铁表面吸附了一薄层水膜,其中含有少量 、
、 、
、 等,它与钢铁里的铁和少量的
等,它与钢铁里的铁和少量的_______ (填化学式)形成了无数微小的原电池,使钢铁发生电化学腐蚀。
(3)检验 溶液中是否存在
溶液中是否存在 可选用的试剂是
可选用的试剂是_______ 。
(4)写出一个能实现图中转化⑦的离子方程式_______ 。
(5)高铁酸盐(含 )常用作杀菌消毒剂,从化合价的角度分析是因为其具有
)常用作杀菌消毒剂,从化合价的角度分析是因为其具有_______ 性(填“氧化”或“还原”)。用 与
与 在强碱性条件下可制取
在强碱性条件下可制取 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为_______ 。

回答下列问题:
(1)工业上冶炼铁的主要方法是_______(填标号)。
| A.热分解法 | B.高温还原法 | C.电解法 | D.物理富集法 |
 、
、 、
、 等,它与钢铁里的铁和少量的
等,它与钢铁里的铁和少量的(3)检验
 溶液中是否存在
溶液中是否存在 可选用的试剂是
可选用的试剂是(4)写出一个能实现图中转化⑦的离子方程式
(5)高铁酸盐(含
 )常用作杀菌消毒剂,从化合价的角度分析是因为其具有
)常用作杀菌消毒剂,从化合价的角度分析是因为其具有 与
与 在强碱性条件下可制取
在强碱性条件下可制取 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
【推荐2】磷化氢 、氧硫化碳
、氧硫化碳 均可作储粮害虫杀剂。请回答下列问题:
均可作储粮害虫杀剂。请回答下列问题:
(1)磷原子的核外电子排布式______ ,核外有___ 种不同能量的电子;其最外层有___ 种运动状态不同的电子,这些电子占据的轨道数为___ 个。
(2)氧硫化碳中,元素的非金属性最强的元素在周期表中的位置是______ ;已知 与
与 的结构相似,试写出
的结构相似,试写出 的电子式
的电子式_______________ , 属于
属于_____ 分子(填“极性”或“非极性”)。
(3)用硫酸铜溶液吸收 时的化学方程式为:
时的化学方程式为:
___  +
+___  +
+___  →
→___ 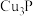 ↓+
↓+___  +
+____ 
(4)配平上述方程式,并标出电子转移方向与数目。
上述反应中氧化剂是______ ,当吸收 转移电子
转移电子______  。
。
氧硫化碳水解及部分应用流程如下(部分产物已略去):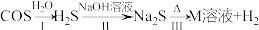
(5)写出反应Ⅱ的离子方程式:_________ ;
(6)若M溶液中硫元素的存在形式为 ,则反应Ⅲ的离子方程式为
,则反应Ⅲ的离子方程式为_________ 。
 、氧硫化碳
、氧硫化碳 均可作储粮害虫杀剂。请回答下列问题:
均可作储粮害虫杀剂。请回答下列问题:(1)磷原子的核外电子排布式
(2)氧硫化碳中,元素的非金属性最强的元素在周期表中的位置是
 与
与 的结构相似,试写出
的结构相似,试写出 的电子式
的电子式 属于
属于(3)用硫酸铜溶液吸收
 时的化学方程式为:
时的化学方程式为: +
+ +
+ →
→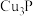 ↓+
↓+ +
+
(4)配平上述方程式,并标出电子转移方向与数目。
上述反应中氧化剂是
 转移电子
转移电子 。
。氧硫化碳水解及部分应用流程如下(部分产物已略去):
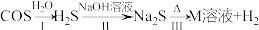
(5)写出反应Ⅱ的离子方程式:
(6)若M溶液中硫元素的存在形式为
 ,则反应Ⅲ的离子方程式为
,则反应Ⅲ的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。
(1)氯原子的结构示意图_____ ;工业上利用电解饱和食盐水来获得氯气,其化学方程式为_____ 。
(2)将氯气通入石灰乳中可制取漂白粉,化学方程式为_____ 。漂白粉溶于水后,和空气中的二氧化碳作用,所得的溶液可用于漂白这是利用生成的 HClO,而该溶液长时间放置又会失去漂白能力,所涉及的化学反应方程式为_____ 。
(3)向盛有 KI 溶液的试管中加入少许 CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4 层会逐渐变浅,最后变成无色。
完成下列填空:
(a)写出并配平 CCl4层由紫色变成无色的化学反应方程式,并用“单线桥”标出电子转移的方向和数目。_____________
_____ +_____ +_____ →_____ HIO3+_____ 该反应中,_____ 元素的化合价升高。
(b)把 KI 换成 KBr,则 CCl4层变为_____ 色,继续滴加氯水,CCl4 层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是_____ 。
(c)加碘盐中含碘量为 20mg~50mg/kg。制取加碘盐(含 KIO3 的食盐)1000kg,若 KI 与 Cl2 反应之 KIO3,至少需要消耗 Cl2_____ mol(保留 2 位小数)。
(1)氯原子的结构示意图
(2)将氯气通入石灰乳中可制取漂白粉,化学方程式为
(3)向盛有 KI 溶液的试管中加入少许 CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4 层会逐渐变浅,最后变成无色。
完成下列填空:
(a)写出并配平 CCl4层由紫色变成无色的化学反应方程式,并用“单线桥”标出电子转移的方向和数目。
(b)把 KI 换成 KBr,则 CCl4层变为
(c)加碘盐中含碘量为 20mg~50mg/kg。制取加碘盐(含 KIO3 的食盐)1000kg,若 KI 与 Cl2 反应之 KIO3,至少需要消耗 Cl2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,表中的每个编号表示一种元素,请根据要求回答问题

(1)⑤和⑥两种元素的原子半径大小是⑤____ ⑥(填“<"或“>”);
(2)由①和②两种元素组成的最简单化合物的化学式是________ ;
(3)⑥的单质与⑤的最高价氧化物的水化物的水溶液反应的化学方程式为____________ 。

(1)⑤和⑥两种元素的原子半径大小是⑤
(2)由①和②两种元素组成的最简单化合物的化学式是
(3)⑥的单质与⑤的最高价氧化物的水化物的水溶液反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据题意,完成下列填空:
(1)基态铜离子的核外电子排布式为___________ ,
(2)通常制造的农药含元素F、P、S、Cl,四种元素的电负性从大到小的顺序为___________ ;第一电离能从大到小的顺序为___________ 。
(3)第二周期中,第一电离能介于B和N之间的元素共有___________ 种。
(4)第四周期中,原子核外电子排布有两个未成对电子的元素有___________ 种。
(5)向FeCl3溶液中滴加NaHCO3溶液,有沉淀和气体生成的离子方程式___________ 。
(1)基态铜离子的核外电子排布式为
(2)通常制造的农药含元素F、P、S、Cl,四种元素的电负性从大到小的顺序为
(3)第二周期中,第一电离能介于B和N之间的元素共有
(4)第四周期中,原子核外电子排布有两个未成对电子的元素有
(5)向FeCl3溶液中滴加NaHCO3溶液,有沉淀和气体生成的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】锂离子电池在生产生活中应用广泛,LiFePO4、LiPF6和LiAsF6均可作锂离子电池的电极材料。回答下列问题:
(1)基态锂原子的轨道表达式为_______ 。
(2)O2-和F-半径更大的是_______ ;O、F、Fe的第一电离能由大到小的顺序为_______ 。
(3)H3AsO4的酸性强于H3AsO3的原因为_______ 。
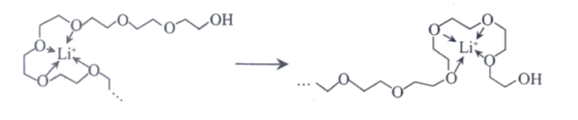
(4)锂离子电池工作时,Li+可在离子导体中迁移。Li+沿聚乙二醇分子中的碳氧链迁移的过程如图所示,该迁移过程属于_______ (填“物理变化”或“化学变化”)。
(5)以LiPF6和LiAsF6作锂离子电池的负极材料时,放电过程的实质是Li+从负极材料脱嵌。相同条件下,Li+更易在_______ (填“LiPF6”或“LiAsF6”)电极中脱嵌,解释其原因为_______ 。
(1)基态锂原子的轨道表达式为
(2)O2-和F-半径更大的是
(3)H3AsO4的酸性强于H3AsO3的原因为
(4)锂离子电池工作时,Li+可在离子导体中迁移。Li+沿聚乙二醇分子中的碳氧链迁移的过程如图所示,该迁移过程属于

(5)以LiPF6和LiAsF6作锂离子电池的负极材料时,放电过程的实质是Li+从负极材料脱嵌。相同条件下,Li+更易在
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
(1)有下列物质① ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥ ,其中含非极性键的离子化合物有
,其中含非极性键的离子化合物有________ (用物质前的序号填空,下同),只含共价键的物质有______ ,熔化时只破坏范德华力的是____________ 。
(2)硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图,图2是硫元素的“价类二维图”,回答下列问题: 均为图1中的物质,写出X与Y反应的化学方程式
均为图1中的物质,写出X与Y反应的化学方程式__________ 。
②芒硝的化学式为_________ 。
③工业制硫酸时, 参与的化学方程式为
参与的化学方程式为______________ 。
(3)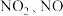 是大气污染物的主要成分,可以用
是大气污染物的主要成分,可以用 溶液吸收,当
溶液吸收,当 与
与 的体积比为
的体积比为 时,所得
时,所得 与
与 的物质的量之比为
的物质的量之比为_________ .用 也能处理
也能处理 和
和 ,反应原理如图所示,当
,反应原理如图所示,当 与
与 的物质的量之比为
的物质的量之比为 ,写出相应的化学方程式
,写出相应的化学方程式______ 。
(1)有下列物质①
 ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥ ,其中含非极性键的离子化合物有
,其中含非极性键的离子化合物有(2)硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图,图2是硫元素的“价类二维图”,回答下列问题:

 均为图1中的物质,写出X与Y反应的化学方程式
均为图1中的物质,写出X与Y反应的化学方程式②芒硝的化学式为
③工业制硫酸时,
 参与的化学方程式为
参与的化学方程式为(3)
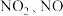 是大气污染物的主要成分,可以用
是大气污染物的主要成分,可以用 溶液吸收,当
溶液吸收,当 与
与 的体积比为
的体积比为 时,所得
时,所得 与
与 的物质的量之比为
的物质的量之比为 也能处理
也能处理 和
和 ,反应原理如图所示,当
,反应原理如图所示,当 与
与 的物质的量之比为
的物质的量之比为 ,写出相应的化学方程式
,写出相应的化学方程式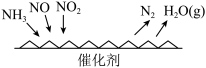
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有下列几种物质:a.Na2O2b.CH3COOH c.NH4Cld.CO2e. NaOHf.Si。请回答下列问题:
(1)属于共价化合物的是___________ (填写编号,下同);含有非极性共价键的离子化合物是___________ 。
(2)NH4Cl溶于水需要破坏___________ (填写一种作用力名称,下同),干冰升华需要破坏___________ 。
(3)写出 CH3COOH 溶于水的电离方程式___________ 。
(4)试比较 d、e、f 三种晶体的熔点由高到低的顺序:___________ 。(填写编号)
(1)属于共价化合物的是
(2)NH4Cl溶于水需要破坏
(3)写出 CH3COOH 溶于水的电离方程式
(4)试比较 d、e、f 三种晶体的熔点由高到低的顺序:
您最近一年使用:0次



