研究化学反应是为了更好地利用化学反应。回答下列问题:
(1)在①置换反应 ②化合反应 ③分解反应 ④复分解反应四种基本反应类型中,一定属于氧化还原反应的是____ (填标号)。
(2)在下列反应中:K2Cr2O7+14HCl==2KCl+2CrCl3+3Cl2↑+7H2O,___ 是氧化剂,___ 元素被氧化,___ 是还原产物,___ 是氧化产物。用双线桥标明电子转移的方向和数目:____ 。
K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O
(1)在①置换反应 ②化合反应 ③分解反应 ④复分解反应四种基本反应类型中,一定属于氧化还原反应的是
(2)在下列反应中:K2Cr2O7+14HCl==2KCl+2CrCl3+3Cl2↑+7H2O,
K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O
更新时间:2019-10-18 12:08:50
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氧化剂和还原剂在生产生活中广泛使用。
(1)高锰酸钾和氢溴酸溶液可以发生如下反应:2KMnO4+16HBr=2KBr+2MnBr2+8H2O+5Br2
①其中还原剂为_________ ,还原产物为_________ (均填化学式)
②若消耗0.1mol氧化剂,则被氧化的还原剂的物质的量为_________ ,转移电子的数目是_________ 。
③用线桥表示转移电子的数目_________________________________ 。
(2)人体内所含铁元素以Fe2+和Fe3+的形式存在。市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为____________________ ,但Fe2+在酸性条件下很容易被空气中的氧气氧化,写出该反应的离子方程式_________________________________ 。
(3)次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而用于化学镀银。利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4︰1,则氧化产物为:_________ 。
A.PH3 B.H3PO3 C.P D.H3PO4
(1)高锰酸钾和氢溴酸溶液可以发生如下反应:2KMnO4+16HBr=2KBr+2MnBr2+8H2O+5Br2
①其中还原剂为
②若消耗0.1mol氧化剂,则被氧化的还原剂的物质的量为
③用线桥表示转移电子的数目
(2)人体内所含铁元素以Fe2+和Fe3+的形式存在。市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为
(3)次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而用于化学镀银。利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4︰1,则氧化产物为:
A.PH3 B.H3PO3 C.P D.H3PO4
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】高铁酸钾( )是一种新型,高效,多功能绿色消毒剂.比
)是一种新型,高效,多功能绿色消毒剂.比 、
、 、
、 、
、 氧化性更强,无二次污染,主要用于饮用水的处理.工业上先制得高铁酸钠.然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出.
氧化性更强,无二次污染,主要用于饮用水的处理.工业上先制得高铁酸钠.然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出.
(1)湿法制备高铁酸钾( )的反应体系中有六种微粒:
)的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 .写出湿法制备高铁酸钾的离子反应方程式并用双线桥标出电子转移的方向和数目
.写出湿法制备高铁酸钾的离子反应方程式并用双线桥标出电子转移的方向和数目______________ 氧化性:NaClO____________  (填“大于”或“小于”).
(填“大于”或“小于”).
(2)干法制备高铁酸钠的主要反应为: .
.
①该反应中的氧化产物是__________ ,每生成1个 转移
转移__________ 个 .
.
②简要说明 作为水处理剂时所起的作用:
作为水处理剂时所起的作用:__________________________ .
 )是一种新型,高效,多功能绿色消毒剂.比
)是一种新型,高效,多功能绿色消毒剂.比 、
、 、
、 、
、 氧化性更强,无二次污染,主要用于饮用水的处理.工业上先制得高铁酸钠.然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出.
氧化性更强,无二次污染,主要用于饮用水的处理.工业上先制得高铁酸钠.然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出.(1)湿法制备高铁酸钾(
 )的反应体系中有六种微粒:
)的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 .写出湿法制备高铁酸钾的离子反应方程式并用双线桥标出电子转移的方向和数目
.写出湿法制备高铁酸钾的离子反应方程式并用双线桥标出电子转移的方向和数目 (填“大于”或“小于”).
(填“大于”或“小于”).(2)干法制备高铁酸钠的主要反应为:
 .
.①该反应中的氧化产物是
 转移
转移 .
.②简要说明
 作为水处理剂时所起的作用:
作为水处理剂时所起的作用:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】填空。
(1)宋代的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理为 ,则
,则 的化学式是
的化学式是______ ,其中 在该反应中
在该反应中________ (填字母)。
A.作氧化剂 B.作还原剂
C.既是氢化剂又是还原剂 D.既不是氧化剂又不是还原剂
(2)实现下列反应必须需要加入氧化剂的是_________ ,需要加入还原剂的是_________ ,
A. B.
B. C.
C.
D. E.
E. F.
F.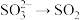
G. H.
H.
(3)氢化钠( )广泛应用于工业生产,回答下列问题。
)广泛应用于工业生产,回答下列问题。
①氢化钠( )中氢元素的化合价为
)中氢元素的化合价为___________ 。
② 能与水剧烈反应:
能与水剧烈反应: ,该反应中的氧化剂是
,该反应中的氧化剂是___________ ,氧化剂与还原剂的量之比是___________ 。
③在高温下氢化钠( )可将四氯化钛(
)可将四氯化钛( )还原成金属钛,该反应的化学方程式为
)还原成金属钛,该反应的化学方程式为________ 。
(4)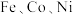 能与
能与 反应,其中
反应,其中 和
和 均生成二氯化物,由此推断
均生成二氯化物,由此推断 和
和 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为________ , 与盐酸反应有
与盐酸反应有 气体生成,写出反应的离子方程式:
气体生成,写出反应的离子方程式:___________ 。
(5)在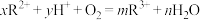 的离子方程式中,对系数
的离子方程式中,对系数 和
和 、
、 判断正确的是___________(填字母)。
判断正确的是___________(填字母)。
(1)宋代的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理为
 ,则
,则 的化学式是
的化学式是 在该反应中
在该反应中A.作氧化剂 B.作还原剂
C.既是氢化剂又是还原剂 D.既不是氧化剂又不是还原剂
(2)实现下列反应必须需要加入氧化剂的是
A.
 B.
B. C.
C.
D.
 E.
E. F.
F.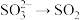
G.
 H.
H.
(3)氢化钠(
 )广泛应用于工业生产,回答下列问题。
)广泛应用于工业生产,回答下列问题。①氢化钠(
 )中氢元素的化合价为
)中氢元素的化合价为②
 能与水剧烈反应:
能与水剧烈反应: ,该反应中的氧化剂是
,该反应中的氧化剂是③在高温下氢化钠(
 )可将四氯化钛(
)可将四氯化钛( )还原成金属钛,该反应的化学方程式为
)还原成金属钛,该反应的化学方程式为(4)
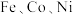 能与
能与 反应,其中
反应,其中 和
和 均生成二氯化物,由此推断
均生成二氯化物,由此推断 和
和 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为 与盐酸反应有
与盐酸反应有 气体生成,写出反应的离子方程式:
气体生成,写出反应的离子方程式:(5)在
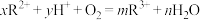 的离子方程式中,对系数
的离子方程式中,对系数 和
和 、
、 判断正确的是___________(填字母)。
判断正确的是___________(填字母)。A. , , 是还原剂 是还原剂 | B.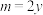 , , 被氧化 被氧化 |
C. , , 是氧化剂 是氧化剂 | D. , , 是还原剂 是还原剂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.根据所学知识,完成下列问题
(1)下列古诗词描述的场景中发生的化学反应不属于氧化还原反应的是_______
(2)下列反应不属于四种基本反应类型,但属于氧化还原反应的是_______
(3)某元素在化学反应中由化合态变为游离态,则该元素_______
Ⅱ实验室可用高锰酸钾与盐酸反应制得氯气,其反应的化学方程式:
(4)被氧化的元素是___________ ,被还原的元素是___________ ,发生氧化反应的物质是___________ ,发生还原反应的物质是___________ 。
(5)用单线桥法表示反应电子得失的方向和数目:___________ 。
(1)下列古诗词描述的场景中发生的化学反应不属于氧化还原反应的是_______
| A.爆竹声中一岁除——黑火药受热爆炸 | B.烈火焚烧若等闲——石灰石分解 |
| C.蜡炬成灰泪始干——石蜡的燃烧 | D.炉火照天地,红星乱紫烟——铁的冶炼 |
A.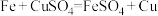 |
B. |
C. |
D.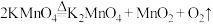 |
| A.一定得到电子 | B.一定失去电子 |
| C.可能被氧化也可能被还原 | D.无法判断 |
Ⅱ实验室可用高锰酸钾与盐酸反应制得氯气,其反应的化学方程式:

(4)被氧化的元素是
(5)用单线桥法表示反应电子得失的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)虽然分类的方法不同,但四种基本反应和离子反应、氧化还原反应之间也存在着一定的关系。如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是___ (填字母)。

(2)利用氧化还原反应原理配平如下方程式:___
____NH3+____O2 ____NO+____H2O
____NO+____H2O
(3)用单线桥法标出如下反应的电子转移的方向和数目:___ 。
Cl2+SO2+2H2O=H2SO4+2HCl
(1)虽然分类的方法不同,但四种基本反应和离子反应、氧化还原反应之间也存在着一定的关系。如图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

(2)利用氧化还原反应原理配平如下方程式:
____NH3+____O2
 ____NO+____H2O
____NO+____H2O(3)用单线桥法标出如下反应的电子转移的方向和数目:
Cl2+SO2+2H2O=H2SO4+2HCl
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】有以下6个反应(反应条件略):
A. 2Na + 2H2O ==2NaOH + H2↑ B. CH4 + 2O2==CO2 + 2H2O
C. KClO3==2KCl + 3O2↑ D. CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
E. Na2O+CO2==Na2CO3 F. CO2+C==2CO
属于化合反应的有________ (填编号,下同),属于分解反应的有____________ ,属于复分解反应的有_________ ,属于置换反应的有________ ,属于氧化还原反应的有___________ 。
A. 2Na + 2H2O ==2NaOH + H2↑ B. CH4 + 2O2==CO2 + 2H2O
C. KClO3==2KCl + 3O2↑ D. CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
E. Na2O+CO2==Na2CO3 F. CO2+C==2CO
属于化合反应的有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知铜在常温下能被稀HNO3溶解,反应为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
(1)请将上述反应改写成离子方程式:___________ 。
(2)上述反应中,被还原的物质是___________ (填化学式,下同),发生氧化反应的物质是___________ 。
(3)用双线桥法标出该反应的电子转移情况:___________ 。
(1)请将上述反应改写成离子方程式:
(2)上述反应中,被还原的物质是
(3)用双线桥法标出该反应的电子转移情况:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学是一门以实验为基础的自然科学。
(1)下列说法中,符合实验规范要求的是_______ (填序号)。
①闻气体的气味时,应用手在瓶口轻轻煽动,使少量的气体飘进鼻孔
②在实验室做二氧化锰和浓盐酸反应制备氯气的实验时,应该在通风橱中进行
③实验中当有少量的钠剩余时,用纸包裹好后将其放入垃圾桶中
④用容量瓶稀释某一浓度的硫酸溶液
(2)将某碳酸钠和碳酸氢钠的混合物 2.74g 加热到质量不再变化时,剩余物质的质量为 2.12g。混合物中碳酸氢钠与碳酸钠的物质的量之比_______ ;
(3)i.用毛笔蘸取少量30%的FeCl3溶液在铜片上写一个“Cu”,放置片刻后用少量蒸馏水冲洗铜片后,在铜片上会出现凹凸的“Cu”。
ii. Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O。
①写出i中反应的离子方程式:_______ 。
②反应ii中氧化剂与还原剂的物质的量之比为_______ ,用双线桥法标出电子转移的方向与数目:_______ ,当反应中有0.6 mol电子转移时,生成NO的体积为_______ L(标准状况)。
(1)下列说法中,符合实验规范要求的是
①闻气体的气味时,应用手在瓶口轻轻煽动,使少量的气体飘进鼻孔
②在实验室做二氧化锰和浓盐酸反应制备氯气的实验时,应该在通风橱中进行
③实验中当有少量的钠剩余时,用纸包裹好后将其放入垃圾桶中
④用容量瓶稀释某一浓度的硫酸溶液
(2)将某碳酸钠和碳酸氢钠的混合物 2.74g 加热到质量不再变化时,剩余物质的质量为 2.12g。混合物中碳酸氢钠与碳酸钠的物质的量之比
(3)i.用毛笔蘸取少量30%的FeCl3溶液在铜片上写一个“Cu”,放置片刻后用少量蒸馏水冲洗铜片后,在铜片上会出现凹凸的“Cu”。
ii. Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O。
①写出i中反应的离子方程式:
②反应ii中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
(1)该反应中的还原剂是____________ 。
(2)该反应中,发生还原反应的过程是______________ →______________ 。
(3)写出该反应的化学方程式,并用双线桥法标出电子转移的方向和数目:__________ 。
(4)若反应转移了0.3 mol电子,则产生的气体在标准状况下体积为__________ L。
(1)该反应中的还原剂是
(2)该反应中,发生还原反应的过程是
(3)写出该反应的化学方程式,并用双线桥法标出电子转移的方向和数目:
(4)若反应转移了0.3 mol电子,则产生的气体在标准状况下体积为
您最近一年使用:0次



