I.(1)指出如下图实验装置中的错误之处(加热装置中烧杯底部已垫有石棉网)
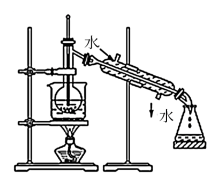
①_______ ;
②_______ 。
(2)图是某学生的过滤操作示意图,其操作不规范的是_______
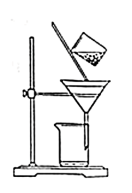
a.漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
II.海藻中提取碘的流程如图,已知②中发生反应的化学方程式为:Cl2+2KI=2KCl+I2.请回答下列问题:
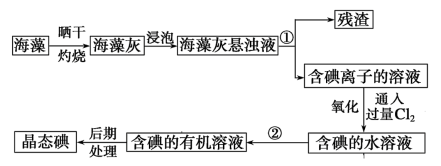
(1)指出提取碘的过程中有关实验操作①和②的名称:_______ ;_______ 。
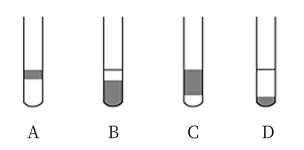
(2)在3 mL含碘的水溶液中加入1mL四氯化碳,振荡静置后观察到试管里的分层现象是上图中的_______ (注:试管中深色区为有色溶液),上层无色溶液的溶质是_______ 下层颜色是_______ 。
(3)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过的操作是_______ 。
III.某溶液中含有MgSO4和Na2SO4两种溶质,选择适当试剂将溶液中的镁离子转化为沉淀或固体分离出来,设计实验流程如下:
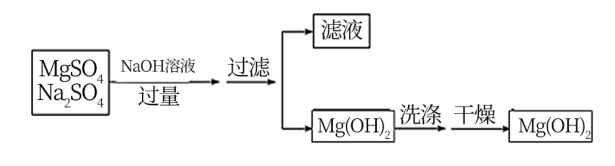
欲证明滤液中存在 、OH-,选用的方案是先取少量的滤液滴加
、OH-,选用的方案是先取少量的滤液滴加_______ ,发现溶液变红,再向其中加入_______ 溶液,出现白色沉淀,则可证明 、OH-,均存在。
、OH-,均存在。

①
②
(2)图是某学生的过滤操作示意图,其操作不规范的是

a.漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
II.海藻中提取碘的流程如图,已知②中发生反应的化学方程式为:Cl2+2KI=2KCl+I2.请回答下列问题:


(1)指出提取碘的过程中有关实验操作①和②的名称:
(2)在3 mL含碘的水溶液中加入1mL四氯化碳,振荡静置后观察到试管里的分层现象是上图中的
(3)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过的操作是
III.某溶液中含有MgSO4和Na2SO4两种溶质,选择适当试剂将溶液中的镁离子转化为沉淀或固体分离出来,设计实验流程如下:

欲证明滤液中存在
 、OH-,选用的方案是先取少量的滤液滴加
、OH-,选用的方案是先取少量的滤液滴加 、OH-,均存在。
、OH-,均存在。
更新时间:2019-11-03 13:10:05
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】肼(N2H4)是一种重要的工业产品。资料表明,氨和次氯酸钠溶液反应能生成肼,肼有极强的还原性。可用下图装置制取肼:

(1)写出肼的电子式__________ ,写出肼与硫酸反应可能生成的盐的化学式_______ ;
(2)装置A中反应的化学方程式_____ ;
(3)实验时,先点燃A处的酒精灯,一段时间后再向B的三口烧瓶中滴加NaClO溶液。滴加NaClO溶液时不能过快、过多的原因___________ ;
(4)从实验安全性角度指出该实验装置中存在的缺陷_______ 。
(5)准确量取20.00mL含肼溶液,加入硫酸和碳酸氢钠,用0.1000mol/L的标准碘液进行滴定,滴定终点时,消耗V0mL(在此过程中N2H4→N2)。该实验可选择______ 做指示剂;该溶液中肼的浓度为______ mol/L(用含V0的代数式表达,并化简)。

(1)写出肼的电子式
(2)装置A中反应的化学方程式
(3)实验时,先点燃A处的酒精灯,一段时间后再向B的三口烧瓶中滴加NaClO溶液。滴加NaClO溶液时不能过快、过多的原因
(4)从实验安全性角度指出该实验装置中存在的缺陷
(5)准确量取20.00mL含肼溶液,加入硫酸和碳酸氢钠,用0.1000mol/L的标准碘液进行滴定,滴定终点时,消耗V0mL(在此过程中N2H4→N2)。该实验可选择
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】测定反应Zn(s) + CuSO4(aq) = ZnSO4(aq) + Cu(s)的反应焓变ΔH值的实验步骤如下:
第1步,按下图装配简易量热计。
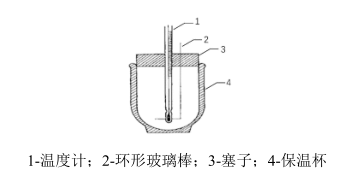
第2步,测定量热计的水当量(仪器常数) q: 取100.0 mL水加入保温杯,稳定后测量其温度(T1)。 再加入温度为T2的温水100.0 mL,仔细搅拌后测量其温度(T3)。 倒出瓶中的水并擦干内壁。
第3步,测定反应的热效应:将100.0 mL 0.200 mol·L-1硫酸铜溶液全部加入保温杯中,盖好插有温度计和搅拌棒的盖子;不断搅拌,每10 s测一次温度。温度稳定后迅速向溶液中加入3.0g锌粉,立即盖好盖子;不断搅拌,开始时每10s测一次温度,反应1 min后每30s测一次温度,温度上升到最高值后继续测2min。
请回答下列问题:
(1)为什么要用环形玻璃棒搅拌_______ ?是否可用铁丝代替环行玻璃棒_______ ?为什么_______ ?
(2)实验中,所用锌粉只需用台式天平称取,而CuSO4溶液的浓度与体积则要求比较准确,为什么_______ ?
(3)第2步测得的实验数据见下表:
已知水的比热容cp= 4.18 J/(g·K),水的密度ρ(H2O)=1.00 g·mL-1,可算出q = 56.0 J/K, 请列出q的计算式_______ (用字母表示)。
(4)根据第3步测得的实验数据可绘图如下:
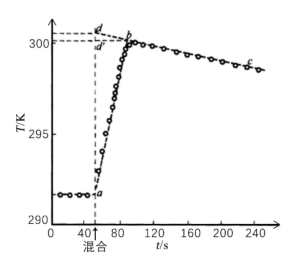
图中,a、dˊ、d点对应的温度分别为291.84、300.16、 300.50 K。反应后溶液的比热容cs可用水的比热容cp近似代替;反应后溶液的密度ρs可近似地取室温时0.200 mol·L -1 ZnSO4溶液的密度(1.03 g·mL-1)。
①图中,线段bc、 dd ˊ分别表示什么含义_______ 、_______ 。
②请计算题中所给反应的焓变ΔH=_______ 。
③加锌粉后,若温度计的水银球不小心跟保温杯壁接触,这对反应焓变的测定结果有什么影响_______ 。理由是_______ 。
第1步,按下图装配简易量热计。

第2步,测定量热计的水当量(仪器常数) q: 取100.0 mL水加入保温杯,稳定后测量其温度(T1)。 再加入温度为T2的温水100.0 mL,仔细搅拌后测量其温度(T3)。 倒出瓶中的水并擦干内壁。
第3步,测定反应的热效应:将100.0 mL 0.200 mol·L-1硫酸铜溶液全部加入保温杯中,盖好插有温度计和搅拌棒的盖子;不断搅拌,每10 s测一次温度。温度稳定后迅速向溶液中加入3.0g锌粉,立即盖好盖子;不断搅拌,开始时每10s测一次温度,反应1 min后每30s测一次温度,温度上升到最高值后继续测2min。
请回答下列问题:
(1)为什么要用环形玻璃棒搅拌
(2)实验中,所用锌粉只需用台式天平称取,而CuSO4溶液的浓度与体积则要求比较准确,为什么
(3)第2步测得的实验数据见下表:
| 项目 | 冷水体积V1/mL | 热水体积 V2/ mL | T1/K | T2/K | T3/ K |
| 数据 | 100.0 | 100.0 | 291.82 | 309.68 | 300.18 |
(4)根据第3步测得的实验数据可绘图如下:

图中,a、dˊ、d点对应的温度分别为291.84、300.16、 300.50 K。反应后溶液的比热容cs可用水的比热容cp近似代替;反应后溶液的密度ρs可近似地取室温时0.200 mol·L -1 ZnSO4溶液的密度(1.03 g·mL-1)。
①图中,线段bc、 dd ˊ分别表示什么含义
②请计算题中所给反应的焓变ΔH=
③加锌粉后,若温度计的水银球不小心跟保温杯壁接触,这对反应焓变的测定结果有什么影响
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】用如图测定常温下1molO2的体积。
提供试剂:二氧化锰、过氧化氢溶液。
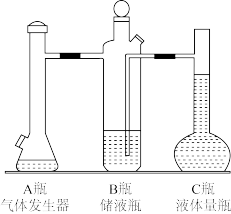
(1)气体发生器A中预先盛放的试剂是____ ,用注射器向A中注入的试剂是____ 。
(2)已知常温下O2摩尔体积为24.0L/mol,液体量瓶C的刻度范围是110-130mL,过氧化氢溶液取10.0mL,则H2O2溶液浓度(mol/L)范围可能是____ (保留三位有效数字)。
(3)现取0.90mol/L的过氧化氢溶液10.0mL,完全反应后且恢复室温,量瓶C中的读数为120.0mL,为保证储液瓶B的导管内外液面相平,又抽出了1.00mL气体,则室温下1mol氧气体积的测定值是____ L(保留三位有效数字)。
提供试剂:二氧化锰、过氧化氢溶液。

(1)气体发生器A中预先盛放的试剂是
(2)已知常温下O2摩尔体积为24.0L/mol,液体量瓶C的刻度范围是110-130mL,过氧化氢溶液取10.0mL,则H2O2溶液浓度(mol/L)范围可能是
(3)现取0.90mol/L的过氧化氢溶液10.0mL,完全反应后且恢复室温,量瓶C中的读数为120.0mL,为保证储液瓶B的导管内外液面相平,又抽出了1.00mL气体,则室温下1mol氧气体积的测定值是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】填空
(1)物质的量是高中化学常用的物理量,请完成有关填空:
①0.6molO2与0.4molO3的质量之比为_____ ,分子个数之比为________ 。
②5.6g铁单质与稀硫酸反应,产生H2的质量为________ g。
③标准状况下,2.2gCO2的体积为________ L。
(2)实验室用NaCl固体配制100mL1.00mol/L的NaCl溶液。
①需要用托盘天平称取NaCl固体_________ g。
②配制溶液时,必须用到的玻璃仪器有烧杯、玻璃棒、________ 。
③下列关于100mL容量瓶的操作,正确的是________ 。
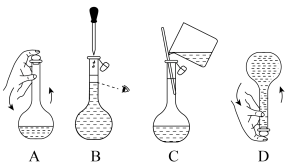
④用胶头滴管滴加蒸馏水至刻度线时,某同学俯视容量瓶上的刻度线,最后配成的溶液中NaCl的实际浓度比所要求的________ (填“偏大”或“偏小”)。
(1)物质的量是高中化学常用的物理量,请完成有关填空:
①0.6molO2与0.4molO3的质量之比为
②5.6g铁单质与稀硫酸反应,产生H2的质量为
③标准状况下,2.2gCO2的体积为
(2)实验室用NaCl固体配制100mL1.00mol/L的NaCl溶液。
①需要用托盘天平称取NaCl固体
②配制溶液时,必须用到的玻璃仪器有烧杯、玻璃棒、
③下列关于100mL容量瓶的操作,正确的是

④用胶头滴管滴加蒸馏水至刻度线时,某同学俯视容量瓶上的刻度线,最后配成的溶液中NaCl的实际浓度比所要求的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】欲用18.4mol·L-1的浓硫酸配制250 mL 0.2 mol·L-1的硫酸溶液,完成下列问题:
(1)所需的主要仪器有__________________________________________________ 。
(2)根据计算,所取18.4mol·L-1的浓硫酸的体积为________ mL,稀释浓硫酸的正确操作方法是____________________________________________________________ 。
(3)下列操作会使所配制硫酸浓度偏低的是________ 。
A.转移溶液时未洗涤烧杯与玻璃棒
B.容量瓶水洗后未干燥
C.定容时加水越过刻度线
D.定容时仰视刻度线
(1)所需的主要仪器有
(2)根据计算,所取18.4mol·L-1的浓硫酸的体积为
(3)下列操作会使所配制硫酸浓度偏低的是
A.转移溶液时未洗涤烧杯与玻璃棒
B.容量瓶水洗后未干燥
C.定容时加水越过刻度线
D.定容时仰视刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】硫酸是实验室常用化学试剂之一,用98%浓硫酸(18.4mol•L-1)配制100mL1mol•L-1的稀硫酸。
(1)实验步骤如下:
①用10mL量筒量取98%浓硫酸____ mL(保留一位小数)浓硫酸;
②取小烧杯,将____ 缓缓注入____ 中,边加边用玻璃棒搅拌;
③用玻璃棒引流,将溶液转入____ ;
④用蒸馏水洗涤____ 2~3次,将洗涤液一并转移;
⑤加水至刻度线2~3cm处,用胶头滴管滴加蒸馏水至刻度线;
⑥塞上容量瓶塞,摇匀;
⑦将配制好的溶液转移入含有少量蒸馏水的试剂瓶中,贴上标签,贮存备用。
(2)实验操作中缺少一步操作,请指出错误:____ 。
(3)下列操作对所配溶液的浓度有何影响?(填“偏高”“偏低”或“无影响”)
①浓硫酸较粘稠,有部分浓硫酸残留在量筒上____ 。
②配制溶液前容量瓶中有少量蒸馏水____ 。
③转移液体后,未进行洗涤操作____ 。
④定容时俯视容量瓶刻度线____ 。
⑤摇匀后,发现液面低于刻度线,继续滴加液体至相切____ 。
(4)正确配制溶液后,取所得溶液10mL。
①10mL溶液中硫酸的物质的量为____ 。
②10mL溶液中氢离子(H+)物质的量浓度为____ 。10mL溶液中硫酸根(SO )物质的量浓度为
)物质的量浓度为____ 。
③中和10mL稀硫酸,需要1mol•L-1的NaOH溶液的体积是___ 。
(1)实验步骤如下:
①用10mL量筒量取98%浓硫酸
②取小烧杯,将
③用玻璃棒引流,将溶液转入
④用蒸馏水洗涤
⑤加水至刻度线2~3cm处,用胶头滴管滴加蒸馏水至刻度线;
⑥塞上容量瓶塞,摇匀;
⑦将配制好的溶液转移入含有少量蒸馏水的试剂瓶中,贴上标签,贮存备用。
(2)实验操作中缺少一步操作,请指出错误:
(3)下列操作对所配溶液的浓度有何影响?(填“偏高”“偏低”或“无影响”)
①浓硫酸较粘稠,有部分浓硫酸残留在量筒上
②配制溶液前容量瓶中有少量蒸馏水
③转移液体后,未进行洗涤操作
④定容时俯视容量瓶刻度线
⑤摇匀后,发现液面低于刻度线,继续滴加液体至相切
(4)正确配制溶液后,取所得溶液10mL。
①10mL溶液中硫酸的物质的量为
②10mL溶液中氢离子(H+)物质的量浓度为
 )物质的量浓度为
)物质的量浓度为③中和10mL稀硫酸,需要1mol•L-1的NaOH溶液的体积是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2= Na2S2O5。
(1)装置Ⅰ中产生气体的化学方程式为______________________________ 。
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是________ 。
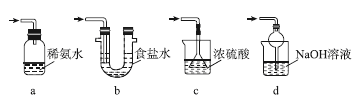
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为________ (填序号)。
实验二 焦亚硫酸钠的性质
已知:Na2S2O5溶于水即生成NaHSO3。
(4)检测Na2S2O5晶体在空气中已被氧化的实验方案是____________________ 。
实验一 焦亚硫酸钠的制取
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2= Na2S2O5。
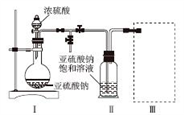
(1)装置Ⅰ中产生气体的化学方程式为
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为
实验二 焦亚硫酸钠的性质
已知:Na2S2O5溶于水即生成NaHSO3。
(4)检测Na2S2O5晶体在空气中已被氧化的实验方案是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性。将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,所需溶液的pH分别为6.4、6.4、3.7。现有含FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按图示步骤进行提纯:

请回答下列问题:
(1)本实验最适合的氧化剂X是________。
(2)物质Y是_______ 。
(3)本实验用加碱沉淀法_______ (填“能”或“不能”)达到目的,原因是_______ 。
(4)加氧化剂X发生的离子方程式:_______ 。
(5)除去Fe3+的有关化学方程式是:_______ 。
(6)加氧化剂的目的是_______ 。

请回答下列问题:
(1)本实验最适合的氧化剂X是________。
| A.K2Cr2O7 | B.NaClO | C.H2O2 | D.KMnO4 |
(3)本实验用加碱沉淀法
(4)加氧化剂X发生的离子方程式:
(5)除去Fe3+的有关化学方程式是:
(6)加氧化剂的目的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】氧化锌为白色粉末,可用于湿疹、癖等皮肤病的治疗。纯化工业级氧化锌[含有Fe(Ⅱ)、Mn(Ⅱ)、Ni(Ⅱ)等杂质]的流程如下:

提示:在本实验条件下,Ni(II)不能被氧化;高锰酸钾的还原产物是MnO2。回答下列问题:
(1)反应②中除掉的杂质离子所发生的离子方程式为_______ 、_______ ;在加高锰酸钾溶液前,若pH较低,对除杂的影响是_______ 。
(2)反应③的反应类型为_______ ,过滤得到的滤渣中,除了过量的锌外还有_______ 。
(3)反应④中产物的成分是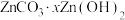 ,取干燥后的滤饼11.2g,煅烧后可得到产品8.1g,则x=
,取干燥后的滤饼11.2g,煅烧后可得到产品8.1g,则x=_______ 。

提示:在本实验条件下,Ni(II)不能被氧化;高锰酸钾的还原产物是MnO2。回答下列问题:
(1)反应②中除掉的杂质离子所发生的离子方程式为
(2)反应③的反应类型为
(3)反应④中产物的成分是
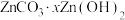 ,取干燥后的滤饼11.2g,煅烧后可得到产品8.1g,则x=
,取干燥后的滤饼11.2g,煅烧后可得到产品8.1g,则x=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室从海藻中提取碘的流程如图:
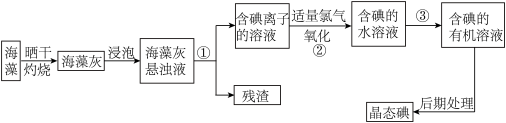
(1)指出从海藻中提取I2的实验操作名称:①___ ,③___ ;过程②中有关反应的离子方程式___ 。
(2)加氯水要适量,原因是___ 。
(3)提取碘的过程中,可供选择的有机溶剂是___ 。
A.酒精 B.四氯化碳 C.苯
(4)为使海藻中I-转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器。尚缺少的仪器是___ 。

(1)指出从海藻中提取I2的实验操作名称:①
(2)加氯水要适量,原因是
(3)提取碘的过程中,可供选择的有机溶剂是
A.酒精 B.四氯化碳 C.苯
(4)为使海藻中I-转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器。尚缺少的仪器是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】碘和铁均是人体必需的微量元素。
(1)海带中含有丰富的以碘离子形式存在的碘元素。在实验室中,从海藻中提取碘的流程如下:
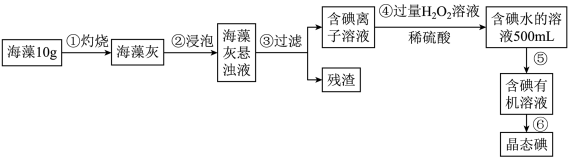
①上述流程中涉及下列操作,其中错误的是________________ (填标号)。
A.将海藻灼烧成灰
B.过滤含I-溶液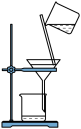
C.下口放出含碘的苯溶液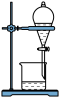
D.分离碘并回收苯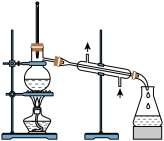
②写出步骤④发生反应的离子方程式:_______________________________________
③要证明步骤④所得溶液中含有碘单质,可加入___________________ (填试剂名称),观察到________________________ (填现象)说明溶液中存在碘。
(2)探究铁与稀硝酸的反应。用5.6gFe粉和含有0.3 mol HNO3的稀硝酸进行实验,若两种物质恰好完全反应,且HNO3只被还原成NO。回答下列问题:
①Fe粉与稀硝酸反应生成硝酸铁的化学方程式为___________________________________
②反应结束后的溶液中Fe3+、Fe2+的物质的量之比n(Fe3+):n(Fe2+)=_________________ 。
③标准状况下,生成NO气体的体积为_________________ L(保留两位小数)。
(1)海带中含有丰富的以碘离子形式存在的碘元素。在实验室中,从海藻中提取碘的流程如下:

①上述流程中涉及下列操作,其中错误的是
A.将海藻灼烧成灰

B.过滤含I-溶液

C.下口放出含碘的苯溶液

D.分离碘并回收苯

②写出步骤④发生反应的离子方程式:
③要证明步骤④所得溶液中含有碘单质,可加入
(2)探究铁与稀硝酸的反应。用5.6gFe粉和含有0.3 mol HNO3的稀硝酸进行实验,若两种物质恰好完全反应,且HNO3只被还原成NO。回答下列问题:
①Fe粉与稀硝酸反应生成硝酸铁的化学方程式为
②反应结束后的溶液中Fe3+、Fe2+的物质的量之比n(Fe3+):n(Fe2+)=
③标准状况下,生成NO气体的体积为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】Ⅰ.某化学实验室产生的废液中含有 ,
, ,
, 三种金属离子,实验室设计如下方案对废液进行处理,以回收金属并制得氧化铁,保护环境。回答下列问题:
三种金属离子,实验室设计如下方案对废液进行处理,以回收金属并制得氧化铁,保护环境。回答下列问题:
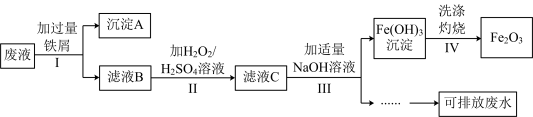
(1)沉淀A中含有的金属单质是铁、___________ (填名称)。
(2)步骤Ⅱ中加入 溶液从浅绿色变为黄色,发生反应的离子方程式为
溶液从浅绿色变为黄色,发生反应的离子方程式为___________ 。
(3)请设计实验方案检验步骤Ⅲ中 是否沉淀完全
是否沉淀完全___________ 。
(4)“可排放废水”中含有的主要离子是___________ (填离子符号)。
Ⅱ.海洋中蕴含着丰富的化学元素,是人类资源的宝库,海带中含有碘元素。从海带中提取碘的实验过程如下图所示:

(5)海带灰中含有硫酸镁、碳酸钠等,在实验步骤___________ (填名称)中实现与碘分离。
(6)步骤④中反应的离子方程式为___________ 。
(7)请设计一种检验水溶液中是否含有碘单质的方法:___________ 。
Ⅲ.镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:
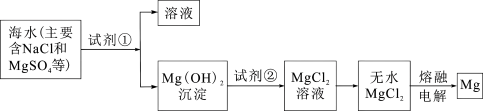
(8)为了使 转化为
转化为 ,试剂①可以选用
,试剂①可以选用___________ (填化学式)。
(9)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为_______ 。
 ,
, ,
, 三种金属离子,实验室设计如下方案对废液进行处理,以回收金属并制得氧化铁,保护环境。回答下列问题:
三种金属离子,实验室设计如下方案对废液进行处理,以回收金属并制得氧化铁,保护环境。回答下列问题:
(1)沉淀A中含有的金属单质是铁、
(2)步骤Ⅱ中加入
 溶液从浅绿色变为黄色,发生反应的离子方程式为
溶液从浅绿色变为黄色,发生反应的离子方程式为(3)请设计实验方案检验步骤Ⅲ中
 是否沉淀完全
是否沉淀完全(4)“可排放废水”中含有的主要离子是
Ⅱ.海洋中蕴含着丰富的化学元素,是人类资源的宝库,海带中含有碘元素。从海带中提取碘的实验过程如下图所示:

(5)海带灰中含有硫酸镁、碳酸钠等,在实验步骤
(6)步骤④中反应的离子方程式为
(7)请设计一种检验水溶液中是否含有碘单质的方法:
Ⅲ.镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:

(8)为了使
 转化为
转化为 ,试剂①可以选用
,试剂①可以选用(9)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为
您最近一年使用:0次



