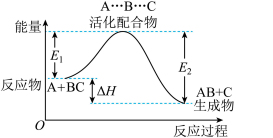
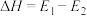对于在一定条件下进行的化学反应 2SO2(g)+O2(g)  2SO3(g),改变下列条件,能提高反应物中活化分子百分数的是:
2SO3(g),改变下列条件,能提高反应物中活化分子百分数的是:
 2SO3(g),改变下列条件,能提高反应物中活化分子百分数的是:
2SO3(g),改变下列条件,能提高反应物中活化分子百分数的是:| A.增大压强 | B.升高温度 | C.降低温度 | D.增大反应物浓度 |
16-17高一下·黑龙江牡丹江·期末 查看更多[17]
(已下线)专题03 化学反应速率及影响因素、活化能【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)云南昆明市昆明行知中学2021-2022学年高二上学期期中考试化学试题(已下线)2.3.2 影响化学反应速率因素的微观分析-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修1)江西省贵溪市实验中学2020-2021学高二上学期期中考试化学试题吉林公主岭范家屯一中2020-2021学年高二上学期期中考试化学试题(已下线)2.1.2 活化能(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)吉林省吉林市顶级名校2019-2020学年高二上学期12月月考化学考试题吉林省辽源市田家炳高级中学2019-2020学年高二上学期期中考试化学试题江西省赣州市赣县三中2019-2020学年高二上学期入学考试化学试题(已下线)2019年9月4日《每日一题》 选修4 活化能与化学反应速率的关系山东省微山县第二中学2018-2019学年高二上学期第三学段教学质量监测化学试题甘肃省岷县一中2018-2019学年高二上学期期中考试化学试题四川省泸州泸县第五中学2018-2019学年高二上学期期中考试理科综合化学试题【全国百强校】吉林省实验中学2018-2019学年高二上学期期中考试化学试题江西省上饶中学2018-2019学年高二上学期开学检测化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二上学期开学阶段性考试(8月)化学试题黑龙江省牡丹江市第一高级中学2016-2017学年高一下学期期末考试化学试题
更新时间:2019-11-06 09:11:57
|
相似题推荐
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】实验室用锌粒与4 mol·L-1硫酸溶液制取氢气,下列措施能加快化学反应速率的是
| A.向该硫酸溶液中加入等体积的水 | B.加入等体积6 mol·L-1盐酸 |
| C.加热溶液 | D.增加锌粒质量 |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐2】下列实验事实与相关的解释或结论均正确的是
选项 | 实验事实 | 解释或结论 |
A | 进行铝热反应实验时,需要加入氯酸钾,插上镁条,并点燃镁条 | 铝热反应是吸热反应 |
B | 用硫酸和氢氧化钡稀溶液可以准确测定中和热 | 硫酸和氢氧化钡分别是强酸和强碱 |
C | 锌与稀硫酸反应实验,产生氢气的速率先逐渐增大,后逐渐减小 | 该反应放热,温度升高,反应速率增大,随着反应进行,c(H+)降低,反应速率减小 |
D | 向Fe(NO3)2溶液滴加稀硫酸酸化,再滴加KSCN溶液,溶液变成红色 | Fe(NO3)2已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐1】密闭容器中反应:2CO2(g) + 6H2(g)⇌CH3CH2OH(g) + 3H2O(g) △H < 0,下列说法正确的是
| A.升高温度,平衡常数增大 |
| B.选择合适的催化剂可以提高乙醇的平衡产率 |
| C.压缩体积可增大单位体积活化分子百分数 |
| D.分离出CH3CH2OH和H2O可提高H2的转化率 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是
| A.Cu能与浓硝酸反应,而不与浓盐酸反应 |
| B.Cu与浓硝酸反应比与稀硝酸反应快 |
C. 与 与 在常温、常压下不反应,放电时可反应 在常温、常压下不反应,放电时可反应 |
D.加热时, 与浓盐酸反应,而不与稀盐酸反应 与浓盐酸反应,而不与稀盐酸反应 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】升高温度时,某化学反应速率增大,主要原因是
| A.分子运动速率加快,使反应物分子的碰撞机会增多 |
| B.反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多 |
| C.该化学反应的过程是吸热的 |
| D.该化学反应的过程是放热的 |
您最近一年使用:0次
单选题
|
容易
(0.94)
解题方法
【推荐2】研究发现,腐蚀严重的青铜器大都存在 。
。 在青铜器腐蚀过程中起催化作用。下列于
在青铜器腐蚀过程中起催化作用。下列于 叙述不正确的是
叙述不正确的是
 。
。 在青铜器腐蚀过程中起催化作用。下列于
在青铜器腐蚀过程中起催化作用。下列于 叙述不正确的是
叙述不正确的是| A.加快了反应的速率 | B.减小了反应的焓变 |
| C.改变了反应的历程 | D.降低了反应的活化能 |
您最近一年使用:0次
【推荐1】H2与ICl的反应分两步完成,其能量曲线如图所示。反应①:H2(g)+2ICl(g)=HCl(g)+HI(g)+ICl(g),反应②:HCl(g)+HI(g)+ICl(g)=I2(g)+2HCl(g),下列有关说法不正确 的是
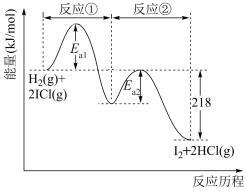

| A.总反应的活化能为(Ea1+Ea2)kJ·mol-1 |
| B.反应①、②均是反应物总能量高于生成物总能量 |
| C.H2(g)+2ICl(g)=I2(g)+2HCl(g) ∆H=-218kJ·mol-1 |
| D.温度升高,活化分子百分数增大,反应碰撞概率增大,反应速率加快 |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐2】下列说法正确的是( )
| A.活化分子的每一次碰撞都能够发生化学反应 |
| B.反应物用量增加后,有效碰撞次数增多,反应速率增大 |
| C.能够发生有效碰撞的分子叫做活化分子 |
| D.加入催化剂对化学反应速率无影响 |
您最近一年使用:0次

 2H2O+CH4。下列关于该反应的说法正确的是
2H2O+CH4。下列关于该反应的说法正确的是