下列说法中正确的是
| A.氯酸钾分解是一个熵增的过程 |
| B.△H>0,△S>0的反应一定可以自发进行 |
| C.电解水产生氢气、氧气的反应具有自发性 |
| D.可逆反应正向进行时,正反应具有自发性,△H一定小于零 |
更新时间:2019-11-03 16:57:10
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.自发反应在任何条件下都能实现,而非自发反应一定不能发生 |
| B.常温下,氢氧化钡晶体与氯化铵晶体混合放出氨气,该反应为放热反应 |
| C.等质量的硫蒸气和硫固体分别完全燃烧,前者放出热量更多 |
D.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 不同 不同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】对于化学反应能否自发进行,下列说法中错误的是( )
| A.若ΔH<0,ΔS>0,任何温度下都能自发进行 |
| B.若ΔH>0,ΔS<0,任何温度下都不能自发进行 |
| C.若ΔH>0,ΔS>0,低温时可自发进行 |
| D.若ΔH<0,ΔS<0,低温时可自发进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】化学反应伴随能量变化。下列相关描述正确的是
| A.放热过程(△H<0)或熵增加(△S>0)的过程一定是自发的 |
| B.甲烷的标准燃烧热为890.3kJ·mol-1,则甲烷燃烧热的热化学方程式表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ·mol-1 |
C.已知N2(g)+3H2(g) 2NH3(g)△H=-92.2kJ·mol-1,在密闭容器中,过量的N2与3molH2反应时放出的能量小于92.2kJ 2NH3(g)△H=-92.2kJ·mol-1,在密闭容器中,过量的N2与3molH2反应时放出的能量小于92.2kJ |
| D.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关说法正确的是
| A.电解精炼铜时,电解液CuSO4溶液的物质的量浓度不变 |
| B.NaClO溶液中通入少量CO2后,ClO-水解程度增大,溶液碱性增强 |
| C.SO3(g)+H2O(l)=H2SO4(aq)在常温下能自发进行,则该反应的△H<0 |
D.0.1 mol·L-1CH3COOH溶液加水稀释后,溶液中 的值减小 的值减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法中,正确的是
A.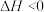 的反应均是自发进行的反应 的反应均是自发进行的反应 |
| B.反应熵变是决定反应能否自发进行的唯一因素 |
| C.使用催化剂,一定可以改变化学反应进行的方向 |
D.判断反应能否自发进行需要根据 与 与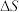 综合考虑 综合考虑 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】正确判断反应自发进行的方向对于科学研究、生产实践具有重要意义。下列说法不正确 的是
A.反应 在任何温度条件都可自发进行 在任何温度条件都可自发进行 |
B.已知反应  。积极研究此反应合适的催化剂有助于除二氧化碳 。积极研究此反应合适的催化剂有助于除二氧化碳 |
C.已知: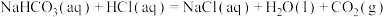 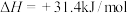 。说明在常温常压下,此反应自发进行的决定因素是熵增 。说明在常温常压下,此反应自发进行的决定因素是熵增 |
D.常温常压下可发生反应: ,说明此反应 ,说明此反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
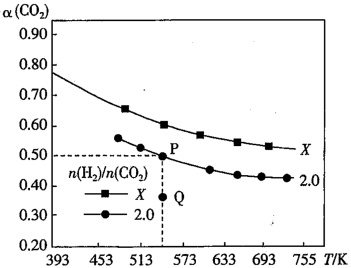
【推荐3】在两个固定体积均为1L密闭容器中以不同的氢碳比 充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)=C2H4(g)+4H2O(g)△H。CO2的平衡转化率α(CO2)与温度的关系如图所示。下列说法正确的是( )
充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)=C2H4(g)+4H2O(g)△H。CO2的平衡转化率α(CO2)与温度的关系如图所示。下列说法正确的是( )
 充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)=C2H4(g)+4H2O(g)△H。CO2的平衡转化率α(CO2)与温度的关系如图所示。下列说法正确的是( )
充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)=C2H4(g)+4H2O(g)△H。CO2的平衡转化率α(CO2)与温度的关系如图所示。下列说法正确的是( )
| A.该反应在常温下不可能自发进行 |
| B.X的氢碳比X>2.0,在氢碳比为2.0时Q点v逆(H2)>P点v逆(H2) |
| C.若起始时CO2、H2浓度分别为0.5mol/L、1.0mol/L,则可得P点对应温度的平衡常数的值为512 |
| D.向处于P点状态的容器中,按2:4:1:4的比例再充入CO2、H2、C2H4、H2O,再次平衡后α(CO2)减小 |
您最近一年使用:0次

 晶体与
晶体与 晶体的反应吸热,因此该反应在室温下是非自发反应
晶体的反应吸热,因此该反应在室温下是非自发反应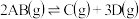 在高温时能自发进行,其逆反应在低温时能自发进行,则该反应的正反应的
在高温时能自发进行,其逆反应在低温时能自发进行,则该反应的正反应的
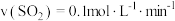 表示在
表示在 时,
时, 的浓度为
的浓度为