下列说法中,正确的是
A. 晶体与 晶体与 晶体的反应吸热,因此该反应在室温下是非自发反应 晶体的反应吸热,因此该反应在室温下是非自发反应 |
B.某反应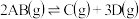 在高温时能自发进行,其逆反应在低温时能自发进行,则该反应的正反应的 在高温时能自发进行,其逆反应在低温时能自发进行,则该反应的正反应的 |
| C.活化分子之间的碰撞一定是有效碰撞 |
D.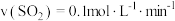 表示在 表示在 时, 时, 的浓度为 的浓度为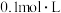 |
更新时间:2023-10-13 10:05:07
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
| A.能量达到活化能的分子发生的碰撞均为有效碰撞 |
B. 和 和 的反应活化能接近于零,反应几乎在瞬间完成 的反应活化能接近于零,反应几乎在瞬间完成 |
| C.升高温度,可以提高活化分子的能量,会减慢反应速率 |
| D.选用适当的催化剂,分子运动加快,增加了碰撞频率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知: 、
、 、
、 (
( 的作用是活化催化剂)按照一定的体积比在催化剂表面可发生反应
的作用是活化催化剂)按照一定的体积比在催化剂表面可发生反应
 ,该反应的部分反应历程如图所示(吸附在催化剂表面的物种用“*”标注,
,该反应的部分反应历程如图所示(吸附在催化剂表面的物种用“*”标注, 代表过渡态),下列说法正确的是
代表过渡态),下列说法正确的是
 、
、 、
、 (
( 的作用是活化催化剂)按照一定的体积比在催化剂表面可发生反应
的作用是活化催化剂)按照一定的体积比在催化剂表面可发生反应
 ,该反应的部分反应历程如图所示(吸附在催化剂表面的物种用“*”标注,
,该反应的部分反应历程如图所示(吸附在催化剂表面的物种用“*”标注, 代表过渡态),下列说法正确的是
代表过渡态),下列说法正确的是
| A.中间产物只有一种 |
| B.催化剂降低了该反应的焓变,使反应快速发生 |
C.决速步骤的方程式为 |
D.增大 的投入量,可使 的投入量,可使 的平衡转化率增大 的平衡转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】含硫矿物是多种化工生产的原料,主要有硫磺、黄铁矿( )、辉铜矿(
)、辉铜矿( )、明矾
)、明矾 、绿矾(
、绿矾( )、胆矾(
)、胆矾( )、重晶石(
)、重晶石( )等。硫磺、黄铁矿可作为工业制硫酸的原料,辉铜矿煅烧时可发生反应:
)等。硫磺、黄铁矿可作为工业制硫酸的原料,辉铜矿煅烧时可发生反应: 。
。 直接排放会造成环境污染,可将其转化,或用石灰乳、
直接排放会造成环境污染,可将其转化,或用石灰乳、 等物质进行回收再利用。对于反应
等物质进行回收再利用。对于反应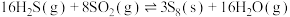
 ,下列说法正确的是
,下列说法正确的是
 )、辉铜矿(
)、辉铜矿( )、明矾
)、明矾 、绿矾(
、绿矾( )、胆矾(
)、胆矾( )、重晶石(
)、重晶石( )等。硫磺、黄铁矿可作为工业制硫酸的原料,辉铜矿煅烧时可发生反应:
)等。硫磺、黄铁矿可作为工业制硫酸的原料,辉铜矿煅烧时可发生反应: 。
。 直接排放会造成环境污染,可将其转化,或用石灰乳、
直接排放会造成环境污染,可将其转化,或用石灰乳、 等物质进行回收再利用。对于反应
等物质进行回收再利用。对于反应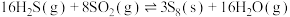
 ,下列说法正确的是
,下列说法正确的是A.该反应 |
B.反应平衡常数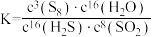 |
| C.其他条件一定,增大体系的压强可以增大反应的平衡转化率 |
| D.其他条件一定,升高温度可以增大反应的平衡常数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法中正确的是
| A.熵增加且放热的反应一定是自发反应 |
| B.自发反应一定是熵增大的反应,非自发反应一定是熵减小或不变的反应 |
| C.凡是放热反应都是能自发进行的反应,而吸热反应都是非自发进行的反应 |
| D.非自发反应在任何条件下都不能发生 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】相同的温度和压强下,有关下列两个反应的说法不正确 的是
注:①其中△n表示反应方程式中气体系数差;
②△H-T△S<0的反应方向自发
| 反应 | △H/kJ•mol-1 | △n | △S/J•K•mol-1 |
| MgCO3(s)=MgO(s)+CO2(g) | 117.6 | 1 | a |
| CaCO3(s)=CaO(s)+CO2(g) | 177.9 | 1 | b |
②△H-T△S<0的反应方向自发
| A.因为△n相同,所以a与b大小相近 |
| B.热分解温度:MgCO3(s)>CaCO3(s) |
| C.a-b=S[MgO(s)]+S[CaCO3(s)]-S[MgCO3(s)]-S[CaO(s)] |
| D.两个反应在不同温度下的△H和△S都大于零 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】反应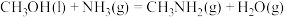 在某温度下才能自发进行,若反应的
在某温度下才能自发进行,若反应的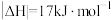 ,该温度下
,该温度下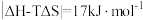 ,则下列选项正确的是
,则下列选项正确的是
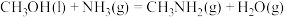 在某温度下才能自发进行,若反应的
在某温度下才能自发进行,若反应的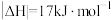 ,该温度下
,该温度下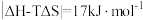 ,则下列选项正确的是
,则下列选项正确的是A. ,该温度下 ,该温度下 | B. ,该温度下 ,该温度下 |
C. ,该温度下 ,该温度下 | D. ,该温度下 ,该温度下 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于焓判据和熵判据的说法中,不正确的是
| A.放热的自发过程可能是熵减小的过程,吸热的自发过程一定为熵增加的过程 |
| B.4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s) ΔH=-444.3kJ·mol-1,ΔS=-280.1J·mol-1·K-1。此反应在常温常压下能自发进行 |
| C.碳酸钙分解为吸热反应,该反应室温下不能自发进行,但在高温下则能自发进行 |
| D.吉布斯自由能大于0的反应一定不能发生 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用活性炭与NO2反应:为2C(s)+2NO2(g)⇌2CO2(g)+N2(g)  来消除氮氧化物产生的空气污染。下列说法正确的是
来消除氮氧化物产生的空气污染。下列说法正确的是
 来消除氮氧化物产生的空气污染。下列说法正确的是
来消除氮氧化物产生的空气污染。下列说法正确的是| A.该反应只在高温条件下能自发进行 |
B.该反应平衡常数的表达式为 |
C.该反应中消耗1molNO2,转移电子的数目为 |
| D.该反应到达平衡后,升高温度,正反应速率减慢,逆反应速率加快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】氯化亚铜的化学式CuCl或Cu2Cl2,为白色立方结晶或白色粉末。微溶于水,可溶于不同浓度的KCl溶液,生成[CuCl2]-、[CuCl3]2-和[CuCl4]3-等离子。例如:CuCl(s)+2Cl-(aq) [CuCl3]2-(aq) △H。氯化亚铜溶于氨水生成氯化二氨合亚铜([Cu(NH3)2]Cl),不溶于乙醇。对于反应CuCl(s)+2Cl-(aq)
[CuCl3]2-(aq) △H。氯化亚铜溶于氨水生成氯化二氨合亚铜([Cu(NH3)2]Cl),不溶于乙醇。对于反应CuCl(s)+2Cl-(aq) [CuCl3]2-(aq),下列说法正确的是
[CuCl3]2-(aq),下列说法正确的是
 [CuCl3]2-(aq) △H。氯化亚铜溶于氨水生成氯化二氨合亚铜([Cu(NH3)2]Cl),不溶于乙醇。对于反应CuCl(s)+2Cl-(aq)
[CuCl3]2-(aq) △H。氯化亚铜溶于氨水生成氯化二氨合亚铜([Cu(NH3)2]Cl),不溶于乙醇。对于反应CuCl(s)+2Cl-(aq) [CuCl3]2-(aq),下列说法正确的是
[CuCl3]2-(aq),下列说法正确的是| A.该反应的△H>0 |
B.该反应的平衡常数可表示为K=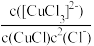 |
| C.加水可使该平衡向逆向移动 |
| D.其他条件相同,增大CuCl的量,可加快生成[CuCl3]2-的速率 |
您最近一年使用:0次


 CO2↑+H2↑
CO2↑+H2↑ :
: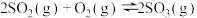
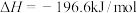 。下表列出了在不同温度和压强下,反应达到平衡时
。下表列出了在不同温度和压强下,反应达到平衡时
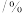

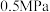


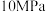
 的平衡产率
的平衡产率

