化合物A仅含两种元素(摩尔质量<200g/mol)是一种矿的主要成分,将A与O2在一定条件下反应可以生成紫红色的金属单质M。经过研究发现,由A生成M经过下列途径,且反应物和产物存在如图中的质量关系。
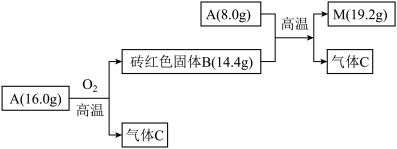
其中气体C可以使品红溶液褪色,加热后恢复红色。回答下列问题:
(1)金属M的化学式为___ ,A的化学式为___ 。
(2)写出A和B在高温下反应生成M的化学方程式为___ 。
(3)在BaCl2溶液中先通入NH3,再通入气体C,溶液出现白色沉淀,写出该反应的总离子方程式___ 。
(4)气体C可以使品红溶液褪色,解释原因:__ 。

其中气体C可以使品红溶液褪色,加热后恢复红色。回答下列问题:
(1)金属M的化学式为
(2)写出A和B在高温下反应生成M的化学方程式为
(3)在BaCl2溶液中先通入NH3,再通入气体C,溶液出现白色沉淀,写出该反应的总离子方程式
(4)气体C可以使品红溶液褪色,解释原因:
18-19高二·浙江·期中 查看更多[1]
(已下线)【新东方】高中化学165
更新时间:2019-11-10 13:26:44
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】为探究某矿物的主要成分X(仅含三种元素)的组成,某兴趣小组进行了如下实验:
①取55.2g固体X在空气存在下高温煅烧,有刺激性气味的气体产生(标况下为13.44L),该 气体能使品红溶液褪色。
②高温煅烧后的固体用磁分离技术进行分离,得到19.2g红色固体单质和23.2g 黑色固体。
③将23.2g固体溶于稀硫酸,再加氢氧化钠,将所得沉淀充分灼烧,得到24g 红棕色固体。 已知各步反应试剂均过量,请回答:
(1)X化学式为______
(2)写出X在空气存在下高温煅烧的化学反应方程式______
(3)写出X高温煅烧后的气体通入碘水中发生的离子反应方程式______
①取55.2g固体X在空气存在下高温煅烧,有刺激性气味的气体产生(标况下为13.44L),该 气体能使品红溶液褪色。
②高温煅烧后的固体用磁分离技术进行分离,得到19.2g红色固体单质和23.2g 黑色固体。
③将23.2g固体溶于稀硫酸,再加氢氧化钠,将所得沉淀充分灼烧,得到24g 红棕色固体。 已知各步反应试剂均过量,请回答:
(1)X化学式为
(2)写出X在空气存在下高温煅烧的化学反应方程式
(3)写出X高温煅烧后的气体通入碘水中发生的离子反应方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】Ⅰ.研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价—物质类别关系图如下。
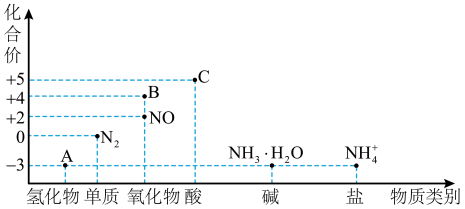
回答下列问题:
(1)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是:___________ 。
(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:___________ 。
(3)实验室中,检验溶液中含有 的操作方法是
的操作方法是___________ 。
(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:___________ ,当反应消耗3.36L(标准状况)物质B时,转移电子的物质的量为___________ mol。
Ⅱ.A、B、C、D是中学化学常见的单质,甲、乙、丙为化合物,乙在常温常压下为无色无味的液体,元素A有可变化合价。它们之间存在如下图所示的转化关系。由此推断:
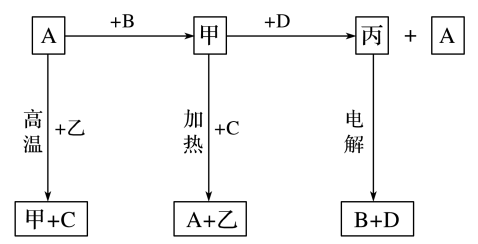
(5)甲的化学式为___________ ,丙的化学式为___________ 。
(6)写出甲和D反应的化学方程式___________ 。
(7)为检验化合物甲中元素的化合价,需要用到的药品有___________(填字母)。

回答下列问题:
(1)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是:
(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:
(3)实验室中,检验溶液中含有
 的操作方法是
的操作方法是(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:
Ⅱ.A、B、C、D是中学化学常见的单质,甲、乙、丙为化合物,乙在常温常压下为无色无味的液体,元素A有可变化合价。它们之间存在如下图所示的转化关系。由此推断:

(5)甲的化学式为
(6)写出甲和D反应的化学方程式
(7)为检验化合物甲中元素的化合价,需要用到的药品有___________(填字母)。
| A.稀硫酸 | B.盐酸 | C.硫氰化钾溶液 | D.高锰酸钾溶液 |
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】A~J分别代表中学化学中常见的一种单质或化合物,其转化关系如图。

已知C、D、G、I为短周期元素形成的单质,D、G、I常温下为气态,且G 为黄绿色;形成D的元素的原子最外层电子数是次外层的3倍;B在焰色反应中呈紫色(透过蓝色钴玻璃);K为红棕色粉末。
请回答:
(1)I在G中燃烧时的现象为________________________________ 。
(2)L是目前应用最广泛的金属,用碳棒作阳极,L作阴极,写出电解E水溶液的化学方程式_____________________________________ 。
(3)写出C与K反应的化学方程式______________________ ,引发该反应的操作为_________________________________ 。
(4)J与H反应的离子方程式为_________________________________ 。若在上述转化关系中每一步反应均为恰好反应,且不考虑C+K→A+L的变化时,为了最终得到J,则A、B的物质的量之比为_____________ 。

已知C、D、G、I为短周期元素形成的单质,D、G、I常温下为气态,且G 为黄绿色;形成D的元素的原子最外层电子数是次外层的3倍;B在焰色反应中呈紫色(透过蓝色钴玻璃);K为红棕色粉末。
请回答:
(1)I在G中燃烧时的现象为
(2)L是目前应用最广泛的金属,用碳棒作阳极,L作阴极,写出电解E水溶液的化学方程式
(3)写出C与K反应的化学方程式
(4)J与H反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】某环保部门处理含CN-电镀废水的方法如图(CN-和CNO-中N的化合价均为-3价):
某学习小组依据上述方法,用下图实验装置进行该电镀废水处理的研究。
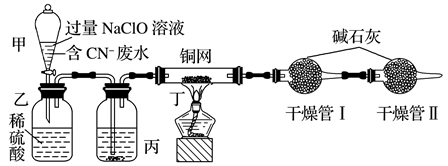
操作步骤:
ⅰ.先关闭装置甲的开关,再将含CN-废水与过量NaClO溶液混合,取200 mL混合液[其中c(CN-)=0.200mol/L]加入装置甲中,塞上橡皮塞。
ⅱ.待装置甲中充分反应后,打开开关,使溶液全部流入装置乙中,关闭开关。
ⅲ.测定干燥管Ⅰ增加的质量。
(1)写出装置乙中反应的离子方程式:________________________________________ 。
(2)装置丙中的试剂是_______________ ,装置丁的作用是_______________________ 。
(3)假定上述实验中的气体都被充分吸收。若干燥管Ⅰ增重1.408 g。则CN-被处理的百分率为__________ 。
(4)你认为用此装置进行实验,与(3)对比,CN-被处理的百分率将________ (填“偏高”、“偏低”、“无法确定”或“无影响”),简述你的理由:________________________________ 。
Ⅱ.防治空气污染,燃煤脱硫很重要。目前科学家对Fe3+溶液脱硫技术的研究已取得新成果。
(5)某学习小组为了探究“SO2与Fe3+反应的产物”,将过量的SO2通入FeCl3溶液中后,各取10 mL反应液分别加入编号为A、B、C的试管中,并设计以下3种实验方案:
方案①:A中加入少量KMnO4溶液,溶液紫红色褪去。
方案②:B中加入KSCN溶液,溶液不变红,再加入新制的氯水,溶液变红。
方案③:C中加入稀盐酸酸化的BaCl2溶液,产生白色沉淀。
上述实验方案中不合理的是________________ 。
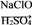
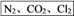
某学习小组依据上述方法,用下图实验装置进行该电镀废水处理的研究。

操作步骤:
ⅰ.先关闭装置甲的开关,再将含CN-废水与过量NaClO溶液混合,取200 mL混合液[其中c(CN-)=0.200mol/L]加入装置甲中,塞上橡皮塞。
ⅱ.待装置甲中充分反应后,打开开关,使溶液全部流入装置乙中,关闭开关。
ⅲ.测定干燥管Ⅰ增加的质量。
(1)写出装置乙中反应的离子方程式:
(2)装置丙中的试剂是
(3)假定上述实验中的气体都被充分吸收。若干燥管Ⅰ增重1.408 g。则CN-被处理的百分率为
(4)你认为用此装置进行实验,与(3)对比,CN-被处理的百分率将
Ⅱ.防治空气污染,燃煤脱硫很重要。目前科学家对Fe3+溶液脱硫技术的研究已取得新成果。
(5)某学习小组为了探究“SO2与Fe3+反应的产物”,将过量的SO2通入FeCl3溶液中后,各取10 mL反应液分别加入编号为A、B、C的试管中,并设计以下3种实验方案:
方案①:A中加入少量KMnO4溶液,溶液紫红色褪去。
方案②:B中加入KSCN溶液,溶液不变红,再加入新制的氯水,溶液变红。
方案③:C中加入稀盐酸酸化的BaCl2溶液,产生白色沉淀。
上述实验方案中不合理的是
您最近一年使用:0次
【推荐2】某兴趣小组设计如图所示装置制取 ,研究其性质,并进一步探究在适当温度和催化剂的条件下,
,研究其性质,并进一步探究在适当温度和催化剂的条件下, 与
与 反应后混合气体的成分。
反应后混合气体的成分。

(1)仪器G的名称是_______ 。
(2)装置C中反应的离子方程式为_______ ,证明 具有氧化性的实验现象是
具有氧化性的实验现象是_______ 。
(3)为了实现绿色化学的目标,某同学设计装置F来代替装置A,写出装置F发生反应的化学方程式是_______ 。
(4)该小组同学设计如下装置来检验 与
与 反应后混合气体的成分。
反应后混合气体的成分。

供选择试剂;品红溶液、蒸馏水、0.5
 溶液、酸性
溶液、酸性 溶液。
溶液。
①c中应选用的试剂是_______ ,e中试剂的作用是_______ ,f中收集的气体是_______ 。
②若b中反应已充分进行,c、d、e、f都有预期的现象,写出e中发生反应的离子方程式是_______ 。
 ,研究其性质,并进一步探究在适当温度和催化剂的条件下,
,研究其性质,并进一步探究在适当温度和催化剂的条件下, 与
与 反应后混合气体的成分。
反应后混合气体的成分。
(1)仪器G的名称是
(2)装置C中反应的离子方程式为
 具有氧化性的实验现象是
具有氧化性的实验现象是(3)为了实现绿色化学的目标,某同学设计装置F来代替装置A,写出装置F发生反应的化学方程式是
(4)该小组同学设计如下装置来检验
 与
与 反应后混合气体的成分。
反应后混合气体的成分。
供选择试剂;品红溶液、蒸馏水、0.5

 溶液、酸性
溶液、酸性 溶液。
溶液。①c中应选用的试剂是
②若b中反应已充分进行,c、d、e、f都有预期的现象,写出e中发生反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】聚合硫酸铁又称聚铁,化学式为 ,广泛用于污水处理。
,广泛用于污水处理。
某化学兴趣小组在实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)
制备聚铁和绿矾 的过程如下:
的过程如下:
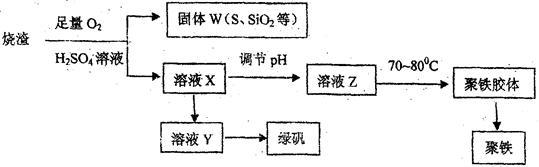
(1) 验证固体W焙烧后产生的气体含有SO2的方法是________________________ 。
(2) 实验室制备、收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各
仪器接口,顺序为a→______ →______ →_______ →_______ →f,装置D的作用是__________ ,装置E中NaOH溶液的作用是____________________ 。

(3) 制备绿矾时,内溶液X中加入过量_______________ ,充分反应后,经_________
操作得到溶液Y,再经浓缩,结晶等步骤得到绿矾。
(4)溶液Z的pH影响聚铁中铁的质量分数,用pH试纸测定溶液pH的操作方法为_________________________________________________ 。
 ,广泛用于污水处理。
,广泛用于污水处理。某化学兴趣小组在实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)
制备聚铁和绿矾
 的过程如下:
的过程如下:
(1) 验证固体W焙烧后产生的气体含有SO2的方法是
(2) 实验室制备、收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各
仪器接口,顺序为a→

(3) 制备绿矾时,内溶液X中加入过量
操作得到溶液Y,再经浓缩,结晶等步骤得到绿矾。
(4)溶液Z的pH影响聚铁中铁的质量分数,用pH试纸测定溶液pH的操作方法为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】某溶液X中只可能含有 、Fe2+、Al3+、
、Fe2+、Al3+、 、
、 、Cl-、
、Cl-、 中的若干种。某研究性小组为探究该溶液的组成,进行了如下实验:
中的若干种。某研究性小组为探究该溶液的组成,进行了如下实验:
实验Ⅰ.取2000mL溶液X,加入足量的浓NaOH溶液并加热,共收集到5.6L(已换算成标准状况)气体A,反应过程中有沉淀产生,最终无沉淀产生;往反应后的溶液中通入足量CO2,充分反应后生成19.5g沉淀B。
实验Ⅱ.另取200mL溶液X,加入足量2mol·L-1BaCl2溶液,充分反应后生成58.25g白色沉淀C;将沉淀C加入盐酸中,无明显现象。
实验Ⅲ.另取200mL溶液X,加入盐酸酸化的FeCl2溶液,无明显现象。
请回答下列问题:
(1)实验过程中需要用BaCl2固体配制250mL2mol·L-1BaCl2溶液,需要用到的玻璃仪器有烧杯、量筒、玻璃棒、___________ 、250mL容量瓶,容量瓶使用前需要___________ 。
(2)写出生成沉淀B的离子方程式___________ ,实验Ⅰ说明溶液中一定含有的离子有___________ 。
(3)实验Ⅱ中生成白色沉淀C后进行的操作为___________ 、___________ 、干燥、称量;由实验Ⅱ可知溶液X中含有___________ (填离子符号)。
(4)通过三组实验检验,溶液X中一定不含有的离子为___________ 。
 、Fe2+、Al3+、
、Fe2+、Al3+、 、
、 、Cl-、
、Cl-、 中的若干种。某研究性小组为探究该溶液的组成,进行了如下实验:
中的若干种。某研究性小组为探究该溶液的组成,进行了如下实验:实验Ⅰ.取2000mL溶液X,加入足量的浓NaOH溶液并加热,共收集到5.6L(已换算成标准状况)气体A,反应过程中有沉淀产生,最终无沉淀产生;往反应后的溶液中通入足量CO2,充分反应后生成19.5g沉淀B。
实验Ⅱ.另取200mL溶液X,加入足量2mol·L-1BaCl2溶液,充分反应后生成58.25g白色沉淀C;将沉淀C加入盐酸中,无明显现象。
实验Ⅲ.另取200mL溶液X,加入盐酸酸化的FeCl2溶液,无明显现象。
请回答下列问题:
(1)实验过程中需要用BaCl2固体配制250mL2mol·L-1BaCl2溶液,需要用到的玻璃仪器有烧杯、量筒、玻璃棒、
(2)写出生成沉淀B的离子方程式
(3)实验Ⅱ中生成白色沉淀C后进行的操作为
(4)通过三组实验检验,溶液X中一定不含有的离子为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】实验室中有一瓶无色溶液A,已知其中的溶质可能是KOH和BaCl2或两者之一,另有一固体混合物B,其中可能含有Mg(NO3)2、NH4Cl、(NH4)2SO4、CuO四种物质中的两种或多种。按如图所示进行探究实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全反应 )。

试根据上述提供的信息及实验过程发生的现象,进行分析推理,并填写以下空白:
(1)气体C的化学式是____ 。
(2)上述实验现象可以证明无色溶液A中,一定存在的金属阳离子有____ 种。
(3)根据上述实验判断,在固体混合物B中,肯定存在的物质是____ (填写化学式)。
(4)无色溶液F中大量存在的阳离子是____ (填写离子符号)。
(5)在固体混合物B里,所述四种物质中,还不能肯定是否存在的物质是____ ,请用固体混合物B样品,设计实验证明该物质是否存在,简要说明实验步骤、现象及结论:____ 。

试根据上述提供的信息及实验过程发生的现象,进行分析推理,并填写以下空白:
(1)气体C的化学式是
(2)上述实验现象可以证明无色溶液A中,一定存在的金属阳离子有
(3)根据上述实验判断,在固体混合物B中,肯定存在的物质是
(4)无色溶液F中大量存在的阳离子是
(5)在固体混合物B里,所述四种物质中,还不能肯定是否存在的物质是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】氧化亚铜(Cu2O)是一种附加值较高的铜类物质,某工厂以硫化铜矿石(含CuFeS2、Cu2S等)为原料制取Cu2O的工艺流程如下:
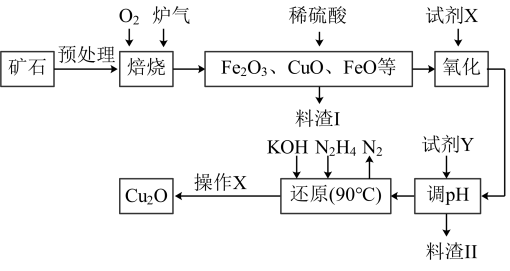
常温下几种物质开始形成沉淀与完全沉淀时的pH如下表:
(1)炉气中的有害气体成分是_______ ,Cu2S与O2反应时,氧化剂与还原剂的物质的量之比为_______ 。
(2)若试剂X是H2O2溶液,写出相应反应的离子方程式:_______ 。
(3)加入试剂Y调pH时,pH的调控范围是_______ 。
(4)写出用N2H4制备Cu2O的化学方程式:______ ,操作X包括过滤、洗涤、烘干,其中过滤后,可以通过______ 的方法检验固体物质是否已被洗涤干净。
(5)Cu2O也常用电解法制备,流程如下:
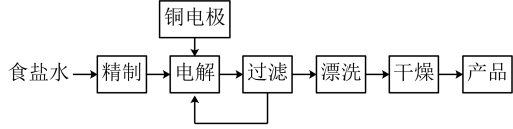
已知:①Cu2O为暗红色的固体,有毒 ②部分难溶物的颜色和常温下的Ksp如下表所示:
实验室模拟电解装置如图所示,观察到的现象如下:

①开始无明显现象,随后液面以下的铜棒表面逐渐变暗;
②5 min后,b极附近开始出现白色沉淀,并逐渐增多,且向a极扩散;
③10 min后,最靠近a极的白色沉淀开始变成红色;
④12 min后,b极附近的白色沉淀开始变成黄色,然后逐渐变成橙黄色;
⑤a极一直有大量气泡产生;
⑥停止电解,将U形管中悬浊液静置一段时间后,上层溶液呈无色,没有出现蓝色,下层沉淀全部显红色。则:
①电解池的阳极反应式为_____ 。
②b极附近的白色沉淀开始变成黄色,此时溶液中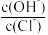 =
=_____ 。

常温下几种物质开始形成沉淀与完全沉淀时的pH如下表:
Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
开始沉淀 | 7.5 | 2.7 | 4.8 |
完全沉淀 | 9.0 | 3.7 | 6.4 |
(2)若试剂X是H2O2溶液,写出相应反应的离子方程式:
(3)加入试剂Y调pH时,pH的调控范围是
(4)写出用N2H4制备Cu2O的化学方程式:
(5)Cu2O也常用电解法制备,流程如下:

已知:①Cu2O为暗红色的固体,有毒 ②部分难溶物的颜色和常温下的Ksp如下表所示:
| 难溶物 | Cu(OH)2 | CuOH | CuCl | Cu2O |
| 颜色 | 蓝色 | 黄色 | 白色 | 红色 |
| Ksp(25 ℃) | 1.6×10-19 | 1.0×10-14 | 1.2×10-6 | — |

①开始无明显现象,随后液面以下的铜棒表面逐渐变暗;
②5 min后,b极附近开始出现白色沉淀,并逐渐增多,且向a极扩散;
③10 min后,最靠近a极的白色沉淀开始变成红色;
④12 min后,b极附近的白色沉淀开始变成黄色,然后逐渐变成橙黄色;
⑤a极一直有大量气泡产生;
⑥停止电解,将U形管中悬浊液静置一段时间后,上层溶液呈无色,没有出现蓝色,下层沉淀全部显红色。则:
①电解池的阳极反应式为
②b极附近的白色沉淀开始变成黄色,此时溶液中
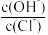 =
=
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】有一包黑色粉末,可能由C、CuO、Fe三种物质中的一种或几种组成。某化学兴趣小组为了探究它的成分,按如下步骤进行实验。
(1)先对实验做了如下设想和分析:黑粉中只有碳粉不溶解于稀盐酸。取少量粉末于烧杯中,向烧杯中加入过量的稀硫酸,则实验中可能出现的现象与对应结论如下表所示(表中未列完所有情况)。请你完成下表。
(2)通过实验及分析,确定该粉末为C、CuO的混合物。为了进一步探究C、CuO的性质,他们又利用这种混合物补充做了下面两个实验。
【实验一】将此粉末敞口在空气中灼烧完全,待冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,反应完全后,静置。烧杯中____________ (填“有”或“无”)不溶物,溶液呈___________ 色。
【实验二】将此粉末隔绝空气加热(若碳完全反应),待冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,反应完全后,静置。请回答:①烧杯中_______ (填“有”或“无”)不溶物;②若静置后溶液呈无色,则该溶液中溶质是_______ (写化学式);③若静置后溶液呈蓝色,该实验过程中所发生反应的化学方程式___________ 、__________ 。
(1)先对实验做了如下设想和分析:黑粉中只有碳粉不溶解于稀盐酸。取少量粉末于烧杯中,向烧杯中加入过量的稀硫酸,则实验中可能出现的现象与对应结论如下表所示(表中未列完所有情况)。请你完成下表。
| 烧杯中可能出现的现象 | 结论 |
| ① | 只含C |
| ②固体部分溶解,溶液变成蓝色,无气泡 | |
| ③有黑色不溶物,有气泡逸出,溶液呈浅绿色 | 含C、Fe |
【实验一】将此粉末敞口在空气中灼烧完全,待冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,反应完全后,静置。烧杯中
【实验二】将此粉末隔绝空气加热(若碳完全反应),待冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,反应完全后,静置。请回答:①烧杯中
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】某化学小组为研究甲醛和新制Cu(OH)2反应,进行如下探究,该小组设计下图装置(气密性良好并进行实验:向试管中依次加入6mol•L-1NaOH溶液12mL0.5mol•L-1CuSO4溶液8mL,振荡,再加入40%的甲醛溶液6mL,放入65°C水浴中加热,20min后冷却至室温;反应过程中观察到有红色固体生成,有少量气体产生并收集该气体。回答下列问题:

已知:Cu2O易溶于浓氨水形成[Cu ( NH3)4]+(无色),它在空气中能被氧化为[Cu(NH3)4]2+(蓝色)。
(1)实验中NaOH溶液过量的目的是__________ 。使用水浴加热的目的是_______________ 。
(2)跟乙醛与氢氧化铜的反应相似,甲醛和新制Cu (OH)2反应的产物为甲酸钠、氧化亚铜和水。该小组同学通过查阅资料发现,甲醛和新制Cu(OH)2还能发生下列反应:
HCHO+Cu(OH)2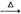 Cu+CO↑+2H2O
Cu+CO↑+2H2O
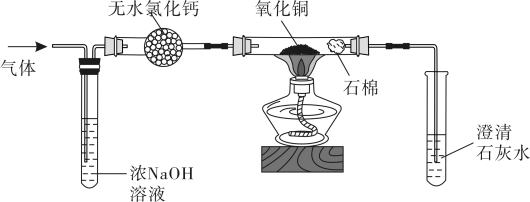
HCHO+4Cu(OH)2+2NaOH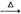 2Cu2O+Na2CO3+6H2O
2Cu2O+Na2CO3+6H2O
小组同学对实验中红色固体产物的组成作出猜想:铜或氧化亚铜或它们的混合物;为了验证固体产物,设计如下实验方案并进行实验(以下每步均充分反应):

①摇动锥形瓶 i 的目的是_________ 。
②锥形瓶 ii 中固体完全溶解得到深蓝色溶液的离子方程式为__________ 。
③将容量瓶 ii 中的溶液稀释 100 倍后,溶液的颜色与容量瓶 i 相近。由此可知固体产物的组成及物质的量之比约为__ 。
(3)为进一步确认生成的气体是CO,将收集的气体利用如图所示的装置进行实验(部分夹持仪器略去)。
①无水氯化钙的作用是______ 。
②实验中“先通气,后加热” 的目的是_____ 。
③证明气体是CO的现象________ 。
(4)甲醛与氢氧化铜反应的实验中,甲醛可能被氧化的产物为甲酸钠或碳酸钠。请设计实验方案证明溶液中甲醛的氧化产物:__ 。

已知:Cu2O易溶于浓氨水形成[Cu ( NH3)4]+(无色),它在空气中能被氧化为[Cu(NH3)4]2+(蓝色)。
(1)实验中NaOH溶液过量的目的是
(2)跟乙醛与氢氧化铜的反应相似,甲醛和新制Cu (OH)2反应的产物为甲酸钠、氧化亚铜和水。该小组同学通过查阅资料发现,甲醛和新制Cu(OH)2还能发生下列反应:
HCHO+Cu(OH)2
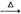 Cu+CO↑+2H2O
Cu+CO↑+2H2OHCHO+4Cu(OH)2+2NaOH
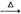 2Cu2O+Na2CO3+6H2O
2Cu2O+Na2CO3+6H2O小组同学对实验中红色固体产物的组成作出猜想:铜或氧化亚铜或它们的混合物;为了验证固体产物,设计如下实验方案并进行实验(以下每步均充分反应):

①摇动锥形瓶 i 的目的是
②锥形瓶 ii 中固体完全溶解得到深蓝色溶液的离子方程式为
③将容量瓶 ii 中的溶液稀释 100 倍后,溶液的颜色与容量瓶 i 相近。由此可知固体产物的组成及物质的量之比约为
(3)为进一步确认生成的气体是CO,将收集的气体利用如图所示的装置进行实验(部分夹持仪器略去)。

①无水氯化钙的作用是
②实验中“先通气,后加热” 的目的是
③证明气体是CO的现象
(4)甲醛与氢氧化铜反应的实验中,甲醛可能被氧化的产物为甲酸钠或碳酸钠。请设计实验方案证明溶液中甲醛的氧化产物:
您最近一年使用:0次




