为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学们分别设计了如图甲、乙所示的实验装置。请回答相关问题:
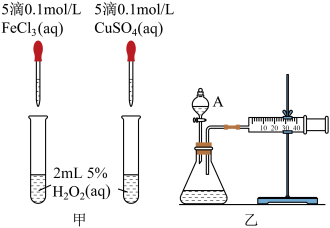
(1)定性分析:如图甲可通过观察_________ 定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_________ 。写出H2O2在二氧化锰作用下发生反应的化学方程式____ 。
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验因素均已忽略。检查该装置气密性的方法是__________________ 。图中仪器A名称为________ ,实验中需要测量的数据是_________________ 。

(1)定性分析:如图甲可通过观察
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验因素均已忽略。检查该装置气密性的方法是
更新时间:2019-11-22 10:24:09
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】传统的定量化学实验受到计量手段的制约而研究范围狭窄、精确度不高,DIS数字化信息系统(由传感器、数据采集器和计算机组成)因为可以准确测量气压、浓度、pH、温度等而在化学实验研究中应用越来越广泛深入。
Ⅰ.将打磨后的镁条放入锥形瓶中,再将注射器中某浓度的盐酸压入锥形瓶中,通过数字传感器测定实验中密闭容器(气密性良好)内压强与时间的关系如图2所示。

(1)镁条与盐酸反应的离子方程式为___________ 。该反应为___________ (填“吸热”或“放热”)反应。
(2)图2中a、b、c、d四个点中,产生氢气最快的为___________ 点。
(3)图中c点镁条已完全溶解,cd段容器内压强逐渐减小的原因可能是___________ 。
Ⅱ.向恒温恒容的密闭容器中,加入足量的碳和一定量NO,发生如下反应
 ,数字传感器测得
,数字传感器测得 浓度随时间变化如表:
浓度随时间变化如表:
(4)若该反应在t s时恰好到达平衡,t所在时间段可能为___________
A.0s<t<80s B.80s≤t<90s C.90s<t<100s D.100s≤t<110s
(5)0〜80s用NO来表示反应的速率为___________
(6)下列能说明反应达到平衡状态是___________
A. B.容器内压强不再改变 C.
B.容器内压强不再改变 C.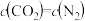 D.
D. 的体积分数不再改变
的体积分数不再改变
已知:反应体系中 的体积分数
的体积分数
Ⅰ.将打磨后的镁条放入锥形瓶中,再将注射器中某浓度的盐酸压入锥形瓶中,通过数字传感器测定实验中密闭容器(气密性良好)内压强与时间的关系如图2所示。

(1)镁条与盐酸反应的离子方程式为
(2)图2中a、b、c、d四个点中,产生氢气最快的为
(3)图中c点镁条已完全溶解,cd段容器内压强逐渐减小的原因可能是
Ⅱ.向恒温恒容的密闭容器中,加入足量的碳和一定量NO,发生如下反应

 ,数字传感器测得
,数字传感器测得 浓度随时间变化如表:
浓度随时间变化如表:| 反应时间/s | 0 | 80 | 90 | 100 | 110 |
 浓度/ 浓度/ | 0.00 | 0.30 | 0.32 | 0.33 | 0.33 |
A.0s<t<80s B.80s≤t<90s C.90s<t<100s D.100s≤t<110s
(5)0〜80s用NO来表示反应的速率为
(6)下列能说明反应达到平衡状态是
A.
 B.容器内压强不再改变 C.
B.容器内压强不再改变 C.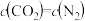 D.
D. 的体积分数不再改变
的体积分数不再改变已知:反应体系中
 的体积分数
的体积分数
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】I某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
(1)写出草酸与高锰酸钾反应的离子方程式____________________________________ 。
(2)通过实验A、B,可探究出________ (填外部因素)的改变对化学反应速率的影响,其中V1=________ 、T1=________ ;通过实验________ (填实验序号)可探究出温度变化对化学反应速率的影响,其中V2=________ 。
(3)若t1<8,则由此实验可以得出的结论是______________________________________ ;忽略溶液体积的变化,利用实验B中数据计算,0-8s内,用KMnO4的浓度变化表示的反应速率v(KMnO4)________ 。
Ⅱ催化剂在生产和科技领域起到重大作用。某化学研究小组的同学分别设计了如图所示的实验,用控制变量法比较Fe3+和Cu2+对H2O2分解的催化效果。请回答相关问题:
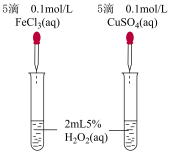
(4)定性分析:某同学通过观察甲中两支试管产生气泡的快慢,由此得出Fe3+和Cu2+对H2O2分解的催化效果,该结论_____ 填 (“合理”或“不合理”),原因________________ 。
(5)向50ml H2O2溶液中加入0.10molMnO2粉末,在标准状况下放出气体的体积和时间的关系如图所示。
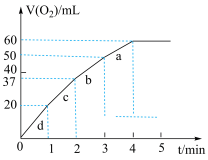
①实验中放出气体的总体积是__________ mL。
②H2O2的初始物质的量浓度是____________ (保留2位有效数字)。
③a、d两段反应速率大小的顺序为_____ >_____ ,原因_____________________________ 。
| 实验 序号 | 实验 温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
| 酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
| V/mL | c/mol﹒L-1 | V mL | c/mol﹒L-1 | V/mL | |||
| A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
| B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
| C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(2)通过实验A、B,可探究出
(3)若t1<8,则由此实验可以得出的结论是
Ⅱ催化剂在生产和科技领域起到重大作用。某化学研究小组的同学分别设计了如图所示的实验,用控制变量法比较Fe3+和Cu2+对H2O2分解的催化效果。请回答相关问题:

(4)定性分析:某同学通过观察甲中两支试管产生气泡的快慢,由此得出Fe3+和Cu2+对H2O2分解的催化效果,该结论
(5)向50ml H2O2溶液中加入0.10molMnO2粉末,在标准状况下放出气体的体积和时间的关系如图所示。

①实验中放出气体的总体积是
②H2O2的初始物质的量浓度是
③a、d两段反应速率大小的顺序为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某实验小组为确定过氧化氢分解的最佳催化条件,用如图实验装置进行实验,反应物用量和反应停止的时间数据如下:

分析表中数据回答下列问题:
(1)相同浓度的过氧化氢的分解速率随着二氧化锰用量的增加而________ 。
(2)从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入________ g的二氧化锰为较佳选择。
(3)该小组的某同学分析上述数据后认为:“当用相同质量的二氧化锰时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确________ ,理由是__________________________________ 。
(4)为加快过氧化氢的分解速率,除了使用MnO2作催化剂和改变过氧化氢的质量分数之外,还可以采取的加快反应速率的措施有_____ 。(回答任意两个合理的措施)

分析表中数据回答下列问题:
MnO2 时间 H2O2 | 0.1g | 0.3g | 0.8g |
10mL1.5% | 223s | 67s | 56s |
10mL3.0% | 308s | 109s | 98s |
10mL4.5% | 395s | 149s | 116s |
(2)从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入
(3)该小组的某同学分析上述数据后认为:“当用相同质量的二氧化锰时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确
(4)为加快过氧化氢的分解速率,除了使用MnO2作催化剂和改变过氧化氢的质量分数之外,还可以采取的加快反应速率的措施有
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】利用 制甲烷可实现碳中和,
制甲烷可实现碳中和, 催化加氢合成
催化加氢合成 反应为
反应为
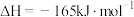
(1) 催化加氢合成
催化加氢合成 过程中,
过程中, 活化的可能途径如题图1所示,CO是
活化的可能途径如题图1所示,CO是 活化的优势中间体,原因是
活化的优势中间体,原因是_______ 。
(2) 催化
催化 与
与 转化为
转化为 的机理如题图2所示。
的机理如题图2所示。
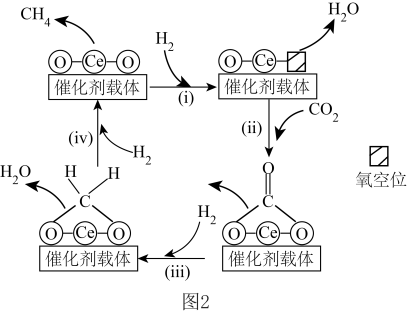
①步骤(ⅱ)中相关的碳原子轨道杂化类型的变化为_______ 。
②催化剂中掺入少量 ,用
,用 替代
替代 结构中部分
结构中部分 形成
形成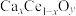 ,可提高催化效率的原因是
,可提高催化效率的原因是_______ 。
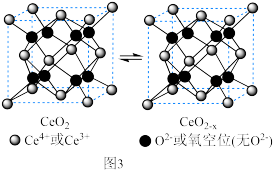
③催化剂 在催化过程中由
在催化过程中由 转变成
转变成 晶胞的组成结构变化如题图3所示,一个
晶胞的组成结构变化如题图3所示,一个 晶胞中
晶胞中 和
和 个数比为
个数比为_______ 。
(3) 催化加氢合成甲烷时,选用Ni和
催化加氢合成甲烷时,选用Ni和 作催化剂时,反应相同时间,测得
作催化剂时,反应相同时间,测得 转化率和生成
转化率和生成 选择性随温度变化的影响分别如题图4和题图5所示。
选择性随温度变化的影响分别如题图4和题图5所示。

①以Ni为催化剂,高于320℃后, 转化率上升的主要原因是
转化率上升的主要原因是_______ 。
②以 为催化剂,高于320℃后,
为催化剂,高于320℃后, 转化率略有下降的可能原因是
转化率略有下降的可能原因是_______ 。
 制甲烷可实现碳中和,
制甲烷可实现碳中和, 催化加氢合成
催化加氢合成 反应为
反应为
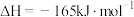
(1)
 催化加氢合成
催化加氢合成 过程中,
过程中, 活化的可能途径如题图1所示,CO是
活化的可能途径如题图1所示,CO是 活化的优势中间体,原因是
活化的优势中间体,原因是
(2)
 催化
催化 与
与 转化为
转化为 的机理如题图2所示。
的机理如题图2所示。
①步骤(ⅱ)中相关的碳原子轨道杂化类型的变化为
②催化剂中掺入少量
 ,用
,用 替代
替代 结构中部分
结构中部分 形成
形成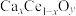 ,可提高催化效率的原因是
,可提高催化效率的原因是③催化剂
 在催化过程中由
在催化过程中由 转变成
转变成 晶胞的组成结构变化如题图3所示,一个
晶胞的组成结构变化如题图3所示,一个 晶胞中
晶胞中 和
和 个数比为
个数比为
(3)
 催化加氢合成甲烷时,选用Ni和
催化加氢合成甲烷时,选用Ni和 作催化剂时,反应相同时间,测得
作催化剂时,反应相同时间,测得 转化率和生成
转化率和生成 选择性随温度变化的影响分别如题图4和题图5所示。
选择性随温度变化的影响分别如题图4和题图5所示。
①以Ni为催化剂,高于320℃后,
 转化率上升的主要原因是
转化率上升的主要原因是②以
 为催化剂,高于320℃后,
为催化剂,高于320℃后, 转化率略有下降的可能原因是
转化率略有下降的可能原因是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】工业利用 、
、 催化合成氨实现了人类“向空气中要面包”的梦想。
催化合成氨实现了人类“向空气中要面包”的梦想。
(1)原料气(含 、
、 、CO)中的CO能被催化剂吸附,需经过铜氨液处理除去,反应为:
、CO)中的CO能被催化剂吸附,需经过铜氨液处理除去,反应为:
 。
。
①为提高CO吸收率,应选择的条件为___________ 。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
② 中的配体为
中的配体为___________
(2)研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的物种用*标注。
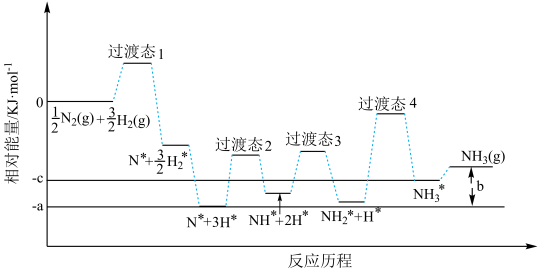
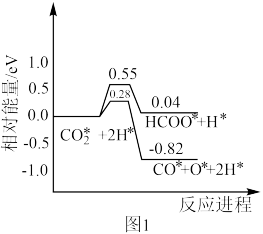
①该反应历程中最大活化能对应步骤的化学方程式为___________ 。合成氨反应: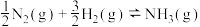 的
的
___________  (用图中字母表示)。
(用图中字母表示)。
②铁催化合成氨时 与
与 需吸附在催化剂表面活性位点进行反应,由合成氨反应的速率方程
需吸附在催化剂表面活性位点进行反应,由合成氨反应的速率方程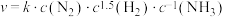 (k为速率常数)可知,
(k为速率常数)可知, 越大,反应速率越小。原因是
越大,反应速率越小。原因是___________ 。
(3)反应 的标准平衡常数可表达为:
的标准平衡常数可表达为: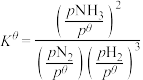 ,其中
,其中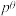 为标准压强(0.1MPa),
为标准压强(0.1MPa),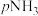 、
、 和
和 分别为各组分的平衡分压(分压=总压×物质的量分数)。若
分别为各组分的平衡分压(分压=总压×物质的量分数)。若 和
和 起始物质的量之比为1:3,反应在恒温、恒压(10MPa)下进行,平衡时
起始物质的量之比为1:3,反应在恒温、恒压(10MPa)下进行,平衡时 转化率为50%,则
转化率为50%,则
___________ (结果保留两位有效数字)。
 、
、 催化合成氨实现了人类“向空气中要面包”的梦想。
催化合成氨实现了人类“向空气中要面包”的梦想。(1)原料气(含
 、
、 、CO)中的CO能被催化剂吸附,需经过铜氨液处理除去,反应为:
、CO)中的CO能被催化剂吸附,需经过铜氨液处理除去,反应为:
 。
。①为提高CO吸收率,应选择的条件为
A.高温高压 B.高温低压 C.低温高压 D.低温低压
②
 中的配体为
中的配体为(2)研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的物种用*标注。

①该反应历程中最大活化能对应步骤的化学方程式为
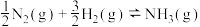 的
的
 (用图中字母表示)。
(用图中字母表示)。②铁催化合成氨时
 与
与 需吸附在催化剂表面活性位点进行反应,由合成氨反应的速率方程
需吸附在催化剂表面活性位点进行反应,由合成氨反应的速率方程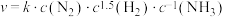 (k为速率常数)可知,
(k为速率常数)可知, 越大,反应速率越小。原因是
越大,反应速率越小。原因是(3)反应
 的标准平衡常数可表达为:
的标准平衡常数可表达为: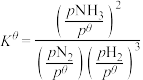 ,其中
,其中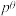 为标准压强(0.1MPa),
为标准压强(0.1MPa),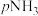 、
、 和
和 分别为各组分的平衡分压(分压=总压×物质的量分数)。若
分别为各组分的平衡分压(分压=总压×物质的量分数)。若 和
和 起始物质的量之比为1:3,反应在恒温、恒压(10MPa)下进行,平衡时
起始物质的量之比为1:3,反应在恒温、恒压(10MPa)下进行,平衡时 转化率为50%,则
转化率为50%,则
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】影响化学反应速率的因素很多,同学们用以下实验进行探究。
(1)实验一:经研究知 、
、 对
对 分解也具有催化作用,为比较
分解也具有催化作用,为比较 和
和 对
对 分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验(其他实验条件相同)。
分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验(其他实验条件相同)。

①定性分析:如图甲所示,可通过观察产生气泡的快慢来比较反应速率的大小,从而得出结论。若图甲所示的实验中反应速率为左边>右边,能否一定说明 比
比 对
对 分解的催化效果更好?
分解的催化效果更好?_____ (填“能”或“否”),其理由是_____________ (若能说明催化效果,此空不填)。
②定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。用简单的方法检验该装置的气密性:________________________ 。实验中需要测量的数据是_____________ 。
(2)实验二:酸性(稀硫酸酸化)高锰酸钾溶液和草酸( )溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显,但不久突然褪色,反应速率明显加快。
)溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显,但不久突然褪色,反应速率明显加快。
①写出酸性高锰酸钾溶液和草酸溶液反应的化学方程式:_____________________________ 。
②针对上述实验现象,某同学认为 与草酸的反应时放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是
与草酸的反应时放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是__________ 的影响。
若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是__________ 。(填序号)
A. 硫酸钾 B. 硫酸锰 C. 水 D. 氯化锰
(1)实验一:经研究知
 、
、 对
对 分解也具有催化作用,为比较
分解也具有催化作用,为比较 和
和 对
对 分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验(其他实验条件相同)。
分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验(其他实验条件相同)。
①定性分析:如图甲所示,可通过观察产生气泡的快慢来比较反应速率的大小,从而得出结论。若图甲所示的实验中反应速率为左边>右边,能否一定说明
 比
比 对
对 分解的催化效果更好?
分解的催化效果更好?②定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。用简单的方法检验该装置的气密性:
(2)实验二:酸性(稀硫酸酸化)高锰酸钾溶液和草酸(
 )溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显,但不久突然褪色,反应速率明显加快。
)溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显,但不久突然褪色,反应速率明显加快。①写出酸性高锰酸钾溶液和草酸溶液反应的化学方程式:
②针对上述实验现象,某同学认为
 与草酸的反应时放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是
与草酸的反应时放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是
A. 硫酸钾 B. 硫酸锰 C. 水 D. 氯化锰
您最近半年使用:0次



