(1)据报道,我国在南海进行的可燃冰(甲烷的水合物)试采获得成功。甲烷是一种重要的化工原料。甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下两种:
水蒸气重整:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=+205.9kJ·mol-1 ①
CO(g)+3H2(g) ΔH1=+205.9kJ·mol-1 ①
CO(g)+H2O(g) CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1 ②
CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1 ②
二氧化碳重整:CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH3 ③
2CO(g)+2H2(g) ΔH3 ③
则反应①自发进行的条件是___ (填“低温”或“高温”),ΔH3=__ kJ·mol-1。
(2)根据部分键能数据,以及热化学方程式CH4(g)+4F2(g)=CF4(g)+4HF(g) ΔH=-1940kJ·mol-1,计算H—F键的键能为__ kJ·mol-1。
(3)0.1mol的氯气和焦炭、TiO2固体完全反应,生成TiCl4液体和CO气体,放出热量4.28kJ,写出该反应的热化学方程式___ 。
水蒸气重整:CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH1=+205.9kJ·mol-1 ①
CO(g)+3H2(g) ΔH1=+205.9kJ·mol-1 ①CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1 ②
CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1 ②二氧化碳重整:CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH3 ③
2CO(g)+2H2(g) ΔH3 ③则反应①自发进行的条件是
(2)根据部分键能数据,以及热化学方程式CH4(g)+4F2(g)=CF4(g)+4HF(g) ΔH=-1940kJ·mol-1,计算H—F键的键能为
| 化学键 | C—H | C—F | H—F | F—F |
| 键能/(kJ·mol-1) | 414 | 489 | ? | 155 |
(3)0.1mol的氯气和焦炭、TiO2固体完全反应,生成TiCl4液体和CO气体,放出热量4.28kJ,写出该反应的热化学方程式
更新时间:2019-11-24 20:18:00
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)反应A(g)+B(g) C(g)+D(g)过程中的能量变化如右图所示,判断该反应△H
C(g)+D(g)过程中的能量变化如右图所示,判断该反应△H_____ 0 (填“>”、“<”、“无法确定”)。

(2)在Al2O3、Ni催化下气态甲酸发生下列反应:
甲酸(g)= CO (g)+ H2O (g) △H1=+34.0 kJ/mol
甲酸(g)= CO2(g)+ H2(g) △H2= —7.0 kJ/mol
则甲酸的分子式为___________ ,在该条件下,气态CO2和气态H2生成气态CO和气态H2O的热化学方程式为__________________________ 。
(3)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水(H2O2)。当把0.4mol液态肼和0.8mol 液态H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101 kPa下测得的热量)。反应的热化学方程式为_______________________ 。
(1)反应A(g)+B(g)
 C(g)+D(g)过程中的能量变化如右图所示,判断该反应△H
C(g)+D(g)过程中的能量变化如右图所示,判断该反应△H
(2)在Al2O3、Ni催化下气态甲酸发生下列反应:
甲酸(g)= CO (g)+ H2O (g) △H1=+34.0 kJ/mol
甲酸(g)= CO2(g)+ H2(g) △H2= —7.0 kJ/mol
则甲酸的分子式为
(3)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水(H2O2)。当把0.4mol液态肼和0.8mol 液态H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101 kPa下测得的热量)。反应的热化学方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)磷是地壳中含量较为丰富的非金属元素,主要以难溶于水的磷酸盐如Ca3(PO4)2等形式存在。它的单质和化合物在工农业生产中有着重要的应用。
白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在一定条件下反应获得。相关热化学方程式如下:
2Ca3(PO4)2(s)+10C(s)═6CaO(s)+P4(s)+10CO(g)△H1=+3359.26 kJ•mol﹣1
CaO(s)+SiO2(s)═CaSiO3(s)△H2=﹣89.61 kJ•mol﹣1
写出白磷(P4)由Ca3(PO4)2、焦炭和SiO2在一定条件下反应的热化学方程式为:_____ 。
(2)电子工业中清洗硅片上的SiO2(s)的反应为SiO2(s)+4HF(g)═SiF4(g)+2H2O(g)△H(298.15 K)=﹣94.0 kJ•mol﹣1△S(298.15 K)=﹣75.8 J•mol﹣1•K﹣1,设△H和△S不随温度而变化,此反应自发进行的温度是_____
白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在一定条件下反应获得。相关热化学方程式如下:
2Ca3(PO4)2(s)+10C(s)═6CaO(s)+P4(s)+10CO(g)△H1=+3359.26 kJ•mol﹣1
CaO(s)+SiO2(s)═CaSiO3(s)△H2=﹣89.61 kJ•mol﹣1
写出白磷(P4)由Ca3(PO4)2、焦炭和SiO2在一定条件下反应的热化学方程式为:
(2)电子工业中清洗硅片上的SiO2(s)的反应为SiO2(s)+4HF(g)═SiF4(g)+2H2O(g)△H(298.15 K)=﹣94.0 kJ•mol﹣1△S(298.15 K)=﹣75.8 J•mol﹣1•K﹣1,设△H和△S不随温度而变化,此反应自发进行的温度是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】(1)硅粉与HCl在 时反应生成
时反应生成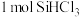 气体和
气体和 ,放出
,放出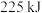 热量,该反应的热化学方程式为
热量,该反应的热化学方程式为_________ 。
(2) 与焦炭、
与焦炭、 完全反应,生成CO气体和
完全反应,生成CO气体和 液体,放热
液体,放热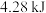 ,该反应的热化学方程式为
,该反应的热化学方程式为___________ 。
(3) 与
与 反应生成
反应生成 和一种黑色固体。在
和一种黑色固体。在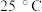 、
、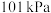 下,已知该反应每消耗
下,已知该反应每消耗 ,放热
,放热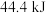 ,该反应的热化学方程式是
,该反应的热化学方程式是________ 。
(4)晶体硅(熔点 )是良好的半导体材料。由粗硅制纯硅过程如下:Si(粗)
)是良好的半导体材料。由粗硅制纯硅过程如下:Si(粗) SiCl4
SiCl4 SiCl4(纯)
SiCl4(纯) Si,在上述由
Si,在上述由 制纯硅的反应中,测得每生成
制纯硅的反应中,测得每生成 纯硅需吸收
纯硅需吸收 热量,写出该反应的热化学方程式:
热量,写出该反应的热化学方程式:__________ 。
 时反应生成
时反应生成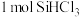 气体和
气体和 ,放出
,放出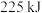 热量,该反应的热化学方程式为
热量,该反应的热化学方程式为(2)
 与焦炭、
与焦炭、 完全反应,生成CO气体和
完全反应,生成CO气体和 液体,放热
液体,放热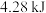 ,该反应的热化学方程式为
,该反应的热化学方程式为(3)
 与
与 反应生成
反应生成 和一种黑色固体。在
和一种黑色固体。在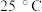 、
、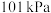 下,已知该反应每消耗
下,已知该反应每消耗 ,放热
,放热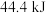 ,该反应的热化学方程式是
,该反应的热化学方程式是(4)晶体硅(熔点
 )是良好的半导体材料。由粗硅制纯硅过程如下:Si(粗)
)是良好的半导体材料。由粗硅制纯硅过程如下:Si(粗) SiCl4
SiCl4 SiCl4(纯)
SiCl4(纯) Si,在上述由
Si,在上述由 制纯硅的反应中,测得每生成
制纯硅的反应中,测得每生成 纯硅需吸收
纯硅需吸收 热量,写出该反应的热化学方程式:
热量,写出该反应的热化学方程式:
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)在25℃、101kPa下,1g甲烷燃烧生成CO2和液态水时放热55.6kJ。则表示甲烷燃烧热 的热化学方程式为__ 。
(2)下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位为kJ·mol-1):
根据键能数据计算以下反应的反应热△H:
CH4(g)+4F2(g)=CF4(g)+4HF(g) △H=__ 。
(3)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。金红石(TiO2)制钛,涉及的步骤为:TiO2—TiCl4—Ti,已知:C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol ①
O2(g)+2CO(g)=2CO2(g) ΔH=-566kJ/mol ②
TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=+141kJ/mol ③
写出金红石与氯气、石墨制取TiCl4(s)和CO的热化学反应方程式___ 。
(2)下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位为kJ·mol-1):
| 化学键 | C—H | C—F | H—F | F—F |
| 键能 | 414 | 489 | 565 | 158 |
根据键能数据计算以下反应的反应热△H:
CH4(g)+4F2(g)=CF4(g)+4HF(g) △H=
(3)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。金红石(TiO2)制钛,涉及的步骤为:TiO2—TiCl4—Ti,已知:C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol ①
O2(g)+2CO(g)=2CO2(g) ΔH=-566kJ/mol ②
TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=+141kJ/mol ③
写出金红石与氯气、石墨制取TiCl4(s)和CO的热化学反应方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】Ⅰ.氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,其中,肼(N2H4)可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。已知:①N2(g)+2O2(g)=N2O4(l) ΔH1=-19.5 kJ·mol-1,②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534.2 kJ·mol-1。
(1)写出肼和N2O4反应的热化学方程式________________________ ;
(2)已知完全断裂1 mol氮气中的键需要吸收热量946kJ,完全断裂1 mol氢气中的键需要吸收热量436kJ,根据热化学方程式: N2(g) + 3H2(g)== 2NH3(g)△H=-92.4 kJ·mol-1,则氨气中1molN—H键断裂时吸收热量是_______ kJ。
Ⅱ.(1)已知1g甲烷在氧气中燃烧生成二氧化碳气体和液态水放出55.6kJ热量,写出表示甲烷燃烧热的热化学方程式____ 。
(2)0.2mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态的三氧化二硼和液态水,放出433kJ热量,其热化学方程式为_____ ,又已知:H2O(l)=H2O(g) ΔH=+44 kJ·mol-1。则5.6 L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量是____ kJ。
(1)写出肼和N2O4反应的热化学方程式
(2)已知完全断裂1 mol氮气中的键需要吸收热量946kJ,完全断裂1 mol氢气中的键需要吸收热量436kJ,根据热化学方程式: N2(g) + 3H2(g)== 2NH3(g)△H=-92.4 kJ·mol-1,则氨气中1molN—H键断裂时吸收热量是
Ⅱ.(1)已知1g甲烷在氧气中燃烧生成二氧化碳气体和液态水放出55.6kJ热量,写出表示甲烷燃烧热的热化学方程式
(2)0.2mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态的三氧化二硼和液态水,放出433kJ热量,其热化学方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)下表中的数据是破坏1mol物质中的化学键所消耗的能量(kJ):
反应2H2(g)+O2(g)=2H2O(g)是__ (填“吸热”或“放热”)反应,这说明2molH2(g)和1mol O2(g)具有的能量比2mol H2O(g)具有的能量__ (填“高”或“低”)。
(2)氮及其化合物在工农业生产生活中有着重要应用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。
已知:N2(g)+O2(g)=2NO(g) △H1 =+180.5 kJ/mol
C(s)+O2(g)=CO2(g) △H2=﹣393.5 kJ/mol
2C(s)+O2(g)=2CO(g) △H3=﹣221 kJ/mol
若某反应的平衡常数表达式为:K= ,请写出此反应的热化学方程式:
,请写出此反应的热化学方程式:___ 。
(3)如图是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能量变化示意图,已知图中E1=134kJ·mol-1、E2=368kJ·mol-1,若在反应体系中加入催化剂,反应速率增大,E1的变化是__ (填“增大”“减小”或“不变”,下同),ΔH的变化是__ 。请写出NO2和CO反应的热化学方程式:__ 。

(4)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。
已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s)ΔH=-159.5kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)ΔH=+116.5kJ·mol-1
③H2O(l)=H2O(g)ΔH=+44.0kJ·mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式:__ 。
| 物质 | H2(g) | O2(g) | H2O(g) |
| 能量 | 436 | 496 | 926 |
(2)氮及其化合物在工农业生产生活中有着重要应用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。
已知:N2(g)+O2(g)=2NO(g) △H1 =+180.5 kJ/mol
C(s)+O2(g)=CO2(g) △H2=﹣393.5 kJ/mol
2C(s)+O2(g)=2CO(g) △H3=﹣221 kJ/mol
若某反应的平衡常数表达式为:K=
 ,请写出此反应的热化学方程式:
,请写出此反应的热化学方程式:(3)如图是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能量变化示意图,已知图中E1=134kJ·mol-1、E2=368kJ·mol-1,若在反应体系中加入催化剂,反应速率增大,E1的变化是

(4)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。
已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s)ΔH=-159.5kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)ΔH=+116.5kJ·mol-1
③H2O(l)=H2O(g)ΔH=+44.0kJ·mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式:
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】已知下列热化学方程式:①2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1
②C3H8(g)+5O2(g)=3CO2(g) +4H2O(g) △H=-2044.0kJ·mol-1
(1)氢气的燃烧热是__________
(2)已知:H2O(l)=H2O(g) △H=+44.0kJ·mol-1,写出丙烷(C3H8)燃烧生成二氧化碳和液态水的热化学方程式:__________
(3)实验测得H2和C3H8的混合气体共3mol,完全燃烧生成液态水时放热2791.6kJ,计算混合气体中H2和C3H8的体积比是_____
(4)恒温恒容条件下,硫可以发生如下反应,其反应过程和能量关系如图所示,已知2SO2(g)+O2(g)=2SO3(g) △H=-196.6kJ·mol-1
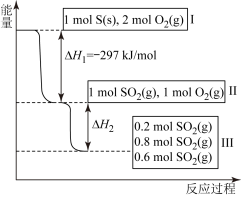
①写出能表示硫的燃烧热的热化学方程式:__________
②△H2=__________ kJ·mol-1
②C3H8(g)+5O2(g)=3CO2(g) +4H2O(g) △H=-2044.0kJ·mol-1
(1)氢气的燃烧热是
(2)已知:H2O(l)=H2O(g) △H=+44.0kJ·mol-1,写出丙烷(C3H8)燃烧生成二氧化碳和液态水的热化学方程式:
(3)实验测得H2和C3H8的混合气体共3mol,完全燃烧生成液态水时放热2791.6kJ,计算混合气体中H2和C3H8的体积比是
(4)恒温恒容条件下,硫可以发生如下反应,其反应过程和能量关系如图所示,已知2SO2(g)+O2(g)=2SO3(g) △H=-196.6kJ·mol-1

①写出能表示硫的燃烧热的热化学方程式:
②△H2=
您最近一年使用:0次

 溶液与
溶液与 锌粉在量热计中充分反应。测得反应前温度为
锌粉在量热计中充分反应。测得反应前温度为 ,反应后最高温度为
,反应后最高温度为 。
。 、溶液的密度均近似为
、溶液的密度均近似为 ,忽略溶液体积、质量变化和金属吸收的热量。请计算:
,忽略溶液体积、质量变化和金属吸收的热量。请计算: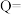
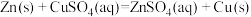 的
的
 (列式计算)。
(列式计算)。



