回答下列问题
(1)配平以下方程式
__ K2Cr2O7+__ HCl=__ KC1+__ CrCl3+__ H2O+__ Cl2↑
(2)以上反应中失电子的物质是__ ,还原产物是__ ,每生成lmol这种还原产物,将有__ mol电子发生转移。氧化剂与还原剂的物质的量之比为___ 。
(3)已知反应:2H2S+H2SO3=2H2O+3S↓,若氧化产物比还原产物多1.6g,则同时会生成水的质量为___ g。
(1)配平以下方程式
(2)以上反应中失电子的物质是
(3)已知反应:2H2S+H2SO3=2H2O+3S↓,若氧化产物比还原产物多1.6g,则同时会生成水的质量为
更新时间:2019-11-26 16:53:16
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】请按要求回答下列问题:
(1)写出硝酸铵溶于水的电离方程式:_______ ;
(2)写出金属钠与水反应的离子反应方程式:_______ ;
(3)现有七种物质:①液氯;②熔融的 ;③稀硫酸;④Cu;⑤NaOH;⑥酒精;⑦
;③稀硫酸;④Cu;⑤NaOH;⑥酒精;⑦ ,属于电解质的是
,属于电解质的是_______ ;能导电的是_______ ;
(4)我国古代四大发明之一的黑火药是由硫黄、硝酸钾和木炭粉按一定比例混合而成,爆炸时的反应为: 。
。
①该反应的氧化剂是_______ ;
②在标准状况下,若生成22.4L ,则转移的电子数目为
,则转移的电子数目为_______  。
。
(1)写出硝酸铵溶于水的电离方程式:
(2)写出金属钠与水反应的离子反应方程式:
(3)现有七种物质:①液氯;②熔融的
 ;③稀硫酸;④Cu;⑤NaOH;⑥酒精;⑦
;③稀硫酸;④Cu;⑤NaOH;⑥酒精;⑦ ,属于电解质的是
,属于电解质的是(4)我国古代四大发明之一的黑火药是由硫黄、硝酸钾和木炭粉按一定比例混合而成,爆炸时的反应为:
 。
。①该反应的氧化剂是
②在标准状况下,若生成22.4L
 ,则转移的电子数目为
,则转移的电子数目为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1) 用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ/mol
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g)ΔH=-1160 kJ/mol
若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移电子总数为________ (阿伏伽德罗常数的值用NA表示),放出的热量为________ kJ。
(2)葡萄糖是人体所需能量的重要来源之一。葡萄糖燃烧的热化学方程式为:C6H12O6(s)+6O2(g)====6CO2(g)+6H2O(l) ΔH=-2800 kJ·mol-1。已知葡萄糖在人体组织中氧化的热化学方程式与它燃烧的热化学方程式相同。计算100 g葡萄糖在人体中完全氧化时所产生的热量为______ kJ。
(3)将等物质的量的A、B混合于2 L密闭容器中发生如下反应:3A(g)+B(g)===xC(g)+2D(g),经5分钟后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率是0.1 mol/(L·min)求:
①此时A的浓度为________ ,反应开始前容器中B的物质的量为________ 。
②B的平均反应速率为________ 。
③x=________ 。
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ/mol
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g)ΔH=-1160 kJ/mol
若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移电子总数为
(2)葡萄糖是人体所需能量的重要来源之一。葡萄糖燃烧的热化学方程式为:C6H12O6(s)+6O2(g)====6CO2(g)+6H2O(l) ΔH=-2800 kJ·mol-1。已知葡萄糖在人体组织中氧化的热化学方程式与它燃烧的热化学方程式相同。计算100 g葡萄糖在人体中完全氧化时所产生的热量为
(3)将等物质的量的A、B混合于2 L密闭容器中发生如下反应:3A(g)+B(g)===xC(g)+2D(g),经5分钟后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率是0.1 mol/(L·min)求:
①此时A的浓度为
②B的平均反应速率为
③x=
您最近一年使用:0次
【推荐3】重铬酸钾 和浓盐酸在一定温度下反应可制备黄绿色的氯气,其化学方程式为
和浓盐酸在一定温度下反应可制备黄绿色的氯气,其化学方程式为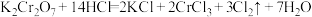 。
。
(1)浓盐酸在反应中表现出来的性质是_______ (填写编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2) 是
是_______ (“氧化”或“还原”)产物;产生 ,则转移电子的物质的量为
,则转移电子的物质的量为____ mol。
(3)从铬元素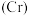 的化合价态上判断,
的化合价态上判断,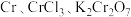 三种物质中的铬元素既表现氧化性又表现还原性的是
三种物质中的铬元素既表现氧化性又表现还原性的是_____________ (写化学式,下同)。
(4)已知氯气有毒,与水反应生成两种酸。实验室制备氯气可选用__________ 溶液进行尾气处理。
 和浓盐酸在一定温度下反应可制备黄绿色的氯气,其化学方程式为
和浓盐酸在一定温度下反应可制备黄绿色的氯气,其化学方程式为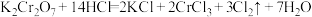 。
。(1)浓盐酸在反应中表现出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)
 是
是 ,则转移电子的物质的量为
,则转移电子的物质的量为(3)从铬元素
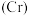 的化合价态上判断,
的化合价态上判断,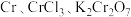 三种物质中的铬元素既表现氧化性又表现还原性的是
三种物质中的铬元素既表现氧化性又表现还原性的是(4)已知氯气有毒,与水反应生成两种酸。实验室制备氯气可选用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.神舟十七号载人航天飞船于2023年10月26日成功发射,飞船搭载的是中国研制的长征二号F遥十七运载火箭,采用四氧化二氮(N2O4)和偏二甲肼(C2H8N2)作为推进剂,二者反应生成二氧化碳、水蒸气和氮气。
(1)偏二甲肼的摩尔质量为___________ 。
(2)四氧化二氮能与水反应生成亚硝酸和___________ (写化学式)。
(3)四氧化二氮和偏二甲肼反应的化学方程式为:2N2O4+C2H8N2 2CO2+3N2+4H2O,若反应生成3mol N2,则转移的电子的物质的量是
2CO2+3N2+4H2O,若反应生成3mol N2,则转移的电子的物质的量是___________ 。
(4)已知N2、CO2混合气体的质量共10.0g,在标准状况下的体积为6.72L,则混合气体中CO2的质量为___________ 。
II.二氧化氯(ClO2)是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。已知:工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。
(5)将二氧化氯通入紫色石蕊试液中,溶液褪色的理由是___________ 。
(6)设NA为阿伏加德罗常数的值,现有10g质量分数为64%的甲醇(CH3OH)水溶液,则该溶液所含氢原子数目为___________ 。
(7)假设CO2和ClO2在标准状况下均为气体,则反应CH3OH+NaClO3+H2SO4 → CO2↑+ClO2↑+Na2SO4 +H2O(未配平)中转移的电子数目为0.6NA时,该反应产生标准状况下气体的体积为___________ 。
(1)偏二甲肼的摩尔质量为
(2)四氧化二氮能与水反应生成亚硝酸和
(3)四氧化二氮和偏二甲肼反应的化学方程式为:2N2O4+C2H8N2
 2CO2+3N2+4H2O,若反应生成3mol N2,则转移的电子的物质的量是
2CO2+3N2+4H2O,若反应生成3mol N2,则转移的电子的物质的量是(4)已知N2、CO2混合气体的质量共10.0g,在标准状况下的体积为6.72L,则混合气体中CO2的质量为
II.二氧化氯(ClO2)是一种黄绿色到橙黄色的气体,是国际上公认的安全、无毒的绿色消毒剂。已知:工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。
(5)将二氧化氯通入紫色石蕊试液中,溶液褪色的理由是
(6)设NA为阿伏加德罗常数的值,现有10g质量分数为64%的甲醇(CH3OH)水溶液,则该溶液所含氢原子数目为
(7)假设CO2和ClO2在标准状况下均为气体,则反应CH3OH+NaClO3+H2SO4 → CO2↑+ClO2↑+Na2SO4 +H2O(未配平)中转移的电子数目为0.6NA时,该反应产生标准状况下气体的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】一定条件下,Co2+与肼在碱性环境中反应制得高纯度纳米钴。请完成相应的离子方程式_______ :
N2H4+Co2++ Co+N2↑+
Co+N2↑+
检验产品的颗粒尺寸是否为纳米级的简易方案是:_____________ 。
N2H4+Co2++
 Co+N2↑+
Co+N2↑+ 检验产品的颗粒尺寸是否为纳米级的简易方案是:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氧化还原反应是一类重要的化学反应,在工农业生产、日常生活中都有广泛的用途。回答下列问题:
I.氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式: ,
, 、
、 、
、 、
、 四种物质中的一种物质(甲)能使上述还原过程发生。
四种物质中的一种物质(甲)能使上述还原过程发生。
(1)物质(甲)为___________ (填化学式)。
(2)反应中若产生5个NO分子,则转移电子的数目是___________ 个。
Ⅱ.亚硝酸钠( )像食盐一样有咸味但有很强的毒性,误食
)像食盐一样有咸味但有很强的毒性,误食 会使人中毒。已知亚硝酸钠能发生反应
会使人中毒。已知亚硝酸钠能发生反应 。
。
(3)用双线桥法标出该反应中电子转移的方向及数目:___________ ,被氧化的原子与被还原的原子数目之比为___________ 。
(4)自来水中的 对人类健康会产生危害,碱性条件下Al粉还原
对人类健康会产生危害,碱性条件下Al粉还原 ,产物是
,产物是 ,发生的反应可表示如下,完成方程式并配平。
,发生的反应可表示如下,完成方程式并配平。____________
___________ ___________
___________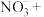 ___________
___________ ___________
___________ ___________
___________ ___________。
___________。
Ⅲ.已知乙醇( )能与
)能与 和
和 的混合溶液在一定条件下发生反应
的混合溶液在一定条件下发生反应 。
。 和
和 在溶液中分别显橙色和绿色。
在溶液中分别显橙色和绿色。
(5)该反应___________ (填“是”或“不是”)离子反应。
(6)写出 的电离方程式:
的电离方程式:___________ 。
(7)该反应___________ (填“是”或“不是”)氧化还原反应,判断的依据是___________ 。
(8)你认为能否用这一反应来检测司机是否酒后驾车?___________ (填“能”或“不能”),简述其原理:___________ 。
I.氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
 ,
, 、
、 、
、 、
、 四种物质中的一种物质(甲)能使上述还原过程发生。
四种物质中的一种物质(甲)能使上述还原过程发生。(1)物质(甲)为
(2)反应中若产生5个NO分子,则转移电子的数目是
Ⅱ.亚硝酸钠(
 )像食盐一样有咸味但有很强的毒性,误食
)像食盐一样有咸味但有很强的毒性,误食 会使人中毒。已知亚硝酸钠能发生反应
会使人中毒。已知亚硝酸钠能发生反应 。
。(3)用双线桥法标出该反应中电子转移的方向及数目:
(4)自来水中的
 对人类健康会产生危害,碱性条件下Al粉还原
对人类健康会产生危害,碱性条件下Al粉还原 ,产物是
,产物是 ,发生的反应可表示如下,完成方程式并配平。
,发生的反应可表示如下,完成方程式并配平。___________
 ___________
___________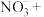 ___________
___________ ___________
___________ ___________
___________ ___________。
___________。Ⅲ.已知乙醇(
 )能与
)能与 和
和 的混合溶液在一定条件下发生反应
的混合溶液在一定条件下发生反应 。
。 和
和 在溶液中分别显橙色和绿色。
在溶液中分别显橙色和绿色。(5)该反应
(6)写出
 的电离方程式:
的电离方程式:(7)该反应
(8)你认为能否用这一反应来检测司机是否酒后驾车?
您最近一年使用:0次



