“84消毒液”因1984年北京某医院研制使用而得名,在日常生活中使用广泛,其有效成分是NaClO。某小组在实验室制备NaClO溶液,并进行性质探究。
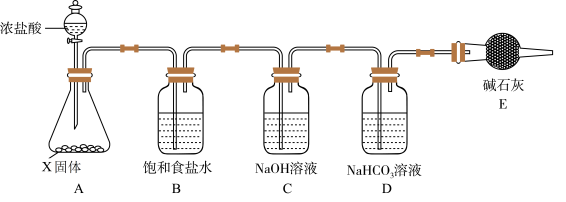
(1)X固体为_________ (填化学式),装置E的名称是_________ 。
(2)氯气与NaOH溶液、NaHCO3溶液都会发生反应,生成物均含有+1价氯的物质,其化学式分别为____________________ 、___________ 。
(3)将反应后的装置C溶液,从pH=11调到pH=5的过程中,其溶液的漂白性逐渐_____ ,理由是_____________ 。
(4)装置C需要冰水浴,否则产率大大下降,原因是__________ 。

(1)X固体为
(2)氯气与NaOH溶液、NaHCO3溶液都会发生反应,生成物均含有+1价氯的物质,其化学式分别为
(3)将反应后的装置C溶液,从pH=11调到pH=5的过程中,其溶液的漂白性逐渐
(4)装置C需要冰水浴,否则产率大大下降,原因是
更新时间:2019-11-25 09:23:31
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)如图是制取氯气并进行有关氯气性质实验的装置,装置中C、D均为洗气瓶,E中有铁粉,右端导管口处放有脱脂棉,F为尾气吸收装置。
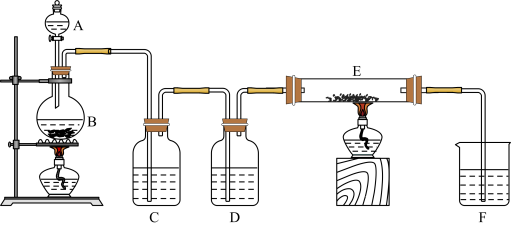
试回答:
①B中发生反应的化学方程式为_______ ;反应中氧化剂为_______ (填化学式)。
②为使E装置中进入纯净干燥的氯气,C中盛装试剂是饱和食盐水,作用是_______ ;D装置中的试剂是_______ 。
③E中发生的化学反应方程式为_______ 。
④F是尾气处理装置,反应离子方程式为_______ 。
⑤实验室也可以用KMnO4替代MnO2与浓HCl反应制取Cl2,但反应不需要加热,写出此反应的离子方程式_______ 。(已知 被还原为Mn2+)
被还原为Mn2+)
(2)Cl2是一种重要的化工原料,下图是一些含氯产品。
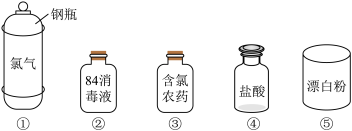
①中钢瓶上应贴的标签为_______ 。
A.腐蚀品 B.有毒品 C.易燃品
②漂白粉可用于游泳池及环境消毒剂,制漂白粉的反应原理为_______ 。
(3)2016年10月20日生活日报讯,一位温州小伙将84消毒液与洁厕灵共用来刷洗厕所时,突然瘫坐在地,无力挪步,呼吸急促。经医生诊断,小伙子为轻度氯气中毒。某大学化工系教授,该教授表示洁厕灵含有盐酸,84消毒液含有NaClO(次氯酸钠),二者不可混用,一旦混合会产生有毒的氯气,如果不慎发生事故,应立即开窗通风,用湿毛巾捂住口鼻向高处转移,事后要多喝水,并及时就医。
①请用离子方程式分析小伙子中毒的原因_______ 。
②发生事故后,要用湿毛巾捂住口鼻向高处转移,事后还要多喝水,用化学方程式表示用湿毛巾捂住口鼻,事后多喝水的原因:_______
(1)如图是制取氯气并进行有关氯气性质实验的装置,装置中C、D均为洗气瓶,E中有铁粉,右端导管口处放有脱脂棉,F为尾气吸收装置。

试回答:
①B中发生反应的化学方程式为
②为使E装置中进入纯净干燥的氯气,C中盛装试剂是饱和食盐水,作用是
③E中发生的化学反应方程式为
④F是尾气处理装置,反应离子方程式为
⑤实验室也可以用KMnO4替代MnO2与浓HCl反应制取Cl2,但反应不需要加热,写出此反应的离子方程式
 被还原为Mn2+)
被还原为Mn2+)(2)Cl2是一种重要的化工原料,下图是一些含氯产品。

①中钢瓶上应贴的标签为
A.腐蚀品 B.有毒品 C.易燃品
②漂白粉可用于游泳池及环境消毒剂,制漂白粉的反应原理为
(3)2016年10月20日生活日报讯,一位温州小伙将84消毒液与洁厕灵共用来刷洗厕所时,突然瘫坐在地,无力挪步,呼吸急促。经医生诊断,小伙子为轻度氯气中毒。某大学化工系教授,该教授表示洁厕灵含有盐酸,84消毒液含有NaClO(次氯酸钠),二者不可混用,一旦混合会产生有毒的氯气,如果不慎发生事故,应立即开窗通风,用湿毛巾捂住口鼻向高处转移,事后要多喝水,并及时就医。
①请用离子方程式分析小伙子中毒的原因
②发生事故后,要用湿毛巾捂住口鼻向高处转移,事后还要多喝水,用化学方程式表示用湿毛巾捂住口鼻,事后多喝水的原因:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】高铁酸钾(K2FeO4)是一种高效的水处理剂,实验室制备K2FeO4的装置如图所示。(夹持装置略去)
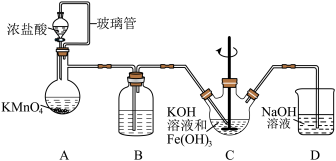
查阅K2FeO4资料如下:①紫色固体,可溶于水、微溶于KOH溶液,不溶于乙醚、醇和氯仿等有机溶剂。②在0~5℃的强碱性溶液中比较稳定。③在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2。④KOH溶于醇,微溶于乙醚。
回答下列问题:
(1)装置A为氯气发生装置,KMnO4体现的性质是___________ ,玻璃管的作用是___________ 。
(2)装置B中盛放的试剂是___________ 。
(3)装置C中KOH溶液过量的目的是___________ 。搅拌操作,除了防止因局部溶液碱性减弱,使K2FeO4与水反应产生Fe(OH)3和O2,另外的作用是___________ 。
(4)装置C中生成K2FeO4的离子方程式为___________ 。该反应放热,不利于K2FeO4固体析出,写出一条实验改进措施___________ 。
(5)反应结束后过滤装置C中浊液,得到K2FeO4粗产品,用冷的3 mo·L-1KOH溶液洗涤粗产品后,再用___________ 除水。(填标号)
a.苯 b.浓硫酸 c.异丙醇
(6)装置D的作用是___________ 。

查阅K2FeO4资料如下:①紫色固体,可溶于水、微溶于KOH溶液,不溶于乙醚、醇和氯仿等有机溶剂。②在0~5℃的强碱性溶液中比较稳定。③在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2。④KOH溶于醇,微溶于乙醚。
回答下列问题:
(1)装置A为氯气发生装置,KMnO4体现的性质是
(2)装置B中盛放的试剂是
(3)装置C中KOH溶液过量的目的是
(4)装置C中生成K2FeO4的离子方程式为
(5)反应结束后过滤装置C中浊液,得到K2FeO4粗产品,用冷的3 mo·L-1KOH溶液洗涤粗产品后,再用
a.苯 b.浓硫酸 c.异丙醇
(6)装置D的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:

(1)写出B中发生反应的化学方程式___________ 。
(2)E中为红色干布条,F中为红色湿布条,可观察到的现象是___________ ,对比E和F中现象的差异可得出的结论及解释是___________ 。
(3)试管C和D中试剂各为___________ 。
(4)装置G处发生反应的离子方程式为___________ 。
(5)用离子方程式表示试剂X的作用___________ 。
(6)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
①“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式___________ 。
②需“密闭保存”的原因___________ 。

(1)写出B中发生反应的化学方程式
(2)E中为红色干布条,F中为红色湿布条,可观察到的现象是
(3)试管C和D中试剂各为
(4)装置G处发生反应的离子方程式为
(5)用离子方程式表示试剂X的作用
(6)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
| 注意事项: 1.本品对棉织品有漂白脱色作用,对金属制品有腐蚀作用。 2.密封保存,请勿与洁厕灵同时作用。 3.保质期为一年 |
②需“密闭保存”的原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】氯气常用于自来水的杀菌消毒,实验室常用MnO2和浓盐酸共热制备氯气。
(1)写出该反应的化学方程式:_______ ,其中氧化剂和还原剂的物质的量比为_______ 。
(2)若0.1molMnO2和25mL12mol•L-1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为_______ (不考虑盐酸的挥发)
(3)若改用漂白粉与浓盐酸反应制备氯气,反应的化学方程式为Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O,装置如图所示,同时验证氯气性质(其中夹持装置已省略)。
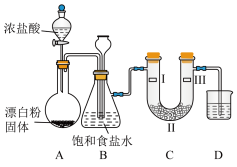
①从反应条件看,MnO2和Ca(ClO)2的氧化能力不同,氧化能力较强的是_______ 。
②装置B除了用于除去挥发的HCl,也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象:_______ 。
③装置C的作用是验证氯气是否具有漂白性,则装置C中I、II、III处依次应放入的物质是_______ (填字母)。
④装置D中为NaOH溶液,其作用是_______ ,发生的反应的化学方程式为_______ 。
(4)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中的还原产物是_______ (写化学式),反应中每生成1个ClO2分子,转移电子的数目为_______ 。
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是_______ (填序号)。
A.O2 B.FeCl2 C.KI D.KMnO4
(1)写出该反应的化学方程式:
(2)若0.1molMnO2和25mL12mol•L-1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为
| A.等于0.15mol | B.小于0.15mol |
| C.大于0.15mol,小于0.3mol | D.以上结论都不正确 |
(3)若改用漂白粉与浓盐酸反应制备氯气,反应的化学方程式为Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O,装置如图所示,同时验证氯气性质(其中夹持装置已省略)。

①从反应条件看,MnO2和Ca(ClO)2的氧化能力不同,氧化能力较强的是
②装置B除了用于除去挥发的HCl,也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象:
③装置C的作用是验证氯气是否具有漂白性,则装置C中I、II、III处依次应放入的物质是
| I | II | III | |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(4)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中的还原产物是
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐(
 ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是A.O2 B.FeCl2 C.KI D.KMnO4
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、W四种化合物均由短周期元素组成。其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。
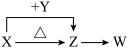
(1)W的电子式是____ 。
(2)X与Y在溶液中反应的离子方程式是____ 。
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用如图装置(夹持固定装置已略去)进行实验。

①若装置III中产生白色沉淀,装置V中可收集到一种无色气体。则装置I中反应的化学方程式是_____ 。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置V中气体(试剂另选),则该化合物的电子式是_____ ,所需仪器装置是_____ 。(从图中选择必要装置,填写编号)
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是_____ 。
(5)城市饮用水处理新技术用NaClO2、高铁酸钠代替Cl2。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么NaClO2、Na2FeO4、Cl2的消毒效率由大到小的顺序是_____ 。

(1)W的电子式是
(2)X与Y在溶液中反应的离子方程式是
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用如图装置(夹持固定装置已略去)进行实验。

①若装置III中产生白色沉淀,装置V中可收集到一种无色气体。则装置I中反应的化学方程式是
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置V中气体(试剂另选),则该化合物的电子式是
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是
(5)城市饮用水处理新技术用NaClO2、高铁酸钠代替Cl2。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么NaClO2、Na2FeO4、Cl2的消毒效率由大到小的顺序是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】工业上,四氯化锡(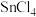 )常用作媒染剂和有机合成的氯化催化剂,在常温下其为无色液体,熔点-33℃,沸点114.1℃,在潮湿空气中极易水解,实验室将熔融的金属锡(熔点231℃)在300℃左右与绝对干燥的氯气反应生成无水四氯化锡,反应原理为:
)常用作媒染剂和有机合成的氯化催化剂,在常温下其为无色液体,熔点-33℃,沸点114.1℃,在潮湿空气中极易水解,实验室将熔融的金属锡(熔点231℃)在300℃左右与绝对干燥的氯气反应生成无水四氯化锡,反应原理为: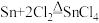 ,其实验装置如下图所示。
,其实验装置如下图所示。

(1)仪器a的名称是_______ ,其中A装置中发生反应的还原剂为_______ 。
(2)装置B和装置C中试剂相同,该试剂的作用为_______ ,进入D中的气体还含有_______ 。
(3)实验开始排完空气后应先点燃_______ 装置酒精灯或者喷灯(填装置序号);装置E中冷凝管的作用是_______ ,冷凝水应从_______ 口出水。
(4)装置F中球形干燥管内试剂为碱石灰,其作用是_______ 。
(5)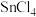 在空气中极易水解,生成白色粉末
在空气中极易水解,生成白色粉末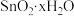 ,并释出HCl而呈现白色状。该反应的化学方程式为
,并释出HCl而呈现白色状。该反应的化学方程式为_______ 。收集少量白色粉末并称量质量,然后加热至恒重时,固体失重率为15%,则
_______ (计算结果保留小数点后一位)。
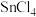 )常用作媒染剂和有机合成的氯化催化剂,在常温下其为无色液体,熔点-33℃,沸点114.1℃,在潮湿空气中极易水解,实验室将熔融的金属锡(熔点231℃)在300℃左右与绝对干燥的氯气反应生成无水四氯化锡,反应原理为:
)常用作媒染剂和有机合成的氯化催化剂,在常温下其为无色液体,熔点-33℃,沸点114.1℃,在潮湿空气中极易水解,实验室将熔融的金属锡(熔点231℃)在300℃左右与绝对干燥的氯气反应生成无水四氯化锡,反应原理为: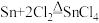 ,其实验装置如下图所示。
,其实验装置如下图所示。
(1)仪器a的名称是
(2)装置B和装置C中试剂相同,该试剂的作用为
(3)实验开始排完空气后应先点燃
(4)装置F中球形干燥管内试剂为碱石灰,其作用是
(5)
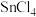 在空气中极易水解,生成白色粉末
在空气中极易水解,生成白色粉末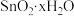 ,并释出HCl而呈现白色状。该反应的化学方程式为
,并释出HCl而呈现白色状。该反应的化学方程式为
您最近一年使用:0次



