国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:_______ 。
(2)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:_________ 。
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:_________ 。若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是________ (填字母)。
A.有铜无铁 B.有铁无铜
C.铁、铜都有 D.铁、铜都无
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:
(2)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
A.有铜无铁 B.有铁无铜
C.铁、铜都有 D.铁、铜都无
更新时间:2019-11-29 23:41:18
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)过氧化钠(Na2O2)是常见的供氧剂,是航空航天和潜水常用呼吸面具的主要成分,请写出过氧化钠的电子式:___ 。
(2)1g甲烷气体完全燃烧生成液态水时放56kJ的热量,请写出甲烷完全燃烧的热化学方程式:___ 。
(3)取久置硫酸酸化的硫酸亚铁溶液加入KSCN溶液,溶液显血红色,请用离子方程式解释原因①:___ ;②Fe3++3SCN-=Fe(SCN)3。
(4)酸性:H2SO4<HClO4,HClO4的沸点为90℃,已知能发生H2SO4(浓)+NaClO4 HClO4+NaHSO4,试从化学平衡移动的角度说明反应能发生的理由:
HClO4+NaHSO4,试从化学平衡移动的角度说明反应能发生的理由:___ 。
(2)1g甲烷气体完全燃烧生成液态水时放56kJ的热量,请写出甲烷完全燃烧的热化学方程式:
(3)取久置硫酸酸化的硫酸亚铁溶液加入KSCN溶液,溶液显血红色,请用离子方程式解释原因①:
(4)酸性:H2SO4<HClO4,HClO4的沸点为90℃,已知能发生H2SO4(浓)+NaClO4
 HClO4+NaHSO4,试从化学平衡移动的角度说明反应能发生的理由:
HClO4+NaHSO4,试从化学平衡移动的角度说明反应能发生的理由:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】写出下列反应的化学方程式或离子方程式
(1)过氧化钠可用在呼吸面具里作为氧气的来源,其反应的化学方程式为:__________________________________________________ ;
(2)氢氧化铝可用作治疗胃酸过多的药剂,其原理用离子方程式表示为:__________________________________________________ ;
(3)实验室要除去NaHCO3溶液中的少量Na2CO3,其离子方程式为:_______________________________________________________________ ;
(4) 除去FeCl2溶液中的少量FeCl3,其离子方程式为:_______________________________________________________________ 。
(1)过氧化钠可用在呼吸面具里作为氧气的来源,其反应的化学方程式为:
(2)氢氧化铝可用作治疗胃酸过多的药剂,其原理用离子方程式表示为:
(3)实验室要除去NaHCO3溶液中的少量Na2CO3,其离子方程式为:
(4) 除去FeCl2溶液中的少量FeCl3,其离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】钠、氯及其化合物有如图转化关系,请按要求填空:
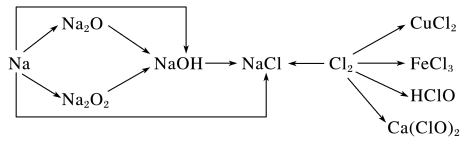
(1)金属钠的密度比水______ ,实验室中金属钠通常保存在______ 中。一小块金属钠投入水中的反应方程式是______ 。
(2)Na2O2是______ 色的固体,Na2O2的重要用途是______ ,有关反应的化学方程式为______ 。
(3)通常情况下,为了防止污染环境,在做完实验后,多余的氯气应用NaOH溶液吸收,其化学方程式为_____ 。
(4)新制的氯水滴入AgNO3溶液中,观察到______ 现象,原因是______ 。
(5)工业上用氯气和石灰乳反应制漂白粉,漂白粉的有效成分是____ ,漂白粉长时期露至在空气中会失效,用化学方程式表示其失效的原因:____ ,____ 。

(1)金属钠的密度比水
(2)Na2O2是
(3)通常情况下,为了防止污染环境,在做完实验后,多余的氯气应用NaOH溶液吸收,其化学方程式为
(4)新制的氯水滴入AgNO3溶液中,观察到
(5)工业上用氯气和石灰乳反应制漂白粉,漂白粉的有效成分是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求填空
(1)我国化学家侯德榜改进国外的纯碱生产工艺,生产流程可简要表示如图
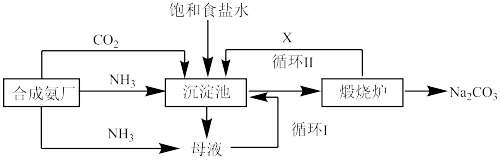
①生产时应往沉淀池中先后通入两种气体,先通入的气体为_______ 上述流程中X物质的化学式_______ 。
②请写出煅烧炉中发生反应的化学反应方程式:_______ 。上述流程中母液中最主要的成分是_______ (填化学式),检验这一组分的阴离子的具体方法是:_______ 。
(2)已知氨气具有还原性,能够和CuO发生氧化还原反应,反应后观察到黑色粉末逐渐变成红色,同时产生了使无水硫酸铜变蓝的物质,还有 一种无污染的气体单质生成,写出该反应的化学方程式:_______
(3)有两瓶无色溶液,分别是K2CO3和NaHCO3,请写出一种能鉴别这两种试剂的方法_______ 。(写出简要操作、现象和结论)
(1)我国化学家侯德榜改进国外的纯碱生产工艺,生产流程可简要表示如图

①生产时应往沉淀池中先后通入两种气体,先通入的气体为
②请写出煅烧炉中发生反应的化学反应方程式:
(2)已知氨气具有还原性,能够和CuO发生氧化还原反应,反应后观察到黑色粉末逐渐变成红色,同时产生了使无水硫酸铜变蓝的物质,还有 一种无污染的气体单质生成,写出该反应的化学方程式:
(3)有两瓶无色溶液,分别是K2CO3和NaHCO3,请写出一种能鉴别这两种试剂的方法
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】 不稳定,受热易分解,现有2.96g未完全分解的碳酸氢钠样品,欲测定其分解率,将其完全溶于水制成溶液,然后向此溶液中缓慢滴加稀盐酸,并不断搅拌。溶液中有关离子的物质的量随盐酸加入的变化如图所示,则
不稳定,受热易分解,现有2.96g未完全分解的碳酸氢钠样品,欲测定其分解率,将其完全溶于水制成溶液,然后向此溶液中缓慢滴加稀盐酸,并不断搅拌。溶液中有关离子的物质的量随盐酸加入的变化如图所示,则
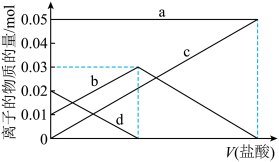
(1)a、d对应的离子分别是_______ (填离子符号);
(2)该样品中 的质量分数为
的质量分数为_______ ;(保留两位小数)
(3)原 的分解率为
的分解率为_______ 。
 不稳定,受热易分解,现有2.96g未完全分解的碳酸氢钠样品,欲测定其分解率,将其完全溶于水制成溶液,然后向此溶液中缓慢滴加稀盐酸,并不断搅拌。溶液中有关离子的物质的量随盐酸加入的变化如图所示,则
不稳定,受热易分解,现有2.96g未完全分解的碳酸氢钠样品,欲测定其分解率,将其完全溶于水制成溶液,然后向此溶液中缓慢滴加稀盐酸,并不断搅拌。溶液中有关离子的物质的量随盐酸加入的变化如图所示,则
(1)a、d对应的离子分别是
(2)该样品中
 的质量分数为
的质量分数为(3)原
 的分解率为
的分解率为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】胃酸过多是常见的胃病,下面是甲、乙两种常见胃药的说明摘要。
甲:(1)白色结晶状粉末;(2)能溶于水,水溶液呈弱碱性;(3)受热分解;④遇酸及酸性药物则产生二氧化碳;(5)胃酸过多患者服用后多见胃胀气,甚至有引起胃溃疡穿孔的危险;(6)焰色反应为黄色。
乙:(1)与胃酸的中和作用缓慢持久,可维持3~4小时;②凝胶本身覆盖于溃疡面上,具有保护作用,并能吸附H+;(3)可溶于稀酸或氢氧化钠溶液中。
(1)请你推测,甲中含有的主要化学成分是______________ (填化学式,下同);乙中含有的主要化学成分是______________ 。
(2)试写出甲中含有的主要化学成分引起胃胀气的离子方程式________________
(3)试写出乙溶于NaOH溶液的离子方程式________________ 。
甲:(1)白色结晶状粉末;(2)能溶于水,水溶液呈弱碱性;(3)受热分解;④遇酸及酸性药物则产生二氧化碳;(5)胃酸过多患者服用后多见胃胀气,甚至有引起胃溃疡穿孔的危险;(6)焰色反应为黄色。
乙:(1)与胃酸的中和作用缓慢持久,可维持3~4小时;②凝胶本身覆盖于溃疡面上,具有保护作用,并能吸附H+;(3)可溶于稀酸或氢氧化钠溶液中。
(1)请你推测,甲中含有的主要化学成分是
(2)试写出甲中含有的主要化学成分引起胃胀气的离子方程式
(3)试写出乙溶于NaOH溶液的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某小组设计实验研究单一组分浓度对化学平衡2Fe3++2I- 2Fe2++I2的影响。
2Fe2++I2的影响。
(1)①待试管中溶液的颜色不变后再进行后续实验,其目的是___________ 。
②加入KSCN溶液的目的是___________ 。
(2)甲同学认为溶液不显红色的原因是反应体系中c(Fe3+)太低,故改进实验方案,进行了实验2.
本实验改用0.1 mol•L-1KI溶液的目的是___________ 。
(3)实验3:研究增大反应物Fe3+浓度对平衡的影响,实验方法如下:
取少量试管a中棕黄色溶液于试管中,加入1~2滴饱和FeCl3溶液,溶液颜色加深,原因是:增大Fe3+浓度,导致Q___________ K(填“>”或“<”),平衡向___________ (填“正反应”或“逆反应”)方向移动。
(4)实验4:研究增大生成物Fe2+浓度对平衡的影响,实验方案如图所示:
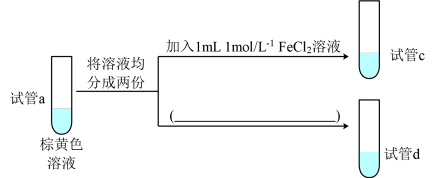
①请在图中将方案补充完整___________ 。
②能够证明增大生成物Fe2+浓度导致平衡移动的实验现象为___________ 。
 2Fe2++I2的影响。
2Fe2++I2的影响。| 实验1 | 实验步骤 | 实验现象 |
| i.取2 mL1 mol•L﹣1KI溶液,滴加0.1 mol•L-1FeCl3溶液2 mL。 | i.溶液呈棕黄色。 | |
| ii.待试管中溶液的颜色不变后向其中滴加2滴0.1 mol•L-1KSCN溶液。 | ii.溶液不显红色。 |
(1)①待试管中溶液的颜色不变后再进行后续实验,其目的是
②加入KSCN溶液的目的是
(2)甲同学认为溶液不显红色的原因是反应体系中c(Fe3+)太低,故改进实验方案,进行了实验2.
| 实验2 | 实验现象 | 实验步骤 |
| i.取2 mL0.1 mol•L﹣1KI溶液于试管a中,滴加0.1 mol•L-1FeCl3溶液2mL | i.溶液呈棕黄色 | |
| ii.待试管中溶液的颜色不变后,取少量试管a中溶液于试管b中,滴加2滴0.1 mol•L-1KSCN溶液。 | ii.溶液显红色 |
本实验改用0.1 mol•L-1KI溶液的目的是
(3)实验3:研究增大反应物Fe3+浓度对平衡的影响,实验方法如下:
取少量试管a中棕黄色溶液于试管中,加入1~2滴饱和FeCl3溶液,溶液颜色加深,原因是:增大Fe3+浓度,导致Q
(4)实验4:研究增大生成物Fe2+浓度对平衡的影响,实验方案如图所示:

①请在图中将方案补充完整
②能够证明增大生成物Fe2+浓度导致平衡移动的实验现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是______________ ,证明Fe3+存在的现象是______________ 。
(2)写出FeCl3溶液与金属铜发生反应的离子方程式_________________
(3)某工程师为了从使用过的腐蚀溶液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:
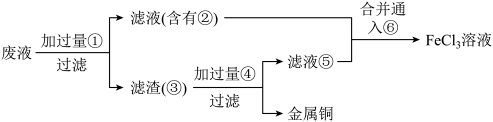
请写出上述实验中加入或生成的有关物质的化学式
①_____ ②_____ ③_____ ④_____ ⑤_____ ⑥_____ 。
(1)检验溶液中Fe3+存在的试剂是
(2)写出FeCl3溶液与金属铜发生反应的离子方程式
(3)某工程师为了从使用过的腐蚀溶液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:

请写出上述实验中加入或生成的有关物质的化学式
①
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】电子工业中,常用氯化铁溶液作为印刷电路铜板蚀刻液。请按要求回答下列问题:
(1)若向氯化铁溶液中加入一定量的澄清石灰水,调节溶液pH,可得红褐色沉淀,该反应的离子方程式为:______________________________________ ,该过程中调节溶液的pH为5,则c(Fe3+)为:____________ mol·L-1。(已知:Ksp[Fe(OH)3]= 4.0×10-38)
(2)某探究小组设计如下线路处理废液和资源回收:
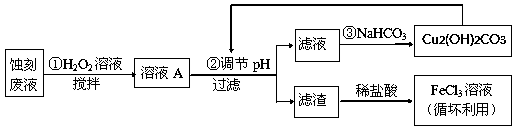
①用足量FeCl3溶液蚀刻铜板后的废液中含有的金属阳离子有:_______________ 。
②FeCl3蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是:_________________ 。
③步骤①中加入H2O2溶液的目的是:______________________________________ 。
④已知:生成氢氧化物沉淀的pH
根据表中数据推测调节pH的范围是:________________ 。
⑤写出步骤②中生成CO2的离子方程式:__________ (已知Cu2(OH)2CO3难溶于水)。
(1)若向氯化铁溶液中加入一定量的澄清石灰水,调节溶液pH,可得红褐色沉淀,该反应的离子方程式为:
(2)某探究小组设计如下线路处理废液和资源回收:

①用足量FeCl3溶液蚀刻铜板后的废液中含有的金属阳离子有:
②FeCl3蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是:
③步骤①中加入H2O2溶液的目的是:
④已知:生成氢氧化物沉淀的pH
| Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 4.7 | 7.0 | 1.9 |
| 沉淀完全时 | 6.7 | 9.0 | 3.2 |
⑤写出步骤②中生成CO2的离子方程式:
您最近一年使用:0次



