设NA代表阿伏加德罗常数,下列说法正确的是( )
| A.0.1mol/L的稀盐酸电离出的H+的物质的量为0.1mol |
| B.常温常压下,92g的NO2和N2O4混合气体含有的氧原子数为6NA |
| C.100mL,0.1mol/L的BaCl2溶液中Ba2+和Cl-离子总数为0.02NA |
| D.101k Pa、4℃时,18 mL水和202 kPa、27℃时32g O2所含分子数均为1NA |
更新时间:2019-11-25 20:02:25
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】设NA为阿伏加德罗常数,下列说法中正确的是
| A.10g 质量分数为46%的乙醇水溶液中所含氢原子数为0.6NA |
| B.将标准状况下22.4LNO与11.2LO2混合后的体积约为22.4L |
| C.在反应KClO4+8HCl=KCl+4Cl2↑+4H2O中,每生成4molCl2转移的电子数为7NA |
| D.6g石英晶体中含有的Si-O键数为0.2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述中正确的是 ( )
| A.Cu和足量的稀硝酸反应产生4.48L气体时,转移的电子数为0.6×6.02×1023 |
| B.常温常压下,8.8g CO2和N2O混合物中所含有的原子总数为0.6×6.02×1023 |
| C.标准状况下,3.36L溴乙烷中含有的溴离子数目为0.15×6.02×1023 |
| D.在1L 0.2mol/L的硫酸铁溶液中含有的三价铁离子数为0.4×6.02×1023 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】设NA是阿伏加德罗常数的值。下列说法正确的是
A. 固体中含有离子总数为3NA 固体中含有离子总数为3NA |
B.11.2L(标准状况) 含有质子数为2NA 含有质子数为2NA |
C.50g46%的乙醇水溶液中,含有 键数为3.5NA 键数为3.5NA |
| D.1molCu与足量的硫蒸气反应,转移电子数为2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】NA为阿伏加 德罗常数的数值,下列说法中正确的是
| A.在密闭容器中加入l.5mol H2和0.5molN2,充分反应后得到NH3分子数为NA |
| B.一定条件下,2. 3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA |
| C.1.0L的0.1 mol·L-1Na2S溶液中含有的S2-离子数为0.1NA |
| D.标准状况下,22.4 L的C8H18 中含有的C8H18 分子数为NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】设NA是阿伏加德罗常数的值,下列说法错误的是
A.将1molNH4NO3溶于稀氨水中,所得溶液呈中性,则溶液中NH 的数目为NA 的数目为NA |
B.5NH4NO 2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75NA 2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75NA |
| C.标准状况下,11.2LCl2溶于水,溶液中Cl2、Cl-、ClO-和HClO的微粒数之和为NA |
| D.23gNa与O2充分反应生成Na2O和Na2O2的混合物,消耗O2的分子数在0.25NA和0.5NA之间 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列数量的各物质所含原子数由大到小顺序排列的是( )
①0.5mol NH3 ②22.4L氦气(标准状况) ③4℃时9mL水 ④0.2mol CO2
①0.5mol NH3 ②22.4L氦气(标准状况) ③4℃时9mL水 ④0.2mol CO2
| A.①③②④ | B.④③②① | C.②③④① | D.①④②③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用NA代表阿伏加 德罗常数,下列说法不正确的是
| A.1mol NH3和34g H2O2所含的原子数一定相等 |
| B.标准状况下,11.2L H2O所含的分子数为5NA |
| C.18g的NH4+离子中含有的电子数为10NA |
| D.2mol钠与过量稀盐酸反应生成NA个H2分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.常温下,9 g D2O所含有的电子数为5NA |
| B.0.1 mol Na2O和Na2O2的混合物含有的阴离子数目为0.1NA |
| C.标准状况下,11.2 L氦气含有的原子数目为NA |
| D.足量MnO2和40 mL10 mol/L浓盐酸共热可生成Cl2分子数目为0.1NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:溶液呈电中性的原因是溶液中阴、阳离子所带的正、负电荷总数相等,在KCl、 、
、 形成的混合溶液中,
形成的混合溶液中,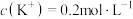 ,
,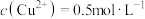 ,
,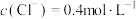 。计算分析判断,则
。计算分析判断,则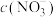 为
为
 、
、 形成的混合溶液中,
形成的混合溶液中,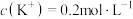 ,
,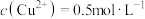 ,
,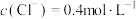 。计算分析判断,则
。计算分析判断,则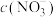 为
为A. | B. | C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法不正确的是
| A.把7.2 g纯铁粉加入40 mL浓度未知的HNO3溶液中,充分反应后剩余固体1.6 g,产生NO2和NO的混合气体0.08 mol,若不考虑N2O4的存在,则原HNO3溶液的物质的量浓度为7.0 mol·L-1 |
| B.将质量分数为a%,物质的量浓度为c1 mol·L-1的稀H2SO4溶液蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2 mol·L-1,则c1和c2的数值关系是c2>2c1 |
C.将标准状况下的a L HCl气体溶于1 000 mL水中,得到的盐酸溶液密度为b g·mL-1,则该盐酸溶液的物质的量浓度为 mol·L-1 mol·L-1 |
D.V L Fe2(SO4)3溶液中含Fe3+m g,则溶液中 的物质的量浓度为 的物质的量浓度为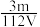 mol·L-1 mol·L-1 |
您最近一年使用:0次

 表示阿伏加德罗常数。下列说法正确的是
表示阿伏加德罗常数。下列说法正确的是 含有
含有 键的数目为
键的数目为 溶液含
溶液含 的数目为
的数目为

 与足量NaOH溶液充分反应,电子转移数为
与足量NaOH溶液充分反应,电子转移数为



