(1)0.3mol NH3中含有质子数与_________ g H2O分子中所含质子数相等。
(2)100mL Al2(SO4)3溶液中c(SO42-)=0.9 mol/L,则n[Al2(SO4)3]=_____________ 。
(3)10mL 6 mol/L稀硫酸加水稀释到200mL,稀释后c(H+)=__________ 。
(4)已知某饱和NaCl溶液的体积为VmL。密度为ρ g/cm3,质量分数为w。物质的量浓度为C mol/L,溶液中含NaCl的质量为m g.
①用m、V表示溶液物质的量浓度__________ ;
②用w、 ρ 表示溶液物质的量浓度__________ ;
③用w表示该温度下NaCl的溶解度________ 。
(2)100mL Al2(SO4)3溶液中c(SO42-)=0.9 mol/L,则n[Al2(SO4)3]=
(3)10mL 6 mol/L稀硫酸加水稀释到200mL,稀释后c(H+)=
(4)已知某饱和NaCl溶液的体积为VmL。密度为ρ g/cm3,质量分数为w。物质的量浓度为C mol/L,溶液中含NaCl的质量为m g.
①用m、V表示溶液物质的量浓度
②用w、 ρ 表示溶液物质的量浓度
③用w表示该温度下NaCl的溶解度
更新时间:2019-11-30 21:39:03
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】例3、将10.6 g Na2CO3溶于水配成1 L溶液。
(1)该溶液中Na2CO3的物质的量浓度为__________ ,溶液中Na+的物质的量浓度为__________ 。
(2)向该溶液中加入一定量NaCl固体,使溶液中Na+的物质的量浓度为0.4 mol·L-1(假设溶液体积不变)需加入NaCl的质量为__________ ,Cl-的物质的量浓度为___________________ 。
(3) 另取该浓度的Na2CO3溶液10 mL,向其中加入10 mL 0.4 mol·L-1的稀盐酸充分反应,忽略反应前后溶液体积的变化,则所得溶液中Na+的物质的量浓度为____________ 。
(1)该溶液中Na2CO3的物质的量浓度为
(2)向该溶液中加入一定量NaCl固体,使溶液中Na+的物质的量浓度为0.4 mol·L-1(假设溶液体积不变)需加入NaCl的质量为
(3) 另取该浓度的Na2CO3溶液10 mL,向其中加入10 mL 0.4 mol·L-1的稀盐酸充分反应,忽略反应前后溶液体积的变化,则所得溶液中Na+的物质的量浓度为
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐2】根据下列各题中所给出的数据,可分别求出其“溶液的溶质质量分数”或“溶液的物质的量浓度”,试判断并求解。
(1)已知某氢氧化钠溶液VL中含有N个氢氧根离子,可求出此溶液的_______ 是_______ 。
(2)已知某氢氧化钠溶液中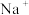 与H2O的个数之比为
与H2O的个数之比为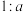 ,则可求出此溶液的
,则可求出此溶液的_______ 为_______ 。
(3)常温下,10.0mL1.0mol·L-1的H2SO4(aq),加水稀释到500mL,所得H2SO4(aq)的浓度为_______ mol·L-1;蒸发浓缩,使溶液的体积为2.40mL,所得H2SO4(aq)的浓度为_______ mol·L-1。
(4)已知标准状况下1体积水能溶解500体积的氯化氢,则可求出标准状况下氯化氢饱和溶液中溶质的质量分数为_______ 。
(1)已知某氢氧化钠溶液VL中含有N个氢氧根离子,可求出此溶液的
(2)已知某氢氧化钠溶液中
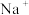 与H2O的个数之比为
与H2O的个数之比为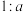 ,则可求出此溶液的
,则可求出此溶液的(3)常温下,10.0mL1.0mol·L-1的H2SO4(aq),加水稀释到500mL,所得H2SO4(aq)的浓度为
(4)已知标准状况下1体积水能溶解500体积的氯化氢,则可求出标准状况下氯化氢饱和溶液中溶质的质量分数为
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐1】请完成下列填空:
(1)已知氢气的化学式是H2,其摩尔质量为______ ;4 g H2的物质的量为____ mol,其标准状况下的体积为_____ L,其含H2分子的个数为________ ,其含氢原子的个数________ 。
(2)现有21.6 g由CO和CO2组成的混合气体,在标准状况下其体积为13.44 L。回答下列问题:该混合气体的平均摩尔质量为_____________ ,该混合气体中含CO2的量为物质的量为_____ mol。
(1)已知氢气的化学式是H2,其摩尔质量为
(2)现有21.6 g由CO和CO2组成的混合气体,在标准状况下其体积为13.44 L。回答下列问题:该混合气体的平均摩尔质量为
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐2】有关物质的量的计算:
(1)2 mol尿素[CO(NH2)2]含__ 个H原子,所含氧原子跟_____ g H2O所含氧原子个数相等。
(2)2.4g 镁中含______ mol电子,在与足量盐酸反应中产生标准状况下的氢气体积为 ______ L。
(3)30.9gNaR含有Na+ 0.3mol,则NaR的摩尔质量为_____ 。
(1)2 mol尿素[CO(NH2)2]含
(2)2.4g 镁中含
(3)30.9gNaR含有Na+ 0.3mol,则NaR的摩尔质量为
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)配制500mL0.2mol/LNa2CO3 溶液需要的Na2CO3 质量是多少?_____________ 。
(2)取上述溶液20mL稀释成100mL后其物质的量浓度是多少?_____________ 。
(2)取上述溶液20mL稀释成100mL后其物质的量浓度是多少?
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)现有以下物质:①NaCl溶液②干冰③Na2O固体④铜⑤BaSO4固体⑥蔗糖⑦液态HCl⑧熔融状态的KNO3,其中属于电解质的是_______ (填序号,下同),该状态下能导电的是_______ 。
(2)三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业技术创新必不可少的关键原料之一,可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F。则:上述反应中,氧化剂为_______ ,还原剂为_______ ,氧化剂与还原剂的物质的量之比为_______ ;若反应中有0.5molNH3被氧化,转移电子的数目为_______ 。
(3)某硫酸铝溶液的密度为1.20g·cm-3,其中铝离子的质量分数为5.4%,则300mL该溶液中SO 的物质的量为
的物质的量为_______
(4)标准状况下,将VL的氨气溶于1L的水中(密度为1g·cm-3),得到的溶液密度为ρg·cm-3,试求得到的氨水中溶质NH3的物质的量浓度为_______
(2)三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业技术创新必不可少的关键原料之一,可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F。则:上述反应中,氧化剂为
(3)某硫酸铝溶液的密度为1.20g·cm-3,其中铝离子的质量分数为5.4%,则300mL该溶液中SO
 的物质的量为
的物质的量为(4)标准状况下,将VL的氨气溶于1L的水中(密度为1g·cm-3),得到的溶液密度为ρg·cm-3,试求得到的氨水中溶质NH3的物质的量浓度为
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】如果1g水中含有m个氢原子,则阿伏伽德罗常数(NA)可表示为(用含有m的式子表示):NA=________________________ 。如果在标准状况下,W升氮气含有n个氮分子,则阿伏伽德罗常数(NA)可表示为(用含有n的式子表示):NA=________________________ 。相对分子质量为M的某物质在室温下的溶解度为S g,此时测得饱和溶液的密度为ρ g·cm-3,则该饱和溶液的物质的量浓度是________________________ 。
您最近半年使用:0次



