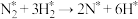碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:
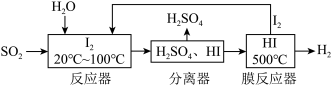
下列说法正确的是

下列说法正确的是
| A.分离器中的物质分离操作为过滤 |
| B.反应器中,控制温度为20-100℃,温度过低速率慢,过高水气化且增大碘的流失,反应速率也慢 |
| C.该工艺中I2和HI的相互转化体现了“碘循环” |
| D.碘循环工艺的总反应为2SO2+4H2O+I2=H2+2H2SO4+2HI |
更新时间:2019-12-05 08:34:25
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】CO2与CH4可制得合成气:CH4(g)+CO2(g) 2CO(g)+2H2(g);ΔH =247 kJ·mol-1。初始温度均为T K时,在3个容器中按不同方式投入反应物,发生上述反应,相关信息如下表:
2CO(g)+2H2(g);ΔH =247 kJ·mol-1。初始温度均为T K时,在3个容器中按不同方式投入反应物,发生上述反应,相关信息如下表:
下列说法正确的是( )
 2CO(g)+2H2(g);ΔH =247 kJ·mol-1。初始温度均为T K时,在3个容器中按不同方式投入反应物,发生上述反应,相关信息如下表:
2CO(g)+2H2(g);ΔH =247 kJ·mol-1。初始温度均为T K时,在3个容器中按不同方式投入反应物,发生上述反应,相关信息如下表:| 容器 | 起始物质的量/mol | CO2平衡转化率(α) | |||||
| 编号 | 容积/L | 条件 | CH4(g) | CO2(g) | CO(g) | H2(g) | |
| Ⅰ | 2 | 恒温恒容 | 2 | 1 | 0 | 0 | 50% |
| Ⅱ | 1 | 0.5 | 1 | 0 | 0 | ||
| Ⅲ | 1 | 绝热恒容 | 1 | 0.5 | 0 | 0 | - |
A.T K时,反应CH4(g)+CO2(g) 2CO(g)+2H2(g)的平衡常数为1/3 2CO(g)+2H2(g)的平衡常数为1/3 |
| B.容器Ⅱ中反应达到平衡时,α(CO2,Ⅱ)=50% |
| C.容器Ⅱ、Ⅲ中反应达到平衡时,c(CH4,Ⅱ)+c(CH4,Ⅲ)<1 mol·L-1 |
| D.容器Ⅱ中反应达到平衡时,再投入0.5 mol CH4、0.25 mol CO,反应达到新平衡前,v(正)>v(逆) |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】近日,北京航空航天大学教授团队与中科院高能物理研究所合作,合成了Y、Sc(Y1/NC,Sc1/NC)单原子催化剂,用于常温常压下的电化学催化氢气还原氮气的反应。反应历程与相对能量模拟计算结果如图所示(*表示稀土单原子催化剂)。下列说法错误的是


| A.Sc1/NC 比Y1/NC更有利于吸附氮气 |
| B.实际生产中将催化剂的尺寸处理成纳米级颗粒可提高氨气的平衡转化率 |
| C.使用Sc1/NC单原子催化剂的反应历程中,最大能垒的反应过程可表示为*N2+H→*NNH |
| D.升高温度一定可以提高氨气单位时间内的产率 |
您最近一年使用:0次
【推荐1】侯氏制碱法是连续循环生产的过程,主要流程见图,有关该流程的叙述中正确的是
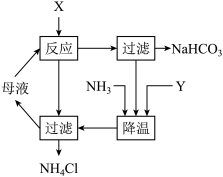

| A.母液中含有大量的Na+、NH4+、Cl-、CO32- |
| B.通入NH3只是为了增加NH4+浓度 |
| C.加入的Y物质为CO2 |
| D.生产过程中还需要补充水 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】雾霾含有大量的污染物SO2、NO。工业上变“废”为宝,吸收工业尾气SO2和NO,可获得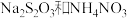 产品的流程图如下(Ce为铈元素):
产品的流程图如下(Ce为铈元素):

下列说法错误的是
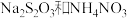 产品的流程图如下(Ce为铈元素):
产品的流程图如下(Ce为铈元素):
下列说法错误的是
A. 中S元素的化合价为+3 中S元素的化合价为+3 |
B.装置Ⅱ消耗36 g 水生成2 个H+( 个H+( 代表阿伏加德罗常数) 代表阿伏加德罗常数) |
C.装置Ⅲ用甲烷燃料电池进行电解,当消耗24 g 甲烷时,理论上可再生10 mol |
D.装置Ⅳ获得粗产品 的实验操作依次为蒸发浓缩、冷却结晶、过滤、洗涤等 的实验操作依次为蒸发浓缩、冷却结晶、过滤、洗涤等 |
您最近一年使用:0次