下列各物质中只有A、B、C三种单质,A的焰色反应为黄色,主要以G形式存在于海水中,F是一种淡黄色的固体,H是一种常见的无色液体,I是造成温室效应的“元凶”,各物质间的转化关系图如下:

回答下列问题:
(1)A是:____________ , I是:____________ (填化学式);
(2)按要求写出下列反应的方程式:
Ⅰ.①的化学方程式:______________________________ ;
Ⅱ.②的化学方程式(同时用双线桥法表示该反应的电子转移情况):________________ ;
Ⅲ. J与过量的澄清石灰水反应的离子方程式:______________________________ 。

回答下列问题:
(1)A是:
(2)按要求写出下列反应的方程式:
Ⅰ.①的化学方程式:
Ⅱ.②的化学方程式(同时用双线桥法表示该反应的电子转移情况):
Ⅲ. J与过量的澄清石灰水反应的离子方程式:
更新时间:2019-12-05 17:42:37
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)已知常温下在溶液中可发生如下两个反应:
Ce4++Fe2+=Fe3++Ce3+
Sn2++2Fe3+=2Fe2++Sn4+
由此可以确定Ce4+、Sn4+、Fe3+三种离子的氧化性由强到弱的顺序是___________ 。
(2)氢能是一种极具发展潜力的清洁能源,以太阳能为热源,热化学硫碘循环分解水是一种高效。无污染的制氢方法。其反应过程如图所示:
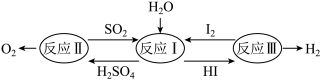
写出反应Ⅰ的化学方程式并用单线桥法标示电子转移情况:___________
(3)Mn2+、Bi3+、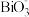 、
、 、H+、H2O组成的一个氧化还原反应体系中,发生
、H+、H2O组成的一个氧化还原反应体系中,发生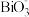 →Bi3+的反应过程。
→Bi3+的反应过程。
①该反应中,被氧化的元素是___________ ,氧化剂是______ 。
②将以上物质分别填入下面对应的横线上,组成一个未配平的离子方程式:______ ___+____+_____→_______+____+H2O。
(1)已知常温下在溶液中可发生如下两个反应:
Ce4++Fe2+=Fe3++Ce3+
Sn2++2Fe3+=2Fe2++Sn4+
由此可以确定Ce4+、Sn4+、Fe3+三种离子的氧化性由强到弱的顺序是
(2)氢能是一种极具发展潜力的清洁能源,以太阳能为热源,热化学硫碘循环分解水是一种高效。无污染的制氢方法。其反应过程如图所示:

写出反应Ⅰ的化学方程式并用单线桥法标示电子转移情况:
(3)Mn2+、Bi3+、
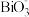 、
、 、H+、H2O组成的一个氧化还原反应体系中,发生
、H+、H2O组成的一个氧化还原反应体系中,发生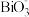 →Bi3+的反应过程。
→Bi3+的反应过程。①该反应中,被氧化的元素是
②将以上物质分别填入下面对应的横线上,组成一个未配平的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上生产漂白剂亚氯酸钠 的同时可获得高氯酸
的同时可获得高氯酸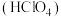 ,其流程如下:
,其流程如下:

已知: 浓度过高时易发生分解爆炸,一般用稀有气体或空气稀释至含量10%以下。
浓度过高时易发生分解爆炸,一般用稀有气体或空气稀释至含量10%以下。
(1)反应器I中发生的反应为: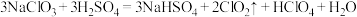 。用“双线桥”标出电子转移的方向和数目
。用“双线桥”标出电子转移的方向和数目___________ ;若生成标况下3.36L的 气体,则转移电子的物质的量为
气体,则转移电子的物质的量为___________ 。
(2)反应器I中反应后溶液冷却的目的是___________ ,可用蒸馏法分离出高氯酸的理由为___________ 。
(3)生产过程中需向反应器I中鼓入一定量空气,鼓入空气的作用是___________ 。
(4)利用反应器Ⅱ吸收 ,发生反应的化学方程式为
,发生反应的化学方程式为___________ ;该反应为放热反应,温度较低时吸收效果好。在不改变吸收液浓度和体积的条件下,欲使反应在0~5℃下进行,实验中可采取的措施有___________ (答出两点)。
 的同时可获得高氯酸
的同时可获得高氯酸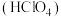 ,其流程如下:
,其流程如下:
已知:
 浓度过高时易发生分解爆炸,一般用稀有气体或空气稀释至含量10%以下。
浓度过高时易发生分解爆炸,一般用稀有气体或空气稀释至含量10%以下。(1)反应器I中发生的反应为:
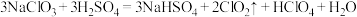 。用“双线桥”标出电子转移的方向和数目
。用“双线桥”标出电子转移的方向和数目 气体,则转移电子的物质的量为
气体,则转移电子的物质的量为(2)反应器I中反应后溶液冷却的目的是
(3)生产过程中需向反应器I中鼓入一定量空气,鼓入空气的作用是
(4)利用反应器Ⅱ吸收
 ,发生反应的化学方程式为
,发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】氧化还原反应是一类非常重要的反应。回答下列问题:
(1)按如图所示操作,充分反应后:

①Ⅰ中发生反应的离子方程式为__________________________________ ;
②Ⅱ中铜丝上观察到的现象是___________________________________ ;
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为_____________ 。
(2)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S===K2S+N2↑+3CO2↑。其中氧化产物是________
(3)人体内的铁元素是以Fe2+和Fe3+的形式存在。Fe2+易被人体吸收,服用维生素C,可使Fe3+转化成Fe2+,有利于人体吸收,说明维生素C具有_______ (填“氧化性”或“还原性”)。
(4)市场上出售的某种麦片中含有微量还原性铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐。此反应的化学方程式为________________________________________________
(5)写出氢气还原氧化铜反应的化学方程式,并用双线桥法表示电子转移的方向和数目。________________________________________________
(1)按如图所示操作,充分反应后:

①Ⅰ中发生反应的离子方程式为
②Ⅱ中铜丝上观察到的现象是
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为
(2)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S===K2S+N2↑+3CO2↑。其中氧化产物是
(3)人体内的铁元素是以Fe2+和Fe3+的形式存在。Fe2+易被人体吸收,服用维生素C,可使Fe3+转化成Fe2+,有利于人体吸收,说明维生素C具有
(4)市场上出售的某种麦片中含有微量还原性铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐。此反应的化学方程式为
(5)写出氢气还原氧化铜反应的化学方程式,并用双线桥法表示电子转移的方向和数目。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】如图1是钠及其化合物与水反应关系图,两圆圈相交的部分表示圆圈内的物质相互发生的反应。请按要求填空。

(1)反应①的化学方程式_________________________________ 。
(2)在反应②中的混合液滴入酚酞,可观察到的现象是__________ 。
(3)研究性学习小组设计图2装置探究反应③是放热反应。

i.向烧杯内滴加水时,可观察到的现象是__________________ 。
ⅱ.该反应的化学方程式为________________________________ 。
ⅲ.举例过氧化钠的用途___________ 。(写一种)
(4)超氧化钾(KO2)与过氧化钠一样能吸收CO2生成碳酸盐及O2,写出该反应的化学方程式_________________ 。
(5)若0.1 mol钠与100g的水反应,产生H2在标况下的体积为________ L。

(1)反应①的化学方程式
(2)在反应②中的混合液滴入酚酞,可观察到的现象是
(3)研究性学习小组设计图2装置探究反应③是放热反应。

i.向烧杯内滴加水时,可观察到的现象是
ⅱ.该反应的化学方程式为
ⅲ.举例过氧化钠的用途
(4)超氧化钾(KO2)与过氧化钠一样能吸收CO2生成碳酸盐及O2,写出该反应的化学方程式
(5)若0.1 mol钠与100g的水反应,产生H2在标况下的体积为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】中学化学常见物质的相互转化如图所示:

(1)写出化学式A:___________ ,Y:___________
(2)写出反应②的离子方程式:___________ ,写出反应④的离子方程式:___________ ,写出反应⑤的化学方程式,并用双线桥表示电子转移情况:___________
(3)气体J溶于水后得到的溶液中存在的分子有:H2O、___________ 、___________

(1)写出化学式A:
(2)写出反应②的离子方程式:
(3)气体J溶于水后得到的溶液中存在的分子有:H2O、
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某研究性学习小组设计了一组实验,验证元素周期律。
(1)甲同学在a、b、c、d四只烧杯里分别加入50 mL冷水,再分别滴加几滴酚酞溶液,依次加入大小相近的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象。
①甲同学设计实验的目的是验证:同一主族,从上到下元素的元素金属性逐渐增强;同一周期,从左到右,元素金属性_____________________ ;
②反应最剧烈的烧杯里金属是_______ (填字母)
A、钠 B、镁 C、铝 D、钾;
③写出a烧杯里发生反应的离子方程式______________________________ 。
④实验中发现b、c两只烧杯中几乎没有什么现象,要想达到实验的目的,请你帮助选择下列合适的方法________ 。
A.把镁、铝的金属块换成金属粉末
B.把烧杯中的冷水换成热水
C.把烧杯中的冷水换成盐酸
D.把烧杯中的冷水换成氢氧化钠溶液
(2)乙同学设计实验验证:非金属元素的非金属性越强,其最高价含氧酸的酸性就越强。他设计了下图装置以验证碳、氮、硅元素的非金属性强弱。乙同学设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,其浓溶液在常温下可与铜反应;B是块状固体;烧杯中盛放C的水溶液,打开分液漏斗的活塞后,C中可观察到白色胶状沉淀生成。
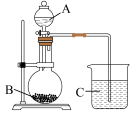
①写出所选用物质的化学式:A、_______ ; C、_______ 。
②写出烧瓶中发生反应的化学方程式:__________________________________ 。
③碳、氮、硅三种元素的非金属性由强到弱顺序为_______________________ 。
(1)甲同学在a、b、c、d四只烧杯里分别加入50 mL冷水,再分别滴加几滴酚酞溶液,依次加入大小相近的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象。
①甲同学设计实验的目的是验证:同一主族,从上到下元素的元素金属性逐渐增强;同一周期,从左到右,元素金属性
②反应最剧烈的烧杯里金属是
A、钠 B、镁 C、铝 D、钾;
③写出a烧杯里发生反应的离子方程式
④实验中发现b、c两只烧杯中几乎没有什么现象,要想达到实验的目的,请你帮助选择下列合适的方法
A.把镁、铝的金属块换成金属粉末
B.把烧杯中的冷水换成热水
C.把烧杯中的冷水换成盐酸
D.把烧杯中的冷水换成氢氧化钠溶液
(2)乙同学设计实验验证:非金属元素的非金属性越强,其最高价含氧酸的酸性就越强。他设计了下图装置以验证碳、氮、硅元素的非金属性强弱。乙同学设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,其浓溶液在常温下可与铜反应;B是块状固体;烧杯中盛放C的水溶液,打开分液漏斗的活塞后,C中可观察到白色胶状沉淀生成。

①写出所选用物质的化学式:A、
②写出烧瓶中发生反应的化学方程式:
③碳、氮、硅三种元素的非金属性由强到弱顺序为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某中学研究性学习小组为探究碳酸钠和碳酸氢钠两种物质的性质、制法和用途,进行了如下实验:
实验一:如图Ⅰ~Ⅳ所示。

(1)若用实验Ⅳ来验证碳酸钠和碳酸氢钠的热稳定性,则试管B中装入的固体最好是_______ ,能说明碳酸钠比碳酸氢钠稳定的实验现象是_______ 。
(2)若用实验来鉴别碳酸钠和碳酸氢钠两种固体,能达到实验目的的是(填装置序号)_______ 。其中能够说明泡沫灭火器中选择碳酸氢钠与酸反应制CO2而不选择碳酸钠的实验是_______ 。
(3)若测定Na2CO3固体中混有的少量NaHCO3的质量分数,采用实验Ⅲ能否达到实验目的?_____ ,若能,请说明其计算所需的数据,若不能,请简要说明理由:_______ 。
实验二:将碳酸氢钠溶液与澄清石灰水混合并充分反应。
(1)当石灰水过量时,反应的离子方程式为_______ 。
(2)当碳酸氢钠与氢氧化钙物质的量之比为2:1时,所得溶液中溶质的化学式为_______ 。
实验三:检验“侯氏制碱法”制得的纯碱中是否混有食盐和小苏打。
(1)检验纯碱中是否混有食盐的试剂是_______ ;
(2)证明纯碱中混有小苏打的实验方法是_______ 。
实验一:如图Ⅰ~Ⅳ所示。

(1)若用实验Ⅳ来验证碳酸钠和碳酸氢钠的热稳定性,则试管B中装入的固体最好是
(2)若用实验来鉴别碳酸钠和碳酸氢钠两种固体,能达到实验目的的是(填装置序号)
(3)若测定Na2CO3固体中混有的少量NaHCO3的质量分数,采用实验Ⅲ能否达到实验目的?
实验二:将碳酸氢钠溶液与澄清石灰水混合并充分反应。
(1)当石灰水过量时,反应的离子方程式为
(2)当碳酸氢钠与氢氧化钙物质的量之比为2:1时,所得溶液中溶质的化学式为
实验三:检验“侯氏制碱法”制得的纯碱中是否混有食盐和小苏打。
(1)检验纯碱中是否混有食盐的试剂是
(2)证明纯碱中混有小苏打的实验方法是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】某学习小组的同学在实验室研究Na2CO3与NaHCO3的性质。
实验I:

(1)产生气体的速率A___ B(填“>”或“<”或“=”),结合化学用语说明原因_________ 。
(2)产生气体的体积A___ B (填“>" 或“<”或“=”),标准状况下,A烧杯中产生气体的体积为____ L。
(3)任意写出一种将NaHCO3转变为Na2CO3的方法______________ (用化学方程式表示)。
实验Ⅱ:1 mL 0.1mol/L NaHCO3溶液与l mL 0.01 mol/L Ca(OH)2溶液混合产生CaCO3白色沉淀。
(4)同学们设计了如下实验方案,验证上述反应过程,请将方案补充完整:
实验步骤
实验现象
i.取1 mL 0.1 mol/LNaHCO3溶液。向其中加入1 mL 0.0 1 mol/L CaCl2 溶液
无明显现象
ⅱ.向上述溶液中滴加________
______________
实验I:

(1)产生气体的速率A
(2)产生气体的体积A
(3)任意写出一种将NaHCO3转变为Na2CO3的方法
实验Ⅱ:1 mL 0.1mol/L NaHCO3溶液与l mL 0.01 mol/L Ca(OH)2溶液混合产生CaCO3白色沉淀。
(4)同学们设计了如下实验方案,验证上述反应过程,请将方案补充完整:
实验步骤
实验现象
i.取1 mL 0.1 mol/LNaHCO3溶液。向其中加入1 mL 0.0 1 mol/L CaCl2 溶液
无明显现象
ⅱ.向上述溶液中滴加
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学小组欲测定某NaHCO3和NaCl混合物中NaHCO3的质量分数,用了两种不同的方法。回答下列问题:
Ⅰ.甲同学用下图所示装置进行测定。在检查完装置气密性后,他将一定质量的待测样品装入装置B中,加热前,先对已连接好的装置A、B和C通入一段时间的空气,再连接装置D、E;停止加热后,又继续通入一段时间的空气。
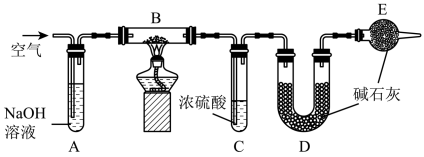
已知:a. 浓硫酸常用于吸收水蒸气。
b. 碱石灰是固体氢氧化钠和氧化钙的混合物。
(1)写出B装置加热时发生反应化学方程式:_______ 。
(2)第一次通入空气的目的是_______ ;第二次通入空气的目的是_______ 。若没有装置E,可能会造成测定结果 _______ (填“偏大”“偏小”或“不变”。)
(3)测定实验前后装置_______ (填字母)的质量,其质量差即为样品产生的二氧化碳的质量。若上述实验测得二氧化碳的质量为 6.6 g,甲同学称量样品的质量为28.0g,则该样品中NaHCO3的质量分数为_______ 。
II.乙同学用图中所示方法和步骤进行实验:

(4)写出①中反应的离子方程式_______ 。
(5)确定溶液M中含有过量氢氧化钡的方法为_______ 。
(6)乙同学测得样品中NaHCO3的质量分数为_______ 。(用含x、y的代数式表示)
Ⅰ.甲同学用下图所示装置进行测定。在检查完装置气密性后,他将一定质量的待测样品装入装置B中,加热前,先对已连接好的装置A、B和C通入一段时间的空气,再连接装置D、E;停止加热后,又继续通入一段时间的空气。

已知:a. 浓硫酸常用于吸收水蒸气。
b. 碱石灰是固体氢氧化钠和氧化钙的混合物。
(1)写出B装置加热时发生反应化学方程式:
(2)第一次通入空气的目的是
(3)测定实验前后装置
II.乙同学用图中所示方法和步骤进行实验:

(4)写出①中反应的离子方程式
(5)确定溶液M中含有过量氢氧化钡的方法为
(6)乙同学测得样品中NaHCO3的质量分数为
您最近一年使用:0次



