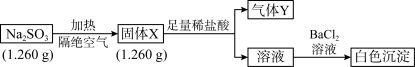
某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如图所示(部分反应物或生成物未列出),其中E为白色沉淀,I为红褐色沉淀。
(1)写出下列物质的化学式:F___ ,G___ 。
(2)分离粉末状混合物最简单的方法是___ 。
(3)D→E转化中,加入足量的X,试剂X可能是___ ,写出其离子方程式___ 。
A.饱和NaCl溶液 B.NaOH溶液 C.氨水 D.Ba(OH)2溶液
(4)A→C的离子方程式___ 。
(5)检验G溶液中的阳离子的方法___ 。

(1)写出下列物质的化学式:F
(2)分离粉末状混合物最简单的方法是
(3)D→E转化中,加入足量的X,试剂X可能是
A.饱和NaCl溶液 B.NaOH溶液 C.氨水 D.Ba(OH)2溶液
(4)A→C的离子方程式
(5)检验G溶液中的阳离子的方法
更新时间:2019-12-10 10:32:52
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】化合物A由四种常见元素组成。某同学为探究其组成进行了如图实验:

已知A在隔绝空气灼烧时发生的是非氧化还原反应,白色沉淀甲是一种盐形成的纯净物。
请回答下列问题:
(1)化合物A中所含的元素除Cu外,还有___ (用元素符号表示)。
(2)化合物A可以通过向蓝色溶液M中加入NaOH溶液来制备,写出生成A的化学方程式:___ 。
(3)写出向蓝色溶液M中加入Na2SO3溶液生成白色沉淀甲的离子方程式:___ 。

已知A在隔绝空气灼烧时发生的是非氧化还原反应,白色沉淀甲是一种盐形成的纯净物。
请回答下列问题:
(1)化合物A中所含的元素除Cu外,还有
(2)化合物A可以通过向蓝色溶液M中加入NaOH溶液来制备,写出生成A的化学方程式:
(3)写出向蓝色溶液M中加入Na2SO3溶液生成白色沉淀甲的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】下表是元素周期表的一部分,针对表中的①~⑩中10种元素用元素符号或化学式填空回答以下问题:
Ⅰ.填写下列空白:
(1)非金属性最强的元素是___________ (填元素符号),
(2)写出①与③形成原子个数比为1:1化合物的电子式:____________ ,该化合物酸性条件下与高锰酸钾反应的离子方程式:__________________________
(3)最高价氧化物对应的水化物中碱性最强的是_______ (填化学式),写出该物质与⑦的最高价氧化物对应的水化物反应的离子方程式为:____________ 。
(4)由①②③⑩四种元素中的三种组成的一种强酸,该强酸的稀溶液与铜反应的离子方程式____________________________
Ⅱ.由上述部分元素组成的物质间,在一定条件下,可以发生下图中的变化,其中A是一种淡黄色固体,可作供氧剂,X是一种氢化物,常温下为液体。则:
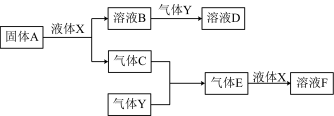
(1)A与液体X反应的化学方程式:____________________________ ;
(2)气体Y是一种大气污染物,无色、有刺激性气味的气体,直接排放会形成酸雨。写出气体Y与氯水反应的离子方程式:___________________________ ;
(3)在100 mL 18 mol/L的F浓溶液中加入过量铜片,加热使之充分反应,产生气体的体积为11.2 L(标况下),则反应过程中转移的电子数为__________ (用“NA”表示)
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
(1)非金属性最强的元素是
(2)写出①与③形成原子个数比为1:1化合物的电子式:
(3)最高价氧化物对应的水化物中碱性最强的是
(4)由①②③⑩四种元素中的三种组成的一种强酸,该强酸的稀溶液与铜反应的离子方程式
Ⅱ.由上述部分元素组成的物质间,在一定条件下,可以发生下图中的变化,其中A是一种淡黄色固体,可作供氧剂,X是一种氢化物,常温下为液体。则:

(1)A与液体X反应的化学方程式:
(2)气体Y是一种大气污染物,无色、有刺激性气味的气体,直接排放会形成酸雨。写出气体Y与氯水反应的离子方程式:
(3)在100 mL 18 mol/L的F浓溶液中加入过量铜片,加热使之充分反应,产生气体的体积为11.2 L(标况下),则反应过程中转移的电子数为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】下列框图中的A~J是中学化学中常见的八种物质,所有物质均由短周期元素组成,已知常温、常压下D为无色液体, C、E、G均为气体单质,B为金属,I是由3个原子组成的一元含氧弱酸分子, A~J可发生如下转化:

请填写下列空白:
(1)G的名称为_______ ,F的电子式为_______ 。
(2)15.6gA与D完全反应,转移的电子的物质的量为_______ 。
(3)常温下,A为一种_______ 色的固体,它的一种重要用途是_______ 。
(4)写出D、G反应转化为I和J的离子方程式_______ 。

请填写下列空白:
(1)G的名称为
(2)15.6gA与D完全反应,转移的电子的物质的量为
(3)常温下,A为一种
(4)写出D、G反应转化为I和J的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】M、N是两种金属单质,W是一种强碱,焰色试验呈黄色,Y在食品行业中可用于焙制糕点;a、b、c是常见的单质或氧化物,它们之间存在如下转化关系,按要求回答问题。

(1)c是常见的温室气体之一,则c的化学式为_______ 。
(2)在溶液中实现过程①和②的措施分别是①_______ 、②_______ (各限填一种)
(3)金属M长期置于空气中,最终后形成的物质是_______ (写化学式)。
(4)N→Z的离子方程式为_______ 。
(5)将1 mol F和2 mol Y置于密闭容器中,加热,充分反应后排出气体,排出气体的成分是_______ 。
(6)将2 mol F投入到含有1 mol G的溶液中充分反应,发生反应的总的离子方程式为_______ 。
(7)向0.1 mol/L 的G溶液中逐滴滴加0.1mol/L的W溶液至过量,整个过程中的实验现象为_______ 。

(1)c是常见的温室气体之一,则c的化学式为
(2)在溶液中实现过程①和②的措施分别是①
(3)金属M长期置于空气中,最终后形成的物质是
(4)N→Z的离子方程式为
(5)将1 mol F和2 mol Y置于密闭容器中,加热,充分反应后排出气体,排出气体的成分是
(6)将2 mol F投入到含有1 mol G的溶液中充分反应,发生反应的总的离子方程式为
(7)向0.1 mol/L 的G溶液中逐滴滴加0.1mol/L的W溶液至过量,整个过程中的实验现象为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】某学习小组用如图装置测定铝镁合金中铝的质量分数和铝的相对原子质量。

(1)A中试剂为_______ 。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是_______ 。记录C的液面位置时,除视线平视外,还应_______ 。
(3)B中发生反应的化学方程式为_______ 。
(4)若实验用铝镁合金的质量为ag,测得氢气体积为bmL(已换算为标准状况),B中剩余固体的质量为cg,则铝的相对原子质量为_______ 。
(5)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将_______ 。(填“偏大”、“偏小”、“不受影响”)

(1)A中试剂为
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是
(3)B中发生反应的化学方程式为
(4)若实验用铝镁合金的质量为ag,测得氢气体积为bmL(已换算为标准状况),B中剩余固体的质量为cg,则铝的相对原子质量为
(5)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】某课外小组研究铝土矿中Al2O3的含量。查阅资料得知,铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:
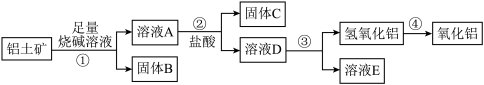
(1)第①步,向铝土矿中加入足量烧碱溶液后,发生反应的离子方程式是_______________________________________________________________ ;_____________________________________________________________ ;
第③步中,生成氢氧化铝的离子方程式是_____________________________________________________________ 。
(2)将实验过程中所得固体精确称量,课外小组发现所得氢氧化铝固体的质量与原铝土矿质量相等,则该铝土矿中Al2O3的质量分数是________ 。(保留一位小数)
(3)工业上制取AlCl3用Al2O3与C、Cl2在高温条件下反应,每消耗0.5 mol 碳单质,转移1mol电子,反应的化学方程式是_____________________________ 。

(1)第①步,向铝土矿中加入足量烧碱溶液后,发生反应的离子方程式是
第③步中,生成氢氧化铝的离子方程式是
(2)将实验过程中所得固体精确称量,课外小组发现所得氢氧化铝固体的质量与原铝土矿质量相等,则该铝土矿中Al2O3的质量分数是
(3)工业上制取AlCl3用Al2O3与C、Cl2在高温条件下反应,每消耗0.5 mol 碳单质,转移1mol电子,反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】某待测液中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 12种离子中的某几种.为探究其组成现设计如图流程.
12种离子中的某几种.为探究其组成现设计如图流程.
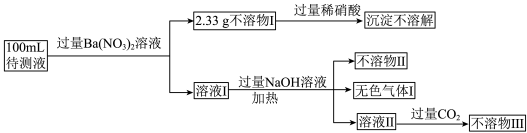
已知该待测液中所有离子的浓度均相等.
(1)待测液中
______  .
.
(2)生成不溶物Ⅰ的离子方程式为______ .
(3)不溶物Ⅱ和不溶物Ⅲ的化学式分别为______ 、______ .
(4)若向溶液Ⅰ中加入过量的稀盐酸,观察到的现象为______ ;若向不溶物Ⅲ中加入过量的NaOH溶液,反应的离子方程式为______ .
(5)待测液中一定不含的离子是______ .
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 12种离子中的某几种.为探究其组成现设计如图流程.
12种离子中的某几种.为探究其组成现设计如图流程.
已知该待测液中所有离子的浓度均相等.
(1)待测液中

 .
.(2)生成不溶物Ⅰ的离子方程式为
(3)不溶物Ⅱ和不溶物Ⅲ的化学式分别为
(4)若向溶液Ⅰ中加入过量的稀盐酸,观察到的现象为
(5)待测液中一定不含的离子是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下:
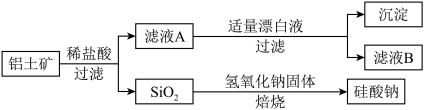
(1)在滤液A中加入漂白液,所得滤液B显酸性。
①滤液A中加入漂白液的目的是___________ (用离子方程式表示)。
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为_________(填代号)。
(2)由滤液B制备少量无水AlCl3(AlCl3极易在空气中水解)。
①由滤液B制备氯化铝晶体(将AlCl3·6H2O)涉及的操作为_______ 、冷却结晶、________ (填操作名称)、洗涤。
②将AlCl3·6H2O溶于浓硫酸进行蒸馏,也能得到一定量的无水AlCl3,此原理是利用浓硫酸下列性质中的________ (填序号)。
(3)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为_____ (填代号)。

(1)在滤液A中加入漂白液,所得滤液B显酸性。
①滤液A中加入漂白液的目的是___________ (用离子方程式表示)。
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为_________(填代号)。
| A.氢氧化钠溶液 | B.硫酸溶液 | C.氨水 | D.二氧化碳 |
①由滤液B制备氯化铝晶体(将AlCl3·6H2O)涉及的操作为_______ 、冷却结晶、________ (填操作名称)、洗涤。
②将AlCl3·6H2O溶于浓硫酸进行蒸馏,也能得到一定量的无水AlCl3,此原理是利用浓硫酸下列性质中的________ (填序号)。
| A.氧化性 | B.吸水性 | C.脱水性 |
A. | B. | C. | D. |
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】A、B、C、D四种物质或其水溶液有如图转化关系。
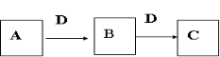
试回答下列问题:
(1)若A为金属单质,C为淡黄色固体,写出物质C的一种用途:_________ ;写出物质C与水反应的化学方程式_________ 。若不考虑其他离子的影响,向同时含有下列离子的混合溶液中加入少量固体C后,再继续滴加足量的稀硫酸,最终离子数目不变的是_________ 。
a.Na+ b.Mg2+ c.K+ d.Fe2+ e.Fe3+
(2)若A是一种引起温室效应的气体,D为焰色试验显黄色的强碱,则B→C的离子方程式_________ ,若A为焰色试验显黄色的强碱, D为引起温室效应的气体,B→ C的离子方程式_________ 。
(3)若A、B、C中均含有同一种非金属元素,A单质常用来自来水杀菌消毒,D是目前使用量最大的金属。实验室常用鉴定B中金属阳离子的试剂(填名称)_________ 。向物质C的溶液中滴加氢氧化钠后得到的沉淀会有一系列颜色变化,试写出该转化的化学反应方程式:_________ 。

试回答下列问题:
(1)若A为金属单质,C为淡黄色固体,写出物质C的一种用途:
a.Na+ b.Mg2+ c.K+ d.Fe2+ e.Fe3+
(2)若A是一种引起温室效应的气体,D为焰色试验显黄色的强碱,则B→C的离子方程式
(3)若A、B、C中均含有同一种非金属元素,A单质常用来自来水杀菌消毒,D是目前使用量最大的金属。实验室常用鉴定B中金属阳离子的试剂(填名称)
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】分已知A、B、C、D分别是AlCl3、BaCl2、FeSO4、NaOH四种化合物中的一种,它们的水溶液之间的一些反应现象如下:
①A+B→白色沉淀,加入稀硝酸,沉淀不溶解。
②B+D→白色沉淀,在空气中放置,沉淀由白色转化为红褐色。
③C+D→白色沉淀,继续加入D溶液,白色沉淀逐渐消失。
(1)试推断A___________ 、B___________ (填化学式)。
(2)写出下列反应的化学方程式:
i.实验②中沉淀由白色转化为红褐色的化学方程式_______________
ii.C溶液与D溶液反应后生成的白色沉淀溶解于D溶液中的离子方程式_________________ 。
①A+B→白色沉淀,加入稀硝酸,沉淀不溶解。
②B+D→白色沉淀,在空气中放置,沉淀由白色转化为红褐色。
③C+D→白色沉淀,继续加入D溶液,白色沉淀逐渐消失。
(1)试推断A
(2)写出下列反应的化学方程式:
i.实验②中沉淀由白色转化为红褐色的化学方程式
ii.C溶液与D溶液反应后生成的白色沉淀溶解于D溶液中的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。
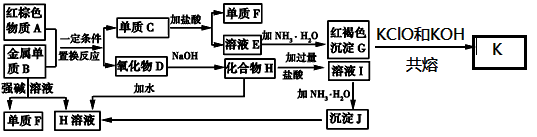
(1)单质F的摩尔质量是_______________ 。
(2)写出单质B与强碱溶液反应的离子方程式___________________________ ,写出由沉淀J生成H溶液的离子方程式_______________________________ 。
(3)溶液E中加入氨水时,先生成白色沉淀L,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式______________________________ 。
(4)K是一种集消毒与净水为一体的新型净水剂,试写出G→K的化学方程式:______________________
(5)溶液I中所含金属离子是__________________ 。

(1)单质F的摩尔质量是
(2)写出单质B与强碱溶液反应的离子方程式
(3)溶液E中加入氨水时,先生成白色沉淀L,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式
(4)K是一种集消毒与净水为一体的新型净水剂,试写出G→K的化学方程式:
(5)溶液I中所含金属离子是
您最近一年使用:0次