运用元素周期律研究元素及其化合物的性质具有重要的意义。
I.部分短周期主族元素的最高价氧化物对应水化物(浓度均为0.01mol·L-1)溶液的pH和原子序数的关系如图所示。
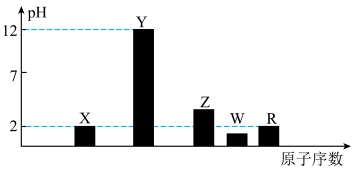
(1)元素R在周期表中的位置是_______ ;元素Z的原子结构示意图是________ 。
(2)元素Y和W形成的Y2W2型化合物中含有化学键的类型为________ 。
II.短周期元素C、O、S能形成多种化合物,如CO2、CS2、COS等。
(1)下列能说明碳、硫两种元素非金属性相对强弱的是__________ (填序号)
A. S与H2发生化合反应比C与H2化合更容易
B. 酸性:H2SO3 >H2CO3
C. CS2中碳元素为+4价,硫元素为-2价
(2)铅(Pb)、锡(Sn)、锗(Ge)与元素C同主族。常温下其单质在空气中,锡、锗不反应,而铅表面会生成一层氧化铅;锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:
①锗的原子序数为_________ 。
②它们+4价氢氧化物的碱性由强到弱顺序为____________ (填化学式)。
(3)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害,其分子结构和CO2相似。羰基硫(COS)的电子式为:______________________ 。
I.部分短周期主族元素的最高价氧化物对应水化物(浓度均为0.01mol·L-1)溶液的pH和原子序数的关系如图所示。

(1)元素R在周期表中的位置是
(2)元素Y和W形成的Y2W2型化合物中含有化学键的类型为
II.短周期元素C、O、S能形成多种化合物,如CO2、CS2、COS等。
(1)下列能说明碳、硫两种元素非金属性相对强弱的是
A. S与H2发生化合反应比C与H2化合更容易
B. 酸性:H2SO3 >H2CO3
C. CS2中碳元素为+4价,硫元素为-2价
(2)铅(Pb)、锡(Sn)、锗(Ge)与元素C同主族。常温下其单质在空气中,锡、锗不反应,而铅表面会生成一层氧化铅;锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:
①锗的原子序数为
②它们+4价氢氧化物的碱性由强到弱顺序为
(3)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害,其分子结构和CO2相似。羰基硫(COS)的电子式为:
更新时间:2019-12-23 09:42:58
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)A是________ ,B是________ ,E是_________ 。(请填写元素符号)
(2) 写出C元素基态原子的电子排布式_________________________ 。
(3) 用轨道表示式表示D元素原子的最外层电子构型____________________ 。
(1)A是
(2) 写出C元素基态原子的电子排布式
(3) 用轨道表示式表示D元素原子的最外层电子构型
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】如图是部分短周期元素(用字母x等表示)化合价与原子序数的关系图。

根据判断出的元素回答问题:
(1)h在周期表中的位置是__________ 。
(2)比较z、f、g、r常见离子的半径大小(用化学式表示,下同):______ >______ >______ >______ ;比较r、m的最高价氧化物对应水化物的酸性强弱:______ >______ >;比较d、m的氢化物的沸点:______ >______ 。
(3)x与氢元素能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质是(写分子式)______ ,实验室制取该物质的化学方程式为:____________________________________ 。
(4)由y、m和氢元素组成一种离子化合物,写出其电子式:___________________________ 。
(5)用铅蓄电池作电源,惰性电极电解饱和em溶液,则电解反应的生成物为(写化学式)___________________________ 。铅蓄电池放电时正极反应式为式)___________________________ 。

根据判断出的元素回答问题:
(1)h在周期表中的位置是
(2)比较z、f、g、r常见离子的半径大小(用化学式表示,下同):
(3)x与氢元素能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质是(写分子式)
(4)由y、m和氢元素组成一种离子化合物,写出其电子式:
(5)用铅蓄电池作电源,惰性电极电解饱和em溶液,则电解反应的生成物为(写化学式)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、B、C、D、E为短周期元素,A-E原子序数依次增大,质子数之和为40,B、C同周期,A、D同主族,A、C能形成两种液态化合物A2C和A2C2,E是地壳中含量最多的金属元素。
(1)E元素在周期表中的位置为__________ ;B、C的氢化物稳定性强的是________ (用化学式表示,下同);B、C、D组成的化合物中含有的化学键为_____________
(2)D2C2的电子式是_________ ,将D的单质投入A2C中,反应后得到一种无色溶液,E的单质在该无色溶液中反应的离子方程式为______________ ;
(3)元素D的单质在一定条件下,能与A单质化合生成氢化物DA,熔点为800℃。DA能与水反应放出氢气,化学反应方程式为_____________ 。
(4)废印刷电路版上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡既达到了上述目的,又保护了环境,试写出反应的化学方程式__________________________
(1)E元素在周期表中的位置为
(2)D2C2的电子式是
(3)元素D的单质在一定条件下,能与A单质化合生成氢化物DA,熔点为800℃。DA能与水反应放出氢气,化学反应方程式为
(4)废印刷电路版上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡既达到了上述目的,又保护了环境,试写出反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】短周期主族元素W、X、Y、Z的原子序数依次增大,W的最简单氢化物甲是一种能使湿润的红色石蕊试纸变蓝的无色气体,常用作制冷剂,Y的金属性是所有短周期主族元素中最强的,Z与X属于同一主族,Z与Y属于同一周期。
(1)元素W在周期表中位置为_______________ 。
(2)元素W的另一常见氢化物乙是一种高能燃料,为18电子微粒,乙的结构式为___________ 。
(3)X、Y、Z的原子半径由小到大的顺序为_________________ 。
(4)若X与Z的最外层电子数之和是W核外电子数的2倍,甲可与Z单质发生置换反应,产物之一可作化肥,其反应的化学方程式为___________________ ,该产物化肥中含有的化学键有________________ 。
(5)若由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气味气体产生。则元素Z是______ (填元素符号),反应的离子方程式为________________ 。
(1)元素W在周期表中位置为
(2)元素W的另一常见氢化物乙是一种高能燃料,为18电子微粒,乙的结构式为
(3)X、Y、Z的原子半径由小到大的顺序为
(4)若X与Z的最外层电子数之和是W核外电子数的2倍,甲可与Z单质发生置换反应,产物之一可作化肥,其反应的化学方程式为
(5)若由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气味气体产生。则元素Z是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分,针对所给的元素,完成下列各小题
(1)第三周期中原子半径最大、金属性最强元素是________ (填元素名称);
(2)氖原子结构示意图为_______________ ;(3)N与O中,原子半径较大的是__________ 。
(4)形成化合物种类最多的元素是__________ ;它的最高价氧化物对应的水化物的化学式______________
(5)铝是大自然赐予人类的宝物。它其中的一个用途是作为铝热剂,该反应的化学方程式为_______________________________
(6)N元素形成的一种氢化物的化学式是__________ ,俗话说“雷雨发庄稼”,请写出二氧化氮溶于水的反应化学方程式__________________________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | C | N | O | F | Ne | |||
| 3 | Na | Mg | Al | Si | P | S | Cl | |
| 4 | K | Ca | Br |
(1)第三周期中原子半径最大、金属性最强元素是
(2)氖原子结构示意图为
(4)形成化合物种类最多的元素是
(5)铝是大自然赐予人类的宝物。它其中的一个用途是作为铝热剂,该反应的化学方程式为
(6)N元素形成的一种氢化物的化学式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表为元素周期表的一部分,请根据元素①~⑧所处的位置回答下列问题:
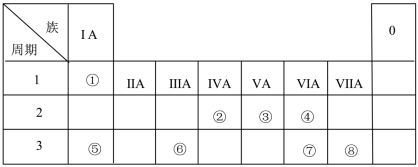
(1)元素⑦的原子结构示意图为_____ ,元素④⑦的最简单氢化物的稳定性关系为_____ (用化学式表示)。
(2)34号元素Se与④同主族,则Se在元素周期表中的位置为_____ 。
(3)元素①~⑧形成的物质中,最高价氧化物的水化物碱性最强的是_____ ,最高价氧化物的水化物酸性最强的是_____ (填化学式)。
(4)由元素④⑤组成原子个数比为 的化合物中含化学键类型为
的化合物中含化学键类型为_____ 。
(5)③④⑥元素简单离子半径由大到小的排列顺序是_____ (用离子符号表示)。

(1)元素⑦的原子结构示意图为
(2)34号元素Se与④同主族,则Se在元素周期表中的位置为
(3)元素①~⑧形成的物质中,最高价氧化物的水化物碱性最强的是
(4)由元素④⑤组成原子个数比为
 的化合物中含化学键类型为
的化合物中含化学键类型为(5)③④⑥元素简单离子半径由大到小的排列顺序是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E是短周期元素,原子序数依次增大,B、C同周期,C的非金属性在元素周期表中最强,A、D同主族、隔周期,E元素原子最外层的p能级电子数是最外层的s能级电子数的一半。A、B能形成常温常压下两种液态化合物甲和乙,原子个数比分别为2:1和1:1.根据以上信息回答下列问题:
(1)甲、乙两种化合物中含有非极性共价键的物质的电子式是___________ ,C元素在元素周期表中的位置是___________ 。
(2)C和D形成的简单离子中,半径较小的是___________ (填离子符号)。
(3)将D的单质投入甲中,待D消失后再向溶液中加入E的单质,此时发生反应的化学方程式是___________ 。
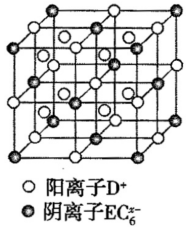
(4)C、D、E可组成离子化合物,其晶胞结构如图所示,阳离子D*(用○表示)位于正方体棱的中点和正方体内部;阴离子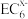 (用
(用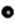 表示)位于该正方体的顶点和面心。该化合物的化学式是
表示)位于该正方体的顶点和面心。该化合物的化学式是___________ 。
(1)甲、乙两种化合物中含有非极性共价键的物质的电子式是
(2)C和D形成的简单离子中,半径较小的是
(3)将D的单质投入甲中,待D消失后再向溶液中加入E的单质,此时发生反应的化学方程式是
(4)C、D、E可组成离子化合物,其晶胞结构如图所示,阳离子D*(用○表示)位于正方体棱的中点和正方体内部;阴离子
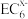 (用
(用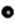 表示)位于该正方体的顶点和面心。该化合物的化学式是
表示)位于该正方体的顶点和面心。该化合物的化学式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】有A、B、C、D、E五种短周期元素,它们的原子序数由A到E依次增大,A原子核内只有一个质子,已知B和D原子有相同的电子层数,且B的L层电子数是K层电子数的两倍,E在空气中燃烧时呈现黄色火焰,E的单质在加热下与D的单质充分反应,可以得到淡黄色固态化合物,试根据以上叙述回答:
(1)写出元素C在周期表中位置________________
(2)E的单质在加热下与D的单质充分反应,可以得到淡黄色固态化合物的电子式_________________
(3)C的氢化物与其最高价含氧酸反应的化学方程式及产物中阳离子的电子式__________ 、__________
(4)B、C、D的氢化物的稳定性的由大到小的顺序为:___________ (氢化物的化学式),理由是:________________
(1)写出元素C在周期表中位置
(2)E的单质在加热下与D的单质充分反应,可以得到淡黄色固态化合物的电子式
(3)C的氢化物与其最高价含氧酸反应的化学方程式及产物中阳离子的电子式
(4)B、C、D的氢化物的稳定性的由大到小的顺序为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】运用元素周期律研究元素及其化合物的性质具有重要的意义。
I.部分短周期主族元素的最高价氧化物对应的水化物 浓度均为
浓度均为 溶液的pH和原子序数的关系如图所示。
溶液的pH和原子序数的关系如图所示。

 元素R在周期表中的位置是
元素R在周期表中的位置是______ ;元素Z的原子结构示意图是______ 。
 元素Y和W形成的
元素Y和W形成的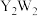 型化合物中含有化学键的类型为
型化合物中含有化学键的类型为______ 。
 短周期元素C、O、S能形成多种化合物,如
短周期元素C、O、S能形成多种化合物,如 、
、 、COS等。
、COS等。
 下列能说明碳、硫两种元素非金属性相对强弱的是
下列能说明碳、硫两种元素非金属性相对强弱的是______  填序号
填序号
A.S与 发生化合反应比C与
发生化合反应比C与 化合更容易
化合更容易
B.酸性:
C. 中碳元素为
中碳元素为 价,硫元素为
价,硫元素为 价
价
 铅
铅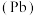 、锡
、锡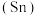 、锗
、锗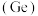 与元素C同主族。常温下其单质在空气中,锡、锗不反应,而铅表面会生成一层氧化铅;锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:
与元素C同主族。常温下其单质在空气中,锡、锗不反应,而铅表面会生成一层氧化铅;锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:
 锗的原子序数为
锗的原子序数为______ 。
 它们
它们 价氢氧化物的碱性由强到弱顺序为
价氢氧化物的碱性由强到弱顺序为______  填化学式
填化学式 。
。
 羰基硫
羰基硫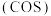 可作为一种熏蒸剂,能防止某些昆虫、线虫的危害,其分子结构和
可作为一种熏蒸剂,能防止某些昆虫、线虫的危害,其分子结构和 相似。
相似。
 用电子式表示羰基硫
用电子式表示羰基硫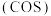 的形成过程:
的形成过程:______ 。
 羰基硫
羰基硫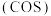 用氢氧化钠溶液处理及利用的过程如图:
用氢氧化钠溶液处理及利用的过程如图:
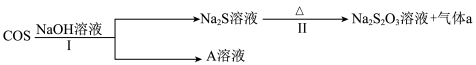
已知A是一种正盐,则A的化学式为______ ;若气体a为单质,反应II的离子方程式为______ 。
I.部分短周期主族元素的最高价氧化物对应的水化物
 浓度均为
浓度均为 溶液的pH和原子序数的关系如图所示。
溶液的pH和原子序数的关系如图所示。
 元素R在周期表中的位置是
元素R在周期表中的位置是 元素Y和W形成的
元素Y和W形成的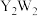 型化合物中含有化学键的类型为
型化合物中含有化学键的类型为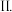 短周期元素C、O、S能形成多种化合物,如
短周期元素C、O、S能形成多种化合物,如 、
、 、COS等。
、COS等。 下列能说明碳、硫两种元素非金属性相对强弱的是
下列能说明碳、硫两种元素非金属性相对强弱的是 填序号
填序号
A.S与
 发生化合反应比C与
发生化合反应比C与 化合更容易
化合更容易B.酸性:

C.
 中碳元素为
中碳元素为 价,硫元素为
价,硫元素为 价
价 铅
铅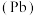 、锡
、锡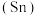 、锗
、锗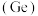 与元素C同主族。常温下其单质在空气中,锡、锗不反应,而铅表面会生成一层氧化铅;锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:
与元素C同主族。常温下其单质在空气中,锡、锗不反应,而铅表面会生成一层氧化铅;锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论: 锗的原子序数为
锗的原子序数为 它们
它们 价氢氧化物的碱性由强到弱顺序为
价氢氧化物的碱性由强到弱顺序为 填化学式
填化学式 。
。 羰基硫
羰基硫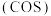 可作为一种熏蒸剂,能防止某些昆虫、线虫的危害,其分子结构和
可作为一种熏蒸剂,能防止某些昆虫、线虫的危害,其分子结构和 相似。
相似。 用电子式表示羰基硫
用电子式表示羰基硫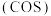 的形成过程:
的形成过程: 羰基硫
羰基硫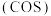 用氢氧化钠溶液处理及利用的过程如图:
用氢氧化钠溶液处理及利用的过程如图: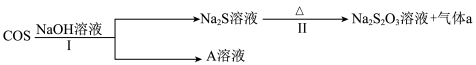
已知A是一种正盐,则A的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表是元素周期表的前三周期及其中的部分元素,请回答相关问题
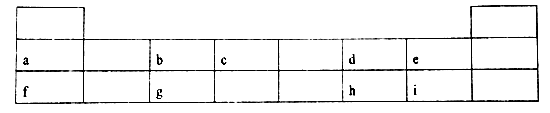
(1) a、f、g 元素最高价氧化物的水化物碱性由强到弱的顺序是__________ (用化学式表示)。表中所给元素中金属性最强的与非金属性最强的形成的化合物溶液显______ (填“中性“酸性”或“碱性” )。
(2) 氢元素可与其它元素形成_________ (填选项序号)等化学键。
A.极性共价键 B.非极性共价键 C.氢键 D.离子键
(3)d、f、h三种元素可形成一种有强还原性的化合物,该化合物中含有非极性键,其化学式为____ ,向该化合物的水溶液中加入盐酸发生反应的离子方程式为______________ 。
(4)表中所给的某两种元素可形成一种常见的有机溶剂,可用于萃取碘水中的碘单质,萃取后有机层的颜色为___________ ,分液时有机层应从________ (填“下口流出“或“上口倒出”)。该有机溶剂的电子式是_______ 。

(1) a、f、g 元素最高价氧化物的水化物碱性由强到弱的顺序是
(2) 氢元素可与其它元素形成
A.极性共价键 B.非极性共价键 C.氢键 D.离子键
(3)d、f、h三种元素可形成一种有强还原性的化合物,该化合物中含有非极性键,其化学式为
(4)表中所给的某两种元素可形成一种常见的有机溶剂,可用于萃取碘水中的碘单质,萃取后有机层的颜色为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】五种短周期元素A、B、C、D、E的原子序数依次增大。A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物是常用的食品调味剂。
回答下列问题:
(1)写出元素D在周期表中的位置____________________________________________ 。
(2)五种元素中,原子半径最大的是________ (填元素符号),非金属最强的是________ (填元素符号)。
(3)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是________ (用化学式表示)。
(4)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为________ ,其中存在的化学键类型为_______________ 和________________ 。
(5)单质E与水反应的离子方程式为____________________________________________
回答下列问题:
(1)写出元素D在周期表中的位置
(2)五种元素中,原子半径最大的是
(3)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是
(4)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为
(5)单质E与水反应的离子方程式为
您最近一年使用:0次



