25. 运用元素周期律研究元素及其化合物的性质具有重要的意义。
I.部分短周期主族元素的最高价氧化物对应水化物(浓度均为0.01mol·L
-1)溶液的pH和原子序数的关系如图所示。
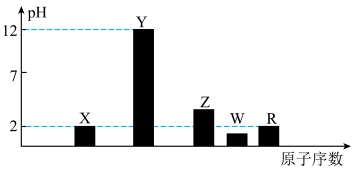
(1)元素R在周期表中的位置是
_______;元素Z的原子结构示意图是
________。
(2)元素Y和W形成的Y
2W
2型化合物中含有化学键的类型为
________。
II.短周期元素C、O、S能形成多种化合物,如CO
2、CS
2、COS等。
(1)下列能说明碳、硫两种元素非金属性相对强弱的是
__________(填序号)
A. S与H
2发生化合反应比C与H
2化合更容易
B. 酸性:H
2SO
3 >H
2CO
3C. CS
2中碳元素为+4价,硫元素为-2价
(2)铅(Pb)、锡(Sn)、锗(Ge)与元素C同主族。常温下其单质在空气中,锡、锗不反应,而铅表面会生成一层氧化铅;锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:
①锗的原子序数为
_________。
②它们+4价氢氧化物的碱性由强到弱顺序为
____________(填化学式)。
(3)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害,其分子结构和CO
2相似。羰基硫(COS)的电子式为:
______________________。