21.
Sn(核电荷数为50)是人类最早使用的元素之一,能形成
SnCl2,
SnCl4两种氯化物,
SnCl2常温下为白色晶体,具有一维链状的聚合结构,气态时以单分子形式存在,而
SnCl4常温下为无色液体.白锡和灰锡是
Sn的两种同素异形体,白锡的晶体结构中
Sn原子的配位数为4和6,灰锡的晶体结构与金刚石的晶体结构相似.白锡的密度大于灰锡的密度.
(1)
Sn元素外围电子排布式为
______.
(2)
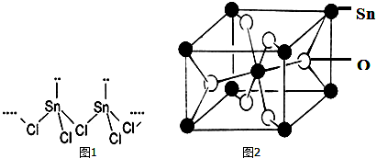
SnCl2的一维链状聚合结构如图1所示,在分子结构中存在的化学键是
______.
(3)
SnCl4与
CCl4中沸点较高的是
______.原因是
______.
(4)锡的某种氧化物的晶胞如图2,其化学式为
______.
(5)解释白锡分子的密度大于灰锡的密度的原因
____________________.