甲、乙、丙、丁、戊代表五种元素.请填空:
(1)甲元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素名称为_______ ,其基态原子的电子排布式为_______ .
(2)乙元素的负一价离子和丙元素的正一价离子的电子层结构都与氩相同,乙的元素符号为_______ ,丙元素的基态原子的电子排布式为_______ .
(3)丁元素的正三价离子的3d能级为半充满,丁的元素符号为_______ ,其基态原子的电子排布式为_______ .
(4)戊元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,该元素在周期表中的位置是_______ (指明周期与族),其基态原子价层电子排布式为_______ .
(1)甲元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素名称为
(2)乙元素的负一价离子和丙元素的正一价离子的电子层结构都与氩相同,乙的元素符号为
(3)丁元素的正三价离子的3d能级为半充满,丁的元素符号为
(4)戊元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,该元素在周期表中的位置是
更新时间:2017-04-24 21:00:03
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下表列出了A~R 9种元素在周期表中的位置:(用元素符号回答)
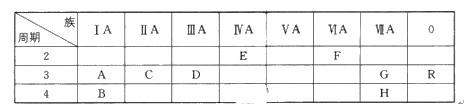
(1)这9种元素其中化学性质最不活泼的是________ ;
(2)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是_______________ ;
(3)A、B、C三种元素按原子半径由大到小的顺序排列为________ ;
(4)F元素氢化物的化学式是________ ,

(1)这9种元素其中化学性质最不活泼的是
(2)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是
(3)A、B、C三种元素按原子半径由大到小的顺序排列为
(4)F元素氢化物的化学式是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求回答下列问题:
(1)元素周期表中位于第8纵行的铁元素属于第______ 族;
(2)第3周期第ⅣA族元素的原子序数是______ ;
(3) 元素的原子序数为11,与之相邻的同族元素的原子序数是
元素的原子序数为11,与之相邻的同族元素的原子序数是______ ;
(4)所含元素超过18种的周期是第____________ 周期;
(5)短周期元素中,主族序数 周期序数的元素有
周期序数的元素有____________ (填元素符号)。
(1)元素周期表中位于第8纵行的铁元素属于第
(2)第3周期第ⅣA族元素的原子序数是
(3)
 元素的原子序数为11,与之相邻的同族元素的原子序数是
元素的原子序数为11,与之相邻的同族元素的原子序数是(4)所含元素超过18种的周期是第
(5)短周期元素中,主族序数
 周期序数的元素有
周期序数的元素有
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】如图是元素周期表的一部分,其中每个数字序号代表一种 短周期元素。根据表中所列①~⑩元素,请按要求回答下列问题:

(1)元素⑤形成的氧化物的电子式为_______ ;①、⑦两种元素的最高价氧化物的熔点较高的是________ (填化学式)。
(2)①~⑨元素的最高价氧化物的水化物中酸性最强的是_______ (填化学式)。
(3)由③④⑩三种元素组成的离子化合物中所含有的化学键有______ 。
(4)①的单质与②的最高价氧化物的水化物的浓溶液反应的化学方程式为_________ 。
(5)下列事实能说明③非金属性比⑧强的有___________ (填字母)。
a.通常状况下,③的单质是无色气体,⑧的单质是固体
b.③的单质与⑧的氢化物溶液反应,溶液变浑浊
c.③与⑧两元素的简单氢化物受热分解,前者的分解温度高
d.常温常压下,③与⑧两元素的简单氢化物的沸点,前者高

(1)元素⑤形成的氧化物的电子式为
(2)①~⑨元素的最高价氧化物的水化物中酸性最强的是
(3)由③④⑩三种元素组成的离子化合物中所含有的化学键有
(4)①的单质与②的最高价氧化物的水化物的浓溶液反应的化学方程式为
(5)下列事实能说明③非金属性比⑧强的有
a.通常状况下,③的单质是无色气体,⑧的单质是固体
b.③的单质与⑧的氢化物溶液反应,溶液变浑浊
c.③与⑧两元素的简单氢化物受热分解,前者的分解温度高
d.常温常压下,③与⑧两元素的简单氢化物的沸点,前者高
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】请回答下列有关问题。
(1) 元素按周期表分区属于
元素按周期表分区属于________ 区元素
(2)地壳中含量最多的三种元素 、
、 、
、 中,电负性最大的是
中,电负性最大的是______ 。
(3)钠在火焰上灼烧产生的黄光是一种_______ (填字母)
A.吸收光谱 B.发射光谱
(4) 分子的空间构型为
分子的空间构型为_______ 。
(5)钛被称为继铁、铝之后的第三金属,基态钛原子价电子层的电子排布图是______ 。
(6)基态 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为________ 。
(7) 分子中所有原子均满足8电子构型,
分子中所有原子均满足8电子构型, 分子中
分子中 键和
键和 键的个数比为
键的个数比为_______ 。
(1)
 元素按周期表分区属于
元素按周期表分区属于(2)地壳中含量最多的三种元素
 、
、 、
、 中,电负性最大的是
中,电负性最大的是(3)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(4)
 分子的空间构型为
分子的空间构型为(5)钛被称为继铁、铝之后的第三金属,基态钛原子价电子层的电子排布图是
(6)基态
 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为(7)
 分子中所有原子均满足8电子构型,
分子中所有原子均满足8电子构型, 分子中
分子中 键和
键和 键的个数比为
键的个数比为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以硼砂、萤石和浓硫酸为原料可制取有机合成的原料三氟化硼。反应原理为:B2O3(s)+3CaF2(s)+3H2SO4(浓)=2BF3(g)+3CaSO4(s)+3H2O(l)。请完成下列填空:
(1)萤石的电子式___________ ,已知BF3为非极性分子,则其分子构型可能为___________ (填编号)。
A. 三角锥形 B. 平面正三角形 C. 直线形 D. 正四面体形
(2)硼原子核外电子的轨道表示式___________ ,硼原子核外有___________ 种不同形状的电子云。
(3)该反应体系中除硼元素外的其他短周期元素的简单离子的半径由小到大排列的是(用离子符号表示)___________ 。
(4)其中O与S相比,非金属性较强的是___________ ,下列能比较它们非金属性强弱的有(填编号)___________ 。
A. 相互之间的置换反应 B. 最高价氧化物对应的水化物的酸性
C. 氢化物水溶液的酸性 D. 相互形成的化合物中元素的化合价
(1)萤石的电子式
A. 三角锥形 B. 平面正三角形 C. 直线形 D. 正四面体形
(2)硼原子核外电子的轨道表示式
(3)该反应体系中除硼元素外的其他短周期元素的简单离子的半径由小到大排列的是(用离子符号表示)
(4)其中O与S相比,非金属性较强的是
A. 相互之间的置换反应 B. 最高价氧化物对应的水化物的酸性
C. 氢化物水溶液的酸性 D. 相互形成的化合物中元素的化合价
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
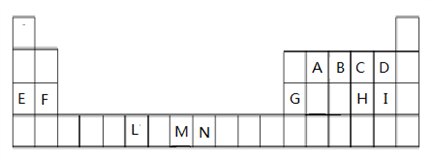
试回答下列问题:
(1)请写出元素M的基态原子的价电子排布式:________________________ 。
(2)标准状况下,11.2L AC2含有π键的数目为______ 。写出AC2的电子式:_________________ 。
(3)E、F、G的第一电离能由大到小的顺序为:____________ 。(填元素符号)
(4)LC2I2常温下为深红色液体,能与 CCl4、CS2 等互溶,据此可判断 LC2I2是________ (填“极性”或“非极性”)分子。
(5)在①苯、②CH3OH、③CS2、④C2H4、⑤CCl4五种物质中,碳原子采取sp2杂化的分子有________ (填序号)。
(6)元素N可以形成分子式为Co(NH3)5BrSO4,配位数均为6的两种配合物,若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为_______________ 。

试回答下列问题:
(1)请写出元素M的基态原子的价电子排布式:
(2)标准状况下,11.2L AC2含有π键的数目为
(3)E、F、G的第一电离能由大到小的顺序为:
(4)LC2I2常温下为深红色液体,能与 CCl4、CS2 等互溶,据此可判断 LC2I2是
(5)在①苯、②CH3OH、③CS2、④C2H4、⑤CCl4五种物质中,碳原子采取sp2杂化的分子有
(6)元素N可以形成分子式为Co(NH3)5BrSO4,配位数均为6的两种配合物,若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为
您最近半年使用:0次



