16. I:汽车尾气中含有较多的氮氧化物和不完全燃烧的CO, 汽车三元催化器可以实现降低氮氧化物的排放量。汽车尾气中的NO(g)和CO(g)在催化剂的作用下转化成两种无污染的气体。如:反应I:2CO +2NO
⇌N
2+2CO
2 △
H1;反应II:4CO+2NO
2⇌N
2+4CO
2 △
H2<0。
(1)已知:反应N(g)+O
2(g)=2NO(g)△
H3=+180.0 kJ/mol, 若CO的燃烧热△
H为-283.5 kJ/mol,则反应I的△
H1=
_____________________。
(2)若在恒容的密闭容器中,充入2 mol CO和l mol NO,发生反应I,下列选项中不能说明该反应已经达到平衡状态的是
_________________。
A.N
2和CO
2的物质的量之比不变 B.混合气体的密度保持不变
C.混合气体的压强保持不变
D.2v (N
2) =v (CO)
E.混合气体的平均相对分子质量保持不变
(3)在2 L密闭容器中充入2 mol CO和1 mol NO
2, 发生上述反应II。
①若在某温度下,该反应达平衡时CO的转化率为50%,则该反应的平衡常数为
___________。
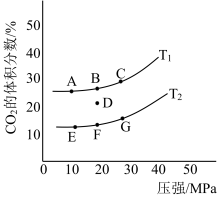
②如图为平衡时CO
2的体积分数与温度、压强的关系。则温度:T
1__T
2(填“<"或">");若在D点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中A~G点中的
______点。
II:CH
4和CO
2都是比较稳定的分子,科学家利用电解装置实现两种分子的耦合转化,其原理如图所示:
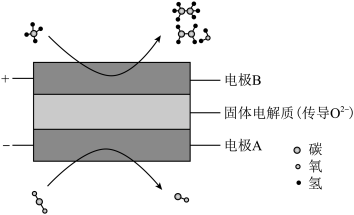
(4)阴极上的反应式为
_______________。
(5)若阳极生成的乙烯和乙烷的体积比为1:1,则两电极消耗的CH
4和CO
2体积比为
____________ (气体体积在相同条件下测定)。