17. 钒(
23V)是我国的丰产元素,广泛应用于催化及钢铁工业,有“化学面包”、金属“维生素”之称。回答下列问题:
(1)钒原子的核外电子排布式为
________________,在元素周期表中的位置为
______。
(2)V
2O
5常用作SO
2转化为SO
3的催化剂。基态S原子电子占据最高能级的电子云轮廓为
________形;气态SO
3以单分子形式存在,其分子的立体构型为
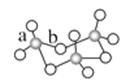
_______形;固体SO
3的三聚体环状结构如图所示,该结构中S—O键长有a、b两类,b的键长大于a的键长的原因为
______________。
(3)V
2O
5溶解在NaOH溶液中,可得到钒酸钠(Na
3VO
4),该盐阴离子中V的杂化轨道类型为
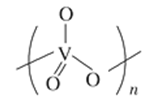
___________;也可得到偏钒酸钠,其阴离子呈如图所示的无限链状结构,则偏钒酸钠的化学式为
_____________。
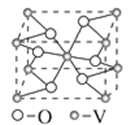
(4)钒的某种氧化物晶胞结构如图所示。该氧化物的化学式为
__________,若它的晶胞参数为x nm,则晶胞的密度为
__________ g/cm
3。