某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度。
(1)用___ 式滴定管盛装cmol/L盐酸标准液。配制c mol/L盐酸标准液,必须使用的主要容器是___ 。如图表示某次滴定时50mL滴定管中前后液面的位置。滴定管读数时应注意___ 。用去的标准盐酸的体积是___ mL。

(2)该实验应选用__ (填“酚酞”或者“石蕊”)作指示剂;操作中如何确定终点?__ 。
(3)对下列两种假定情况进行讨论:(填“无影响”、“偏高”、“偏低”)
a.若滴定前用蒸馏水冲洗锥形瓶,则会使测定结果___ ;
b.若在滴定过程中不慎将数滴酸液滴在锥形瓶外,则会使测定结果___ ;
C,读数时,若滴定前仰视,滴定后俯视,则会使最终测定结果___ 。
(1)用

(2)该实验应选用
(3)对下列两种假定情况进行讨论:(填“无影响”、“偏高”、“偏低”)
a.若滴定前用蒸馏水冲洗锥形瓶,则会使测定结果
b.若在滴定过程中不慎将数滴酸液滴在锥形瓶外,则会使测定结果
C,读数时,若滴定前仰视,滴定后俯视,则会使最终测定结果
更新时间:2019-12-24 13:02:05
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】用盐酸滴定氨水(氯化铵溶液显酸性),选什么作指示剂?怎样描述滴定终点___________ ?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】用标准氢氧化钠溶液(浓度为0.2812mol/L)测定未知浓度的盐酸溶液。
(1)写出化学方程式:____________
(2)滴定时可用_________ 作指示剂,当溶液由___ 色变成___ 色,且0.5min不褪时达到滴定终点。
(3)取20.00mL待测盐酸溶液,滴定终点时,消耗标准氢氧化钠30.00mL,待测盐酸溶液的浓度为________
(1)写出化学方程式:
(2)滴定时可用
(3)取20.00mL待测盐酸溶液,滴定终点时,消耗标准氢氧化钠30.00mL,待测盐酸溶液的浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】请回答有关滴定过程中的相关问题。
(1)用已知浓度的氢氧化钠溶液滴定未知浓度的盐酸,滴定曲线如图所示。

①在图中A的pH范围使用的指示剂是______ ;C的pH范围使用的指示剂是______ 。
②下列关于上述中和滴定过程中的操作,正确的是______ (填序号)。
A.用碱式滴定管量取已知浓度的烧碱溶液
B.滴定管和锥形瓶都必须用待装液润洗
C.滴定过程中始终注视锥形瓶中溶液颜色变化
D.锥形瓶中的待测液可用量筒量取
(2)如图1表示用相同浓度的NaOH溶液分别滴定浓度相同的3种一元酸,由图可确定酸性最强的是______ 。如图2表示用相同浓度的硝酸银标准溶液分别滴定浓度相同的含Cl-、Br-及I-的混合溶液,由图可确定首先沉淀的是 ______ 。

(1)用已知浓度的氢氧化钠溶液滴定未知浓度的盐酸,滴定曲线如图所示。

①在图中A的pH范围使用的指示剂是
②下列关于上述中和滴定过程中的操作,正确的是
A.用碱式滴定管量取已知浓度的烧碱溶液
B.滴定管和锥形瓶都必须用待装液润洗
C.滴定过程中始终注视锥形瓶中溶液颜色变化
D.锥形瓶中的待测液可用量筒量取
(2)如图1表示用相同浓度的NaOH溶液分别滴定浓度相同的3种一元酸,由图可确定酸性最强的是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】判断正误
1.滴定终点就是酸碱恰好中和的点。(_______)
2.滴定管盛标准溶液时,调液面一定要调到“0”刻度。(_______)
3.KMnO4溶液应用碱式滴定管盛装 。(_______)
4.用碱式滴定管准确量取20.00 mL的NaOH溶液。(_______)
5.将液面在0 mL处的25 mL的酸式滴定管中的液体全部放出,液体的体积为25 mL。(_______)
6.中和滴定操作中所需标准溶液越浓越好,指示剂一般加入2~3 mL。(_______)
7.中和滴定实验时,滴定管、锥形瓶均用待测液润洗。(_______)
8.用标准HCl溶液滴定NaHCO3溶液来测定其浓度,选择酚酞为指示剂。(_______)
9.滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁 。(_______)
10.用稀NaOH滴定盐酸,用酚酞作指示剂,当锥形瓶中溶液由红色变无色时停止滴定 。(_______)
11.25 ℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<VNaOH。(_______)
12.等体积、等物质的量浓度的盐酸和醋酸分别与NaOH溶液反应,得到pH=7的溶液所消耗的n(NaOH)相等。(_______)
13.用NaOH溶液滴定白醋,使用酚酞作指示剂,溶液颜色恰好由无色变为浅红色,且半分钟内不褪色时为滴定终点。(_______)
1.滴定终点就是酸碱恰好中和的点。(_______)
2.滴定管盛标准溶液时,调液面一定要调到“0”刻度。(_______)
3.KMnO4溶液应用碱式滴定管盛装 。(_______)
4.用碱式滴定管准确量取20.00 mL的NaOH溶液。(_______)
5.将液面在0 mL处的25 mL的酸式滴定管中的液体全部放出,液体的体积为25 mL。(_______)
6.中和滴定操作中所需标准溶液越浓越好,指示剂一般加入2~3 mL。(_______)
7.中和滴定实验时,滴定管、锥形瓶均用待测液润洗。(_______)
8.用标准HCl溶液滴定NaHCO3溶液来测定其浓度,选择酚酞为指示剂。(_______)
9.滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁 。(_______)
10.用稀NaOH滴定盐酸,用酚酞作指示剂,当锥形瓶中溶液由红色变无色时停止滴定 。(_______)
11.25 ℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<VNaOH。(_______)
12.等体积、等物质的量浓度的盐酸和醋酸分别与NaOH溶液反应,得到pH=7的溶液所消耗的n(NaOH)相等。(_______)
13.用NaOH溶液滴定白醋,使用酚酞作指示剂,溶液颜色恰好由无色变为浅红色,且半分钟内不褪色时为滴定终点。(_______)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用盐酸滴定氨水(氯化铵溶液显酸性),选什么作指示剂?怎样描述滴定终点___________ ?
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】用0.1000 mol/L的Na2S2O3溶液滴定碘水中的碘,从而测定I2的物质的量浓度,已知:I2+2Na2S2O3=2NaI+Na2S4O6
(1)准确量取10.00 mL碘水置于锥形瓶中,加入2滴________ 作指示剂。
(2)确定滴定终点的现象为____________________ 。
(3)当消耗Na2S2O3溶液20 .00 mL时达到目的终点,则碘水中碘的c(I2)=________ 。
(4)下列操作会引起实验结果偏高的是________ 。
A.量取Na2S2O3溶液滴定管用蒸馏水洗干净后,立即注入Na2S2O3溶液
B.锥形瓶用蒸馏水洗干净后直接装入碘水
C.碘水变色后立即读取消耗Na2S2O3溶液的体积
(5)氢氧化铜Ksp=2×10-20,它的悬浊液中存在如下平衡:Cu(OH)2(s) Cu2+(aq)+2OH-(aq),某硫酸铜溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH使之大于
Cu2+(aq)+2OH-(aq),某硫酸铜溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH使之大于_________ 。
(1)准确量取10.00 mL碘水置于锥形瓶中,加入2滴
(2)确定滴定终点的现象为
(3)当消耗Na2S2O3溶液20 .00 mL时达到目的终点,则碘水中碘的c(I2)=
(4)下列操作会引起实验结果偏高的是
A.量取Na2S2O3溶液滴定管用蒸馏水洗干净后,立即注入Na2S2O3溶液
B.锥形瓶用蒸馏水洗干净后直接装入碘水
C.碘水变色后立即读取消耗Na2S2O3溶液的体积
(5)氢氧化铜Ksp=2×10-20,它的悬浊液中存在如下平衡:Cu(OH)2(s)
 Cu2+(aq)+2OH-(aq),某硫酸铜溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH使之大于
Cu2+(aq)+2OH-(aq),某硫酸铜溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH使之大于
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:
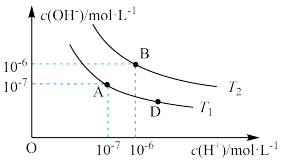
(1)A点水的离子积为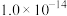 ,B点水的离子积为
,B点水的离子积为_______ 。造成水的离子积变化的原因是_______ 。
(2)下列说法正确的是_______ (填字母)。
a.图中A、B、D三点处Kw的大小关系:B>A>D
b.AB线上任意点的溶液均显中性
c.B点溶液的pH=6,显酸性
d.图中温度T1>T2
(3)某校学生用中和滴定法测定某NaOH溶液的物质的量浓度,选酚酞作指示剂。
①盛装0.2000 mol/L盐酸标准液应该用_______ 式滴定管。
②终点判断方法:_______ 。
③有关数据记录如下:
实验序号待测液体积(mL)所消耗盐酸标准液的体积(mL)
则NaOH溶液的物质的量浓度为_______ mol/L。(保留四位有效数字)
④若滴定时锥形瓶未干燥,则测定结果_______ ;(填“无影响”、“偏高”或“偏低”)。

(1)A点水的离子积为
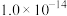 ,B点水的离子积为
,B点水的离子积为(2)下列说法正确的是
a.图中A、B、D三点处Kw的大小关系:B>A>D
b.AB线上任意点的溶液均显中性
c.B点溶液的pH=6,显酸性
d.图中温度T1>T2
(3)某校学生用中和滴定法测定某NaOH溶液的物质的量浓度,选酚酞作指示剂。
①盛装0.2000 mol/L盐酸标准液应该用
②终点判断方法:
③有关数据记录如下:
实验序号待测液体积(mL)所消耗盐酸标准液的体积(mL)
| 实验序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.60 | 20.70 |
| 2 | 20.00 | 6.00 | 25.90 |
| 3 | 20.00 | 0.40 | 23.20 |
则NaOH溶液的物质的量浓度为
④若滴定时锥形瓶未干燥,则测定结果
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】滴定是一种重要的定量实验方法:
I. 常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如下图所示:

(1)滴定盐酸的曲线是图__________ (填“1”或“2”)。
(2)滴定前CH3COOH的电离度为__________ (电离度= ×100%)。
×100%)。
(3)达到B、D状态时,反应消耗的NaOH溶液的体积a__________ b(填“>”“<”或“=”);若图中E点pH=8,则c(Na+)-c(CH3COO-)的精确值为__________ mol/L。
Ⅱ. 现使用酸碱中和滴定法测定市售白醋中醋酸的浓度
(1)实验步骤:
①量取10.00 mL市售白醋,在烧杯中用水稀释后转移到100 mL容量瓶中定容,摇匀得待测白醋溶液。
②用酸式滴定管取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴酚酞作指示剂。
③读取盛装0.1000 mol/L NaOH 溶液的碱式滴定管的初始读数。
④滴定。当___________________ 时,停止滴定,并记录NaOH溶液的最终读数。
⑤重复②、③、④步骤3次。
数据记录如下:
(2)数据处理:
根据实验数据计算,可得市售白醋中醋酸的浓度为_________ mol/L
(3)误差分析:在本实验的滴定过程中,下列操作会使实验结果偏大的是_________ 。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后消失
c.锥形瓶中加入待测白醋溶液后,再加入少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
e.滴定前平视读数,滴定后俯视读数
I. 常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如下图所示:

(1)滴定盐酸的曲线是图
(2)滴定前CH3COOH的电离度为
 ×100%)。
×100%)。(3)达到B、D状态时,反应消耗的NaOH溶液的体积a
Ⅱ. 现使用酸碱中和滴定法测定市售白醋中醋酸的浓度
(1)实验步骤:
①量取10.00 mL市售白醋,在烧杯中用水稀释后转移到100 mL容量瓶中定容,摇匀得待测白醋溶液。
②用酸式滴定管取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴酚酞作指示剂。
③读取盛装0.1000 mol/L NaOH 溶液的碱式滴定管的初始读数。
④滴定。当
⑤重复②、③、④步骤3次。
数据记录如下:
| 滴定次数 实验数据(mL) | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
(2)数据处理:
根据实验数据计算,可得市售白醋中醋酸的浓度为
(3)误差分析:在本实验的滴定过程中,下列操作会使实验结果偏大的是
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后消失
c.锥形瓶中加入待测白醋溶液后,再加入少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
e.滴定前平视读数,滴定后俯视读数
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂。请填写下列空白:
(1)终点的判断:溶液由_______ 。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是( )
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为_______ mL。
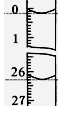
(4)某学生根据3次实验分别记录有关数据如表:
②依据上表数据列式计算该NaOH溶液的物质的量浓度_______ (计算结果取4位有效数)。
(1)终点的判断:溶液由
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为

(4)某学生根据3次实验分别记录有关数据如表:
| 滴定 次数 | 待测NaOH溶液的体积/mL | 0.1000 mol/L盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 平均耗用盐酸 体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.15 | ①V= |
| 第二次 | 25.00 | 0.56 | 30.30 | |
| 第三次 | 25.00 | 0.20 | 26.45 | |
②依据上表数据列式计算该NaOH溶液的物质的量浓度
您最近一年使用:0次



