用0.1000 mol/L的Na2S2O3溶液滴定碘水中的碘,从而测定I2的物质的量浓度,已知:I2+2Na2S2O3=2NaI+Na2S4O6
(1)准确量取10.00 mL碘水置于锥形瓶中,加入2滴________ 作指示剂。
(2)确定滴定终点的现象为____________________ 。
(3)当消耗Na2S2O3溶液20 .00 mL时达到目的终点,则碘水中碘的c(I2)=________ 。
(4)下列操作会引起实验结果偏高的是________ 。
A.量取Na2S2O3溶液滴定管用蒸馏水洗干净后,立即注入Na2S2O3溶液
B.锥形瓶用蒸馏水洗干净后直接装入碘水
C.碘水变色后立即读取消耗Na2S2O3溶液的体积
(5)氢氧化铜Ksp=2×10-20,它的悬浊液中存在如下平衡:Cu(OH)2(s) Cu2+(aq)+2OH-(aq),某硫酸铜溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH使之大于
Cu2+(aq)+2OH-(aq),某硫酸铜溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH使之大于_________ 。
(1)准确量取10.00 mL碘水置于锥形瓶中,加入2滴
(2)确定滴定终点的现象为
(3)当消耗Na2S2O3溶液20 .00 mL时达到目的终点,则碘水中碘的c(I2)=
(4)下列操作会引起实验结果偏高的是
A.量取Na2S2O3溶液滴定管用蒸馏水洗干净后,立即注入Na2S2O3溶液
B.锥形瓶用蒸馏水洗干净后直接装入碘水
C.碘水变色后立即读取消耗Na2S2O3溶液的体积
(5)氢氧化铜Ksp=2×10-20,它的悬浊液中存在如下平衡:Cu(OH)2(s)
 Cu2+(aq)+2OH-(aq),某硫酸铜溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH使之大于
Cu2+(aq)+2OH-(aq),某硫酸铜溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH使之大于
更新时间:2022-12-02 18:48:25
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】为测定某盐酸的物质的量浓度,某学生在中和滴定的实验中,用已知物质的量浓度的NaOH溶液进行滴定,其实验过程如下:
A.取一支有玻璃活塞的滴定管,用蒸馏水洗净,再用已知物质的量浓度的NaOH溶液润洗,然后装入已知物质的量浓度的NaOH溶液
B.调节好液面后,记下液面刻度读数;
C.取一支10m规格的移液管,用蒸馏水洗涤干净后,取出10mL待测盐酸溶液,置于未经待测盐酸润洗的洁净锥形瓶中;
D.加入酚酞试液10滴(酚酞有弱酸性),摇匀;
E.滴定时边滴加边轻轻摇匀,眼睛始终注视着锥形瓶中溶液颜色的变化;
F.当锥形瓶中溶液由无色变成粉红色时,滴定达到终点,立即停止滴定;
G.再重复滴定两次;
H.根据三次滴定消耗的NaOH溶液体积的平均值进行计算。
(1)该学生在实验过程中的错误操作有________ (填字母,下同)。
(2)以上错误操作中,使测定结果一定偏高的是________ ,一定偏低的是________ 。
A.取一支有玻璃活塞的滴定管,用蒸馏水洗净,再用已知物质的量浓度的NaOH溶液润洗,然后装入已知物质的量浓度的NaOH溶液
B.调节好液面后,记下液面刻度读数;
C.取一支10m规格的移液管,用蒸馏水洗涤干净后,取出10mL待测盐酸溶液,置于未经待测盐酸润洗的洁净锥形瓶中;
D.加入酚酞试液10滴(酚酞有弱酸性),摇匀;
E.滴定时边滴加边轻轻摇匀,眼睛始终注视着锥形瓶中溶液颜色的变化;
F.当锥形瓶中溶液由无色变成粉红色时,滴定达到终点,立即停止滴定;
G.再重复滴定两次;
H.根据三次滴定消耗的NaOH溶液体积的平均值进行计算。
(1)该学生在实验过程中的错误操作有
(2)以上错误操作中,使测定结果一定偏高的是
您最近一年使用:0次
【推荐2】实验室常用邻苯二甲酸氢钾(KHC8H4O4)来测定氢氧化钠溶液的浓度,反应如下:KHC8H4O4+NaOH=KNaC8H4O4+H2O。若氢氧化钠溶液的浓度为0.1mol·L-1,到达终点时,溶液的pH约为9.1。
(1)在测定氢氧化钠溶液浓度时,有下列操作:①向溶液中加入1-2滴指示剂②向锥形瓶中加20-30mL蒸馏水溶解③用氢氧化钠溶液滴定到终点,半分钟不褪色④重复以上操作⑤准确称取0.4-0.5g邻苯二甲酸氢钾加入250mL锥形瓶中⑥根据两次实验数据计算氢氧化钠的物质的量浓度。
以上各步中,正确的(填序号)操作顺序是___ 。
(2)该实验应选用___ 作指示剂,达到滴定终点时溶液由___ 色变为___ 色。
(3)上述操作中,将邻苯二甲酸氢钾直接放到锥形瓶中溶解,对实验是否有影响?___ ,并说明理由:___ 。
(4)滴定前,用蒸馏水洗净碱式滴定管,然后加待测定的氢氧化钠溶液滴定,此操作将造成实验结果___ (填“偏大”“偏小”或“无影响”)
(5)现准确称取KHC8H4O4(分子量204.2)晶体0.5105g,溶于水后加入指示剂,用NaOH溶液滴定至终点,消耗NaOH20.00mL,则NaOH溶液的浓度为___ (结果保留四位有效数字)。
(1)在测定氢氧化钠溶液浓度时,有下列操作:①向溶液中加入1-2滴指示剂②向锥形瓶中加20-30mL蒸馏水溶解③用氢氧化钠溶液滴定到终点,半分钟不褪色④重复以上操作⑤准确称取0.4-0.5g邻苯二甲酸氢钾加入250mL锥形瓶中⑥根据两次实验数据计算氢氧化钠的物质的量浓度。
以上各步中,正确的(填序号)操作顺序是
(2)该实验应选用
(3)上述操作中,将邻苯二甲酸氢钾直接放到锥形瓶中溶解,对实验是否有影响?
(4)滴定前,用蒸馏水洗净碱式滴定管,然后加待测定的氢氧化钠溶液滴定,此操作将造成实验结果
(5)现准确称取KHC8H4O4(分子量204.2)晶体0.5105g,溶于水后加入指示剂,用NaOH溶液滴定至终点,消耗NaOH20.00mL,则NaOH溶液的浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现使用酸碱中和滴定法测定某盐酸的浓度。
Ⅰ.实验步骤
(1)如图,用___________ (填“甲”或“乙”)量取待测盐酸溶液20.00mL于锥形瓶中,向其中滴加2滴___________ 作指示剂。

(2)读取盛装0.1000 NaOH溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为
NaOH溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为___________ mL。
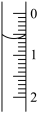
(3)滴定。左手___________ ,右手___________ ,眼睛___________ 。当___________ 时,停止滴定,并记录NaOH溶液的最终读数。重复滴定3次。
Ⅱ.实验记录
Ⅲ.数据处理与讨论
(4)根据图表数据平均消耗的NaOH溶液的体积V=___________ mL,数据处理,可得
___________ 
(5)在本实验的滴定过程中,下列操作会使实验结果偏高的是___________(填字母)。
Ⅰ.实验步骤
(1)如图,用

(2)读取盛装0.1000
 NaOH溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为
NaOH溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为
(3)滴定。左手
Ⅱ.实验记录
| 滴定次数 | 1 | 2 | 3 | 4 |
| V(样品)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
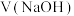 /mL /mL | 15.95 | 15.00 | 15.05 | 14.95 |
(4)根据图表数据平均消耗的NaOH溶液的体积V=


(5)在本实验的滴定过程中,下列操作会使实验结果偏高的是___________(填字母)。
| A.碱式滴定管在滴定时未用NaOH标准溶液润洗 |
| B.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失 |
| C.锥形瓶中加入待测盐酸溶液后,再加少量水 |
| D.锥形瓶在滴定时剧烈摇动,有少量液体溅出 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氧化还原滴定实验的原理与中和滴定相同(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现有0.001mol•L-1酸性KMnO4溶液和未知浓度的无色NaHSO3溶液,有关反应的离子方程式是2 +5
+5 +H+=2Mn2++5
+H+=2Mn2++5 +3H2O。请回答下列问题:
+3H2O。请回答下列问题:
(1)不用碱式滴定管盛放酸性KMnO4溶液的原因是______ 。
(2)______ (填“需要”或“不需要”)选用指示剂,其理由是______ 。
(3)滴定前平视酸性KMnO4溶液液面,刻度为amL,滴定后俯视液面,刻度为bmL,则(b-a)mL比实际消耗酸性KMnO4溶液的体积______ (填“大”或“小”,下同);根据(b-a)mL计算得到的待测液浓度比实际浓度_____ 。
 +5
+5 +H+=2Mn2++5
+H+=2Mn2++5 +3H2O。请回答下列问题:
+3H2O。请回答下列问题:(1)不用碱式滴定管盛放酸性KMnO4溶液的原因是
(2)
(3)滴定前平视酸性KMnO4溶液液面,刻度为amL,滴定后俯视液面,刻度为bmL,则(b-a)mL比实际消耗酸性KMnO4溶液的体积
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】准确称取上述流程中的产品重铬酸钠晶体(Na2Cr2O7·2H2O)3.1700 g配成250 mL溶液,取出25.00 mL放于锥形瓶中,加入10 mL 2 mol·L-1H2SO4溶液和足量碘化钾溶液,放于暗处5 min;然后加入100 mL水和2-3滴淀粉指示剂;最后根据I2+2S2O =2I-+S4O
=2I-+S4O 用0.1000 mol·L-1Na2S2O3标准溶液滴定,判断达到滴定终点的依据是:
用0.1000 mol·L-1Na2S2O3标准溶液滴定,判断达到滴定终点的依据是:___________ 。
 =2I-+S4O
=2I-+S4O 用0.1000 mol·L-1Na2S2O3标准溶液滴定,判断达到滴定终点的依据是:
用0.1000 mol·L-1Na2S2O3标准溶液滴定,判断达到滴定终点的依据是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作:
A.在250mL容量瓶中配制250mL烧碱溶液
B.用移液管(或碱式滴定管)量取25.00mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂
C.在天平上准确称取烧碱样品wg,在烧杯中加蒸馏水溶解
D.将物质的量浓度为mmol/L的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度V1mL
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2mL
请完成下列问题:
(1)正确的操作步骤是(填写字母)______→______→_____→D→_____;___________
(2)若用标准浓度的H2SO4溶液测定NaOH溶液的浓度,参看图示从下表中选出正确选项_____。

(3)操作D中液面应调整到___________ ,尖嘴部分应___________ ;
(4)滴定终点时的颜色变化是___________ ;
(5)若酸式滴定管没用标准H2SO4润洗,会对测定结果有何影响___________ (填“偏高”、“偏低”或“无影响”,其他操作均正确);
(6)该烧碱样品的纯度计算式是___________ 。
A.在250mL容量瓶中配制250mL烧碱溶液
B.用移液管(或碱式滴定管)量取25.00mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂
C.在天平上准确称取烧碱样品wg,在烧杯中加蒸馏水溶解
D.将物质的量浓度为mmol/L的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度V1mL
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2mL
请完成下列问题:
(1)正确的操作步骤是(填写字母)______→______→_____→D→_____;
(2)若用标准浓度的H2SO4溶液测定NaOH溶液的浓度,参看图示从下表中选出正确选项_____。

| 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 | |
| A | 碱 | 酸 | 石蕊 | 乙 |
| B | 酸 | 碱 | 酚酞 | 甲 |
| C | 碱 | 酸 | 甲基橙 | 甲 |
| D | 酸 | 碱 | 石蕊 | 乙 |
| A.A | B.B | C.C | D.D |
(3)操作D中液面应调整到
(4)滴定终点时的颜色变化是
(5)若酸式滴定管没用标准H2SO4润洗,会对测定结果有何影响
(6)该烧碱样品的纯度计算式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:
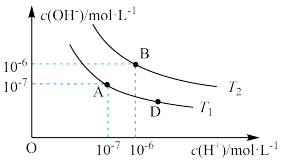
(1)A点水的离子积为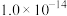 ,B点水的离子积为
,B点水的离子积为_______ 。造成水的离子积变化的原因是_______ 。
(2)下列说法正确的是_______ (填字母)。
a.图中A、B、D三点处Kw的大小关系:B>A>D
b.AB线上任意点的溶液均显中性
c.B点溶液的pH=6,显酸性
d.图中温度T1>T2
(3)某校学生用中和滴定法测定某NaOH溶液的物质的量浓度,选酚酞作指示剂。
①盛装0.2000 mol/L盐酸标准液应该用_______ 式滴定管。
②终点判断方法:_______ 。
③有关数据记录如下:
实验序号待测液体积(mL)所消耗盐酸标准液的体积(mL)
则NaOH溶液的物质的量浓度为_______ mol/L。(保留四位有效数字)
④若滴定时锥形瓶未干燥,则测定结果_______ ;(填“无影响”、“偏高”或“偏低”)。

(1)A点水的离子积为
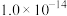 ,B点水的离子积为
,B点水的离子积为(2)下列说法正确的是
a.图中A、B、D三点处Kw的大小关系:B>A>D
b.AB线上任意点的溶液均显中性
c.B点溶液的pH=6,显酸性
d.图中温度T1>T2
(3)某校学生用中和滴定法测定某NaOH溶液的物质的量浓度,选酚酞作指示剂。
①盛装0.2000 mol/L盐酸标准液应该用
②终点判断方法:
③有关数据记录如下:
实验序号待测液体积(mL)所消耗盐酸标准液的体积(mL)
| 实验序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.60 | 20.70 |
| 2 | 20.00 | 6.00 | 25.90 |
| 3 | 20.00 | 0.40 | 23.20 |
则NaOH溶液的物质的量浓度为
④若滴定时锥形瓶未干燥,则测定结果
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】滴定法是重要的化学定量分析方法。国家标准规定,酿造的食醋中醋酸的含量不得低于 ,即每
,即每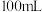 食醋中,折算成的醋酸含量不得低于
食醋中,折算成的醋酸含量不得低于 。某实验小组用酸碱滴定法测定某食用白醋的总酸含量(
。某实验小组用酸碱滴定法测定某食用白醋的总酸含量( ),回答下列问题:
),回答下列问题:
(1)下列仪器,在使用前需要润洗的是___________ 。
A.容量瓶 B.锥形瓶 C.碱性滴定管
(2)准备与滴定
a.待测液的准备:将 食用白醋稀释至
食用白醋稀释至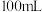 ,用
,用___________ (填仪器名称)量取稀释后的溶液 于锥形瓶中;
于锥形瓶中;
b.标准溶液的准备:用碱式滴定管盛装 标准溶液;
标准溶液;
c.滴定:向盛有白醋样品的锥形瓶中加入2滴酚酞作为指示剂,把锥形瓶放在碱式滴定管的下方,瓶下垫一张白纸,小心地滴入碱。边滴边摇动锥形瓶(接近终点时,改为滴加半滴碱),直到因加入半滴碱后,溶液颜色从________________ 。表示已经到达滴定终点。
d.重复上述操作三次。四次测定数据如表:
(3)数据处理与计算
①所消耗 溶液的平均体积为
溶液的平均体积为______________  。
。
②计算得出白醋的总酸量为______________  。(保留小数点后一位)
。(保留小数点后一位)
(4)分析:
①常温下,若取等体积的 溶液和
溶液和 溶液混合均匀,测定混合液的
溶液混合均匀,测定混合液的 ,若
,若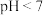 ,可证明:
,可证明:_______________________________
② 溶液滴定过程,如用甲基橙做指示剂,到达滴定终点时,所用NaOH溶液体积
溶液滴定过程,如用甲基橙做指示剂,到达滴定终点时,所用NaOH溶液体积______________ (填写“偏多”“不变”“偏少”);碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失,则测定白醋的总酸量比理论值______________ (填“偏大”“不变”“偏小”)
 ,即每
,即每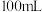 食醋中,折算成的醋酸含量不得低于
食醋中,折算成的醋酸含量不得低于 。某实验小组用酸碱滴定法测定某食用白醋的总酸含量(
。某实验小组用酸碱滴定法测定某食用白醋的总酸含量( ),回答下列问题:
),回答下列问题:(1)下列仪器,在使用前需要润洗的是
A.容量瓶 B.锥形瓶 C.碱性滴定管
(2)准备与滴定
a.待测液的准备:将
 食用白醋稀释至
食用白醋稀释至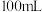 ,用
,用 于锥形瓶中;
于锥形瓶中;b.标准溶液的准备:用碱式滴定管盛装
 标准溶液;
标准溶液;c.滴定:向盛有白醋样品的锥形瓶中加入2滴酚酞作为指示剂,把锥形瓶放在碱式滴定管的下方,瓶下垫一张白纸,小心地滴入碱。边滴边摇动锥形瓶(接近终点时,改为滴加半滴碱),直到因加入半滴碱后,溶液颜色从
d.重复上述操作三次。四次测定数据如表:
| 序号 | 1 | 2 | 3 | 4 |
标准溶液体积 | 20.05 | 20.00 | 8.40 | 19.95 |
①所消耗
 溶液的平均体积为
溶液的平均体积为 。
。②计算得出白醋的总酸量为
 。(保留小数点后一位)
。(保留小数点后一位)(4)分析:
①常温下,若取等体积的
 溶液和
溶液和 溶液混合均匀,测定混合液的
溶液混合均匀,测定混合液的 ,若
,若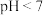 ,可证明:
,可证明:②
 溶液滴定过程,如用甲基橙做指示剂,到达滴定终点时,所用NaOH溶液体积
溶液滴定过程,如用甲基橙做指示剂,到达滴定终点时,所用NaOH溶液体积
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I、某学生用已知物质的量浓度的硫酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂。回答下列问题:
(1)用标准的硫酸滴定待测的NaOH溶液时,终点现象是___________ 。
(2)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用硫酸溶液的体积为___________ mL。

(3)某学生根据3次实验分别记录有关数据如表:
依据上表数据计算可得该NaOH溶液的物质的量浓度为___________ mol·L-1(保留四位有效数字)。
(4)下列操作中可能使所测NaOH溶液的浓度数值偏低的是___________(填字母)。
II、某实验小组用0.50mol/LNaOH溶液和0.50mol/L硫酸溶液进行中和热的测定。实验装置如图所示。
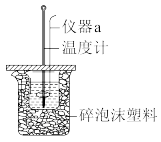
(5)仪器a的名称是___________ 。
(6)取50mLNaOH溶液和30mL硫酸溶液进行实验,测得起止温度差的平均值为4.0°C.近似认为0.50mol/LNaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g·°C)。则计算得中和热△H=___________ (取小数点后一位)。
(7)上述实验结果与-57.3kJ/mol有偏差,产生偏差的原因可能是___________ (填字母)。
a.实验装置保温、隔热效果差
b.用量筒量取NaOH溶液的体积时仰视刻度线读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(1)用标准的硫酸滴定待测的NaOH溶液时,终点现象是
(2)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用硫酸溶液的体积为

(3)某学生根据3次实验分别记录有关数据如表:
| 滴定次数 | 待测NaOH溶液的体积/mL | 0.1000mol·L-1硫酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
(4)下列操作中可能使所测NaOH溶液的浓度数值偏低的是___________(填字母)。
| A.酸式滴定管未用标准硫酸润洗就直接注入标准硫酸 |
| B.读取硫酸体积时,开始仰视读数,滴定结束时俯视读数 |
| C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.锥形瓶用水洗涤后,用待测液润洗 |
II、某实验小组用0.50mol/LNaOH溶液和0.50mol/L硫酸溶液进行中和热的测定。实验装置如图所示。

(5)仪器a的名称是
(6)取50mLNaOH溶液和30mL硫酸溶液进行实验,测得起止温度差的平均值为4.0°C.近似认为0.50mol/LNaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g·°C)。则计算得中和热△H=
(7)上述实验结果与-57.3kJ/mol有偏差,产生偏差的原因可能是
a.实验装置保温、隔热效果差
b.用量筒量取NaOH溶液的体积时仰视刻度线读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】依据水溶液中的离子平衡规律,回答下列问题:
(1)除去酸性 溶液中的
溶液中的 ,可加入
,可加入___________ 物质(至少回答两种),可以使 转化为
转化为 而除去。
而除去。
(2) 时,若体积为
时,若体积为 的某一元强酸与体积为
的某一元强酸与体积为 的某一元强碱混合,恰好中和,且已知
的某一元强碱混合,恰好中和,且已知 和
和 ,则a的取值范围是
,则a的取值范围是___________ 。
(3)工业上用化学法除锅炉的水垢时,先向锅炉中注入饱和 溶液浸泡,将水垢中的
溶液浸泡,将水垢中的 转化为
转化为 ,再用盐酸除去[已知:
,再用盐酸除去[已知: ]。
]。
①沉淀转化的离子方程式为___________ 。
②该温度下,根据 ,计算
,计算 在水中的溶解度的为
在水中的溶解度的为___________ g。
(4)在化学分析中,以 标准溶液滴定溶液中的
标准溶液滴定溶液中的 时,采用
时,采用 为指示剂,利用
为指示剂,利用 与
与 反应生成砖红色沉淀指示滴定终点。当溶液中
反应生成砖红色沉淀指示滴定终点。当溶液中 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 )时,溶液中:
)时,溶液中: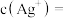
___________  ,
,
___________  。(已知
。(已知 时
时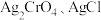 的
的 分别为
分别为 和
和 )
)
(1)除去酸性
 溶液中的
溶液中的 ,可加入
,可加入 转化为
转化为 而除去。
而除去。(2)
 时,若体积为
时,若体积为 的某一元强酸与体积为
的某一元强酸与体积为 的某一元强碱混合,恰好中和,且已知
的某一元强碱混合,恰好中和,且已知 和
和 ,则a的取值范围是
,则a的取值范围是(3)工业上用化学法除锅炉的水垢时,先向锅炉中注入饱和
 溶液浸泡,将水垢中的
溶液浸泡,将水垢中的 转化为
转化为 ,再用盐酸除去[已知:
,再用盐酸除去[已知: ]。
]。①沉淀转化的离子方程式为
②该温度下,根据
 ,计算
,计算 在水中的溶解度的为
在水中的溶解度的为(4)在化学分析中,以
 标准溶液滴定溶液中的
标准溶液滴定溶液中的 时,采用
时,采用 为指示剂,利用
为指示剂,利用 与
与 反应生成砖红色沉淀指示滴定终点。当溶液中
反应生成砖红色沉淀指示滴定终点。当溶液中 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 )时,溶液中:
)时,溶液中: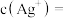
 ,
,
 。(已知
。(已知 时
时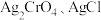 的
的 分别为
分别为 和
和 )
)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。根据要求回答问题
(1)普通泡沫灭火器是利用 溶液跟
溶液跟 溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是
溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是_______ 。
(2)常温下,取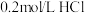 溶液与
溶液与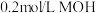 溶液等体积混合,测得混合后溶液的
溶液等体积混合,测得混合后溶液的 。写出MOH的电离方程式:
。写出MOH的电离方程式:_______ 。
(3)往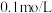 的
的 溶液中滴入紫色石蕊试液,溶液变红。则:
溶液中滴入紫色石蕊试液,溶液变红。则:
①该溶液中
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②得出上述判断的依据是_______ (用文字解释)。
(4)含 的废水毒性较大,某工厂废水中含
的废水毒性较大,某工厂废水中含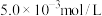 的
的 。为了使废水的排放达标,进行如下处理:
。为了使废水的排放达标,进行如下处理:

①绿矾为 。反应(Ⅰ)中
。反应(Ⅰ)中 与
与 的物质的量之比为
的物质的量之比为_______ 。
②常温下若处理后的废水中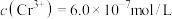 ,则处理后的废水的pH=
,则处理后的废水的pH=_______ 。{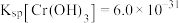 }
}
(1)普通泡沫灭火器是利用
 溶液跟
溶液跟 溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是
溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是(2)常温下,取
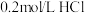 溶液与
溶液与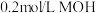 溶液等体积混合,测得混合后溶液的
溶液等体积混合,测得混合后溶液的 。写出MOH的电离方程式:
。写出MOH的电离方程式:(3)往
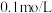 的
的 溶液中滴入紫色石蕊试液,溶液变红。则:
溶液中滴入紫色石蕊试液,溶液变红。则:①该溶液中

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②得出上述判断的依据是
(4)含
 的废水毒性较大,某工厂废水中含
的废水毒性较大,某工厂废水中含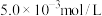 的
的 。为了使废水的排放达标,进行如下处理:
。为了使废水的排放达标,进行如下处理:
①绿矾为
 。反应(Ⅰ)中
。反应(Ⅰ)中 与
与 的物质的量之比为
的物质的量之比为②常温下若处理后的废水中
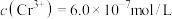 ,则处理后的废水的pH=
,则处理后的废水的pH=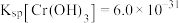 }
}
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】填空。
(1)25℃,在0.10 mol/LH2S溶液中,通入HCl气体成加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图(忽略溶液体积的变化、H2S的挥发)。
①pH=13时,溶液中的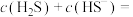
___________ mol/L;
②某溶液含0.020 mol/L Mn2+、0.10mol/LH2S,当溶液pH=___________ 时,Mn2+开始沉淀[已知: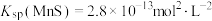 ]。
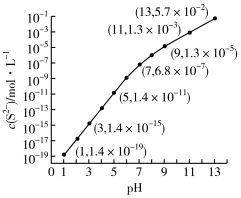
]。
(2)25℃,两种酸的电离平衡常数如下表。
①0.10 mol/LNaHSO3溶液中离子浓度由大到小的顺序为___________ 。
②向NaHCO3溶液中通入少量二氧化硫时反应的离子方程式为___________ 。
(3)银是一种费金属,古代常用于制造钱币及装饰器皿,现代在电池和照明器材等领域亦有广泛应用。已知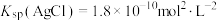 ,若向5 mL0.018 mol/L的AgNO3溶液中加入5 mL0.020 mol/L的盐酸,混合后溶液中的Ag+的浓度为
,若向5 mL0.018 mol/L的AgNO3溶液中加入5 mL0.020 mol/L的盐酸,混合后溶液中的Ag+的浓度为___________ mol/L。
(1)25℃,在0.10 mol/LH2S溶液中,通入HCl气体成加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图(忽略溶液体积的变化、H2S的挥发)。
①pH=13时,溶液中的
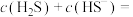
②某溶液含0.020 mol/L Mn2+、0.10mol/LH2S,当溶液pH=
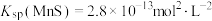 ]。
]。
(2)25℃,两种酸的电离平衡常数如下表。
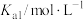 |  | |
| H2SO3 | 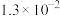 | 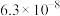 |
| H2CO3 | 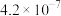 | 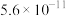 |
①0.10 mol/LNaHSO3溶液中离子浓度由大到小的顺序为
②向NaHCO3溶液中通入少量二氧化硫时反应的离子方程式为
(3)银是一种费金属,古代常用于制造钱币及装饰器皿,现代在电池和照明器材等领域亦有广泛应用。已知
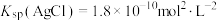 ,若向5 mL0.018 mol/L的AgNO3溶液中加入5 mL0.020 mol/L的盐酸,混合后溶液中的Ag+的浓度为
,若向5 mL0.018 mol/L的AgNO3溶液中加入5 mL0.020 mol/L的盐酸,混合后溶液中的Ag+的浓度为
您最近一年使用:0次



