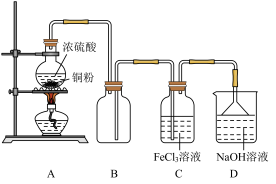
某研究性学习小组用如图装置进行SO2与FeCl3溶液反应的相关实验:
完成下列填空
(1)在配制FeCl3溶液时,需先把FeCl3晶体溶解在________ 中,再加水稀释,才能得到透明澄清溶液。
(2)B装置的作用是__________ ;D装置中吸收尾气的离子方程式是__________ 。
(3)A装置中制备SO2的化学方程式为:_______ ,在该反应中浓硫酸体现的性质是______ 。
(4)当温度较高的SO2气体(足量)通入FeCl3溶液中时,可以观察到溶液由黄色逐渐变为浅绿色。根据此现象,该小组同学认为SO2与FeCl3溶液发生了氧化还原反应。
a.写出SO2与FeCl3溶液反应的离子方程式:___________ 。
b.请设计实验方案检验上述反应中FeCl3是否反应完全:_________________ 。
c.若向得到的浅绿色溶液中逐滴滴加NaOH溶液,可以观察到的现象是:________ 。

完成下列填空
(1)在配制FeCl3溶液时,需先把FeCl3晶体溶解在
(2)B装置的作用是
(3)A装置中制备SO2的化学方程式为:
(4)当温度较高的SO2气体(足量)通入FeCl3溶液中时,可以观察到溶液由黄色逐渐变为浅绿色。根据此现象,该小组同学认为SO2与FeCl3溶液发生了氧化还原反应。
a.写出SO2与FeCl3溶液反应的离子方程式:
b.请设计实验方案检验上述反应中FeCl3是否反应完全:
c.若向得到的浅绿色溶液中逐滴滴加NaOH溶液,可以观察到的现象是:
更新时间:2019-12-24 10:25:02
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】二氧化硫是硫的重要化合物,在生产、生活中有广泛应用,是大气主要污染物之一,具有一定的还原性,探究SO2气体还原Fe3+、I2,可以使用的药品和装置如图所示:

(1)写出由铜和浓硫酸制取SO2的化学方程式_______________________________________ 。
(2)装置A中的现象是__________________________________________ 。
(3)根据以上现象,该小组同学认为SO2与FeCl3发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式____________________________________________ ;
②请设计实验方案检验有Fe2+生成___________________________________________________ 。
(4)B中蓝色溶液褪色,表明I-的还原性比SO2__________ (填“强”或“弱”)。

(1)写出由铜和浓硫酸制取SO2的化学方程式
(2)装置A中的现象是
(3)根据以上现象,该小组同学认为SO2与FeCl3发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式
②请设计实验方案检验有Fe2+生成
(4)B中蓝色溶液褪色,表明I-的还原性比SO2
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】硫酰氯(SO2Cl2)是一种重要的化工试剂,实验室合成硫酰氯的实验装置如图所示:

已知:①SO2(g)+Cl2(g) SO2Cl2(l)△H=-97.3kJ•mol-1
SO2Cl2(l)△H=-97.3kJ•mol-1
②硫酰氯常温下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中易“发烟”;
③100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氯气。
(1)仪器a为恒压分液漏斗,与普通分液漏斗相比,其优点是___________ 。
(2)仪器b的名称为___________ ,干燥管中碱石灰的主要作用是___________ 。
(3)装置E为储气装置,用于提供氯气,则分液漏斗c中盛放的试剂为___________ 。长期存放的硫酰氯会发黄,其原因可能为___________ 。
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为___________ ,分离这两种液态产物的方法是___________ 。
(5)若将SO2、Cl2按照一定比例通入水中,请设计简单实验验证二者是否恰好完全反应。___________ (简要描述实验步骤、现象和结论)。
(6)SO2Cl2纯度的测定:取1.50 g SO2Cl2产品在密闭条件下溶于烧碱溶液,最后定容为250mL溶液,取25.00mL该溶液用0.1000moL/L的AgNO3标准溶液滴定(用K2CrO4作指示剂,滴定过程种 不参与反应),平行滴定三次,平均消耗AgNO3标准溶液22.00mL,则SO2Cl2产品的纯度为
不参与反应),平行滴定三次,平均消耗AgNO3标准溶液22.00mL,则SO2Cl2产品的纯度为___________ 。

已知:①SO2(g)+Cl2(g)
 SO2Cl2(l)△H=-97.3kJ•mol-1
SO2Cl2(l)△H=-97.3kJ•mol-1②硫酰氯常温下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中易“发烟”;
③100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氯气。
(1)仪器a为恒压分液漏斗,与普通分液漏斗相比,其优点是
(2)仪器b的名称为
(3)装置E为储气装置,用于提供氯气,则分液漏斗c中盛放的试剂为
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为
(5)若将SO2、Cl2按照一定比例通入水中,请设计简单实验验证二者是否恰好完全反应。
(6)SO2Cl2纯度的测定:取1.50 g SO2Cl2产品在密闭条件下溶于烧碱溶液,最后定容为250mL溶液,取25.00mL该溶液用0.1000moL/L的AgNO3标准溶液滴定(用K2CrO4作指示剂,滴定过程种
 不参与反应),平行滴定三次,平均消耗AgNO3标准溶液22.00mL,则SO2Cl2产品的纯度为
不参与反应),平行滴定三次,平均消耗AgNO3标准溶液22.00mL,则SO2Cl2产品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
真题
【推荐3】聚合硫酸铁又称聚铁,化学式[Fe2(OH)n(SO4)3-0.5n]n,广泛用于污水处理,实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、 SiO2等)制备聚铁和绿矾(FeSO4·7H2O),过程如下:
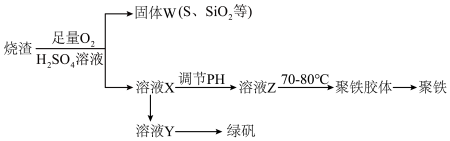
(1)验证固体W焙烧后产生的气体含有SO2的方法是_____________ 。
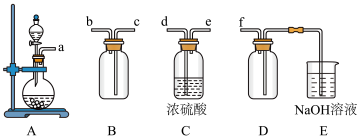
(2)实验室制备,收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各仪器口,顺序为a→_____ →_____ →_____ →_____ →f。装置D的作用是_________ ,装置E中NaOH溶液的作用是________________ 。
(3)制备绿矾时,向溶液X中加入过量_________ ,充分反应后,经_________ 操作得到溶液Y,再经浓缩、结晶等步骤得到绿矾。
(4)溶液Z的pH影响聚铁中铁的质量分数,用pH试纸测定溶液pH的操作方法为________ 。
若溶液Z的pH偏小,将导致聚铁中铁的质量分数偏_____________________ 。

(1)验证固体W焙烧后产生的气体含有SO2的方法是
(2)实验室制备,收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各仪器口,顺序为a→

(3)制备绿矾时,向溶液X中加入过量
(4)溶液Z的pH影响聚铁中铁的质量分数,用pH试纸测定溶液pH的操作方法为
若溶液Z的pH偏小,将导致聚铁中铁的质量分数偏
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】已知 ,某同学认为钠和
,某同学认为钠和 也可以发生类似的反应,他在实验室中选择如图所示的装置对钠与
也可以发生类似的反应,他在实验室中选择如图所示的装置对钠与 的反应进行了实验探究。依据要求回答问题:
的反应进行了实验探究。依据要求回答问题:
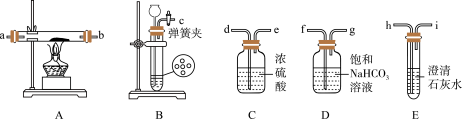
(1)实验室制备 的化学反应方程式为
的化学反应方程式为________
(2)为达到实验目的,题图装置的连接顺序为c→_______
(3)装置气密性良好,装好药品后打开弹簧夹,待装置中的空气排尽后点燃酒精灯。能说明装置中空气已经排尽的现象是____________
(4)该同学用稀盐酸与 反应制备
反应制备 ,向装置B中加入稀盐酸后,发现
,向装置B中加入稀盐酸后,发现 与稀盐酸没有接触。由于稀盐酸已经用完,为使反应顺利进行可再加入的试剂是
与稀盐酸没有接触。由于稀盐酸已经用完,为使反应顺利进行可再加入的试剂是______
A 稀硝酸 B 溶液 C 苯 D
溶液 C 苯 D 
(5)若反应过程中 足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:
足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:
①生成的固体物质为
②生成的固体物质为 和C的混合物
和C的混合物
③生成的固体物质为 和
和 的混合物
的混合物
④生成的固体物质为 和C的混合物
和C的混合物
该同学报告给老师后,老师认为可以排除其中的3种情况,老师排除的理由是________
(6)该同学经过反思,认为上述实验设计中存在缺陷。该缺陷是___________
 ,某同学认为钠和
,某同学认为钠和 也可以发生类似的反应,他在实验室中选择如图所示的装置对钠与
也可以发生类似的反应,他在实验室中选择如图所示的装置对钠与 的反应进行了实验探究。依据要求回答问题:
的反应进行了实验探究。依据要求回答问题:
(1)实验室制备
 的化学反应方程式为
的化学反应方程式为(2)为达到实验目的,题图装置的连接顺序为c→
(3)装置气密性良好,装好药品后打开弹簧夹,待装置中的空气排尽后点燃酒精灯。能说明装置中空气已经排尽的现象是
(4)该同学用稀盐酸与
 反应制备
反应制备 ,向装置B中加入稀盐酸后,发现
,向装置B中加入稀盐酸后,发现 与稀盐酸没有接触。由于稀盐酸已经用完,为使反应顺利进行可再加入的试剂是
与稀盐酸没有接触。由于稀盐酸已经用完,为使反应顺利进行可再加入的试剂是A 稀硝酸 B
 溶液 C 苯 D
溶液 C 苯 D 
(5)若反应过程中
 足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:
足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:①生成的固体物质为

②生成的固体物质为
 和C的混合物
和C的混合物③生成的固体物质为
 和
和 的混合物
的混合物④生成的固体物质为
 和C的混合物
和C的混合物该同学报告给老师后,老师认为可以排除其中的3种情况,老师排除的理由是
(6)该同学经过反思,认为上述实验设计中存在缺陷。该缺陷是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某小组设计了如下图所示的实验装置来探究过氧化钠的强氧化性。
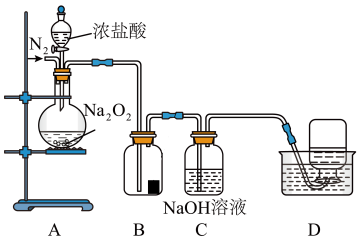
实验步骤及现象如下:
①检查装置气密性后,装入药品并连接装置A、B、C。
②缓慢通入一定量的N2后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,A中剧烈反应,有黄绿色气体产生。
③待装置D中导管口产生连续气泡后,将导管末端伸入集气瓶中,收集到无色气体。
④反应一段时间后,停止滴加浓盐酸,再通一段时间N2,直至装置中气体变为无色。
(1)装置D中收集的无色气体X能使带火星的木条复燃,据此推断该气体X是___________ 。
(2)装置B中湿润的淀粉碘化钾试纸变蓝。
甲同学根据A中气体的颜色推测试纸变蓝时发生反应的离子方程式为___________ ;
乙同学认为使试纸变蓝的原因也可能是___________ (填序号)。
a.挥发的HCl气体使试纸变蓝
b.在此实验过程中生成的X气体也能将I-氧化为I2
c.通入的N2使试纸变蓝
(3)C中NaOH溶液的作用是___________ 。
(4)Na2O2与干燥的HCl能发生化学反应生成Cl2、NaCl和H2O,该反应的化学方程式为___________ ,当反应生成标准状况下2.24L Cl2时,转移的电子数为___________ mol。

实验步骤及现象如下:
①检查装置气密性后,装入药品并连接装置A、B、C。
②缓慢通入一定量的N2后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,A中剧烈反应,有黄绿色气体产生。
③待装置D中导管口产生连续气泡后,将导管末端伸入集气瓶中,收集到无色气体。
④反应一段时间后,停止滴加浓盐酸,再通一段时间N2,直至装置中气体变为无色。
(1)装置D中收集的无色气体X能使带火星的木条复燃,据此推断该气体X是
(2)装置B中湿润的淀粉碘化钾试纸变蓝。
甲同学根据A中气体的颜色推测试纸变蓝时发生反应的离子方程式为
乙同学认为使试纸变蓝的原因也可能是
a.挥发的HCl气体使试纸变蓝
b.在此实验过程中生成的X气体也能将I-氧化为I2
c.通入的N2使试纸变蓝
(3)C中NaOH溶液的作用是
(4)Na2O2与干燥的HCl能发生化学反应生成Cl2、NaCl和H2O,该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】如图所示是一个制取氯气并以氯气为原料进行特定反应的装置,多余的氯气可以贮存在b瓶中,其中各试剂瓶中所装试剂为:C(氯化亚铁溶液)、D(碘化钾淀粉溶液)、E(紫色石蕊试液)、G(含酚酞的氢氧化钠溶液)

(1)A是氯气的发生装置,反应的离子方程式为________________________ 。
(2)a仪器的名称为_________________ ,B中宜加入的液体是_________________ 。
(3)实验开始后C中反应的离子方程式是________________________________ ,D中的现象是___________________ ,E中的现象是____________________________ 。
(4)F装置中硬质玻璃管内盛有炭粉,若F中发生氧化还原反应,其产物为二氧化碳和氯化氢,则F中反应的化学方程式为___________________________________________ 。
(5)G中发生氧化还原反应的离子方程式为________________________________ 。
(6)F处反应完毕后,关闭活塞K,移去酒精灯,由于余热的作用,A处仍有Cl2产生,则装置B中的现象是____________________________ ;若发现装置B中该现象不明显,可能的原因是A或B装置漏气,查找原因时若用蘸有浓氨水的玻璃棒检查时观察到有白烟产生,写出该氧化还原反应的化学方程式_____________________________ 。

(1)A是氯气的发生装置,反应的离子方程式为
(2)a仪器的名称为
(3)实验开始后C中反应的离子方程式是
(4)F装置中硬质玻璃管内盛有炭粉,若F中发生氧化还原反应,其产物为二氧化碳和氯化氢,则F中反应的化学方程式为
(5)G中发生氧化还原反应的离子方程式为
(6)F处反应完毕后,关闭活塞K,移去酒精灯,由于余热的作用,A处仍有Cl2产生,则装置B中的现象是
您最近一年使用:0次



