2016年10月17日7时30分,我国“神舟十一号”载人飞船顺利升入太空。此次火箭的主要燃料是偏二甲肼(C2N2H8)和一种氮的氧化物(用R表示),当火箭发射时,这两种燃料会剧烈反应产生大量气体,并释放出大量的热,化学方程式如下(已配平):C2N2H8+2R=3N2↑+4H2O+2CO2↑
(1)R的化学式是___ ;已知偏二甲肼中N元素显-2价,H元素显+1价,由此推断,C元素的化合价是___ 。
(2)该反应的还原剂是___ ,被还原的元素是___ 。
(3)若反应生成22.4LCO2(标准状况),则反应转移电子___ mol。
(4)火箭发射时,尾部向下喷出的气体会有明显的红棕色,该红棕色气体的化学式可能是___ 。
(5)高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂。Na2FeO4能给水消毒利用的是___ 性。用Na2FeO4给水消毒、杀菌时得到的Fe3+可以净水,其净水原理与明矾相同,Fe3+净水原理是___ (用简要的文字叙述)。
(1)R的化学式是
(2)该反应的还原剂是
(3)若反应生成22.4LCO2(标准状况),则反应转移电子
(4)火箭发射时,尾部向下喷出的气体会有明显的红棕色,该红棕色气体的化学式可能是
(5)高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂。Na2FeO4能给水消毒利用的是
更新时间:2019-12-25 17:27:59
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室制备Cl2通常采用如图所示装置:

(1)A中发生反应的化学方程式是________ ,其中氧化剂是_____ ,还原剂是_____ 。
(2)仪器a的名称是__________ 。
(3)B装置中所盛的试剂是________ ,C装置的作用是___________ 。
(4)装置E的作用是__________ ,该反应的离子方程式为__________ 。
(5)当装置D收集到标况下气体体积11.2L,转移的电子物质的量为______ 。
(6)将下图装置代替D和E装置,可进行“氯气与金属钠反应”的实验,以下叙述正确的是_____。
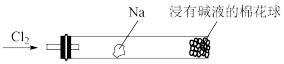

(1)A中发生反应的化学方程式是
(2)仪器a的名称是
(3)B装置中所盛的试剂是
(4)装置E的作用是
(5)当装置D收集到标况下气体体积11.2L,转移的电子物质的量为
(6)将下图装置代替D和E装置,可进行“氯气与金属钠反应”的实验,以下叙述正确的是_____。
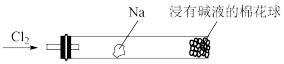
| A.反应生成的大量白烟是氯化钠晶体 |
| B.玻璃管尾部塞一团浸有碱液的棉球是用于吸收过量的氯气,以免其污染空气 |
| C.玻璃管中,钠燃烧时会产生苍白色火焰 |
| D.若在棉球外沿滴一滴淀粉-KI溶液,可据其颜色变化判断氯气是否被碱液完全吸收 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题。
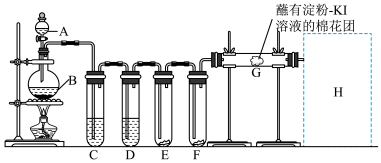
(1)A中盛有浓盐酸,B中盛有MnO2,写出反应的化学方程式___________ ;此反应中盐酸表现___________ 性。如果有8.7克MnO2完全反应完,被氧化的HCl的质量是___________ 。
(2)D中放入浓H2SO4,其目的是___________ 。
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是___________ ,对比E和F中现象的差异可得出的结论及解释是___________ 。
(4)G处的现象是___________ 。
(5)画出H处尾气吸收装置图并注明试剂___________ ,发生反应的离子方程式为___________ 。
(6)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。消毒液与洁厕灵同时使用会产生有毒的氯气,写出反应的离子方程式___________ 。

(1)A中盛有浓盐酸,B中盛有MnO2,写出反应的化学方程式
(2)D中放入浓H2SO4,其目的是
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是
(4)G处的现象是
(5)画出H处尾气吸收装置图并注明试剂
(6)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。消毒液与洁厕灵同时使用会产生有毒的氯气,写出反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、W、P为短周期的主族元素,其原子序数依次增大。Y、Z、W、P位于同一周期。X 元素形成的单质是自然界中含量最多的气体,1mol Y的单质分别与足量盐酸和氢氧化钠溶液反应生成的气体在标况下均为33.6L。W的原子最外层电子数与核外电子总数之比为3:8,X的原子序数是Z的原子序数的一半。
(1)Y在周期表中的位置是_______ ;X的氢化物与P的氢化物接近时的现象是_______ .。
(2)W与P可形成一种个数比为1:2的化合物的电子式是_______ 。
(3)Y与P形成的化合物溶液显_______ 性;用离子方程式表示显示这种性质的原因是_______ 。
(4)Z、W、P三种元素的气态氢化物稳定性由高到低的顺序是_______ ;
(5)X的三氟化物是微电子工业中优良的等离子刻蚀气体,但是在潮湿的环境中能够与水发生反应生成无色气体,遇到空气变为红棕色。写出此三氟化物与水反应的化学方程式_______ ;若0.6mol的X的三氟化物完全与水反应,则转移的电子总数约是_______ 个。
(1)Y在周期表中的位置是
(2)W与P可形成一种个数比为1:2的化合物的电子式是
(3)Y与P形成的化合物溶液显
(4)Z、W、P三种元素的气态氢化物稳定性由高到低的顺序是
(5)X的三氟化物是微电子工业中优良的等离子刻蚀气体,但是在潮湿的环境中能够与水发生反应生成无色气体,遇到空气变为红棕色。写出此三氟化物与水反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】已知氮元素及其化合物的转化关系如图所示,回答下列问题。

(1)①~④各步转化中,属于氮的固定的是___________ (填序号)。
(2)实验室制备氨气时,常用氯化铵与熟石灰制取。
①该原理的化学方程式是___________ 。
②干燥氨气不可选用的试剂是___________ (填字母)。
a.浓硫酸 b.碱石灰 c.氯化钙固体 d.氢氧化钠固体
(3)工业制硝酸时尾气中含有NO、 ,可用以下方法吸收:
,可用以下方法吸收:
①水吸收法。
用水直接吸收 存在明显的缺陷,需通入适量的氧气加以改进,用化学方程式说明通入适量氧气的优势
存在明显的缺陷,需通入适量的氧气加以改进,用化学方程式说明通入适量氧气的优势___________ 。
②NaOH溶液吸收法。
发生的反应有: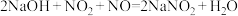 ,
,
___________ 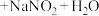 (填化学式,不需要配平方程式)。
(填化学式,不需要配平方程式)。
③用不同浓度的NaOH溶液吸收 含量不同的尾气,关系如图:
含量不同的尾气,关系如图:
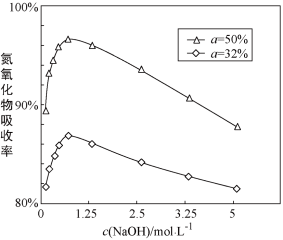
(α表示尾气里 的含量)
的含量)
Ⅰ.根据如图和题中相关信息可得知___________ (填字母)。
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b. 含量越大,氮氧化物的吸收率越大
含量越大,氮氧化物的吸收率越大
c.足量的氢氧化钠溶液吸收尾气,剩余气体只有NO
Ⅱ.标准状况下,当α等于50%时,用一定量尾气与足量NaOH溶液做喷泉实验,假设生成的溶液全在烧瓶中,求实验后得到的 溶液的物质的量浓度
溶液的物质的量浓度___________ (保留两位有效数字)。

(1)①~④各步转化中,属于氮的固定的是
(2)实验室制备氨气时,常用氯化铵与熟石灰制取。
①该原理的化学方程式是
②干燥氨气不可选用的试剂是
a.浓硫酸 b.碱石灰 c.氯化钙固体 d.氢氧化钠固体
(3)工业制硝酸时尾气中含有NO、
 ,可用以下方法吸收:
,可用以下方法吸收:①水吸收法。
用水直接吸收
 存在明显的缺陷,需通入适量的氧气加以改进,用化学方程式说明通入适量氧气的优势
存在明显的缺陷,需通入适量的氧气加以改进,用化学方程式说明通入适量氧气的优势②NaOH溶液吸收法。
发生的反应有:
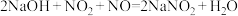 ,
,
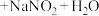 (填化学式,不需要配平方程式)。
(填化学式,不需要配平方程式)。③用不同浓度的NaOH溶液吸收
 含量不同的尾气,关系如图:
含量不同的尾气,关系如图:
(α表示尾气里
 的含量)
的含量)Ⅰ.根据如图和题中相关信息可得知
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b.
 含量越大,氮氧化物的吸收率越大
含量越大,氮氧化物的吸收率越大c.足量的氢氧化钠溶液吸收尾气,剩余气体只有NO
Ⅱ.标准状况下,当α等于50%时,用一定量尾气与足量NaOH溶液做喷泉实验,假设生成的溶液全在烧瓶中,求实验后得到的
 溶液的物质的量浓度
溶液的物质的量浓度
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某强酸性溶液 可能含有
可能含有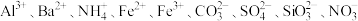 中的一种或几种,取该浴液进行实验,其现象及转化如图所示。反应过程中有一种气体为红棕色。
中的一种或几种,取该浴液进行实验,其现象及转化如图所示。反应过程中有一种气体为红棕色。
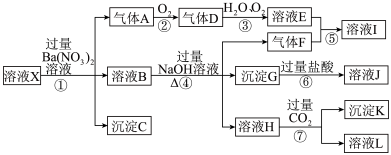
请回答下列问题:
(1)由强酸性条件即可判断溶液X中一定不存在的离子有_______ 。
(2)溶液X中,关于 的判断一定正确的是
的判断一定正确的是_______ (填字母)
A.一定有 B.一定没有 C.可能有
(3)产生气体A的离子方程式为_______ 。
(4)转化⑥发生反应产生的现象为_______ 。
(5)转化④中生成 的离子方程式为
的离子方程式为_______ 。
(6)若转化③中,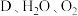 三种物质恰好发生化合反应生成
三种物质恰好发生化合反应生成 ,则反应中
,则反应中 与
与 的物质的量之比为
的物质的量之比为_______ 。
(7)对于不能确定是否存在的离子,可以另取溶液X,加入_______ (填试剂名称),根据现象即可判断。
 可能含有
可能含有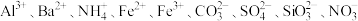 中的一种或几种,取该浴液进行实验,其现象及转化如图所示。反应过程中有一种气体为红棕色。
中的一种或几种,取该浴液进行实验,其现象及转化如图所示。反应过程中有一种气体为红棕色。
请回答下列问题:
(1)由强酸性条件即可判断溶液X中一定不存在的离子有
(2)溶液X中,关于
 的判断一定正确的是
的判断一定正确的是A.一定有 B.一定没有 C.可能有
(3)产生气体A的离子方程式为
(4)转化⑥发生反应产生的现象为
(5)转化④中生成
 的离子方程式为
的离子方程式为(6)若转化③中,
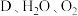 三种物质恰好发生化合反应生成
三种物质恰好发生化合反应生成 ,则反应中
,则反应中 与
与 的物质的量之比为
的物质的量之比为(7)对于不能确定是否存在的离子,可以另取溶液X,加入
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如图所示(反应条件及其他物质已经略去)。请回答下列问题:

(1)若A在常温下为固体单质,B是能使品红溶液褪色的有刺激性气味的无色气体。写出B→C的化学方程式___________ 。
(2)若A在常温下为气体单质,C是红棕色气体。
①写出化学反应方程式:A→B___________ ;B→C__________ ;
②用充满C气体(标准状态下)的圆底烧瓶做喷泉实验,实验结束时,烧瓶内硝酸的物质的量浓度为___________ mol/L。
(3)若A在常温下为非金属气态氢化物,C是红棕色气体。
①写出实验室制取A气体的化学方程式___________ 。
②写出A→B的化学方程式___________ 。
(4)若A是一种非金属单质,C是一种无色无味且能使澄清石灰水变浑浊的气体。
①写出A与 反应的化学方程式
反应的化学方程式___________ 。
②写出A与浓硫酸反应的化学方程式___________ 。

(1)若A在常温下为固体单质,B是能使品红溶液褪色的有刺激性气味的无色气体。写出B→C的化学方程式
(2)若A在常温下为气体单质,C是红棕色气体。
①写出化学反应方程式:A→B
②用充满C气体(标准状态下)的圆底烧瓶做喷泉实验,实验结束时,烧瓶内硝酸的物质的量浓度为
(3)若A在常温下为非金属气态氢化物,C是红棕色气体。
①写出实验室制取A气体的化学方程式
②写出A→B的化学方程式
(4)若A是一种非金属单质,C是一种无色无味且能使澄清石灰水变浑浊的气体。
①写出A与
 反应的化学方程式
反应的化学方程式②写出A与浓硫酸反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】硫酸厂烧渣(主要成分是Fe2O3,其次含少量的SiO2和FeS)经回收处理可制得绿矾(FeSO4·7H2O)和一种重要的水处理剂聚铁胶体[Fe(OH)SO4]n,上述生产工艺流程如下:
请通过分析回答下列相关问题:
(1)操作Ⅰ的名称是_____ 。
(2)灼烧产生的尾气对大气有污染,因此工业生产中必须进行回收处理,下列方法可行的是____________ 。
A.直接用水吸收 B. 用氨水吸收
C. 用浓硫酸吸收 D. 与空气混合用石灰石粉末悬浊液吸收
(3)操作Ⅲ经蒸发浓缩、___________ 、过滤、____ 、干燥等。
(4)在由溶液X制聚铁胶体过程中①调节pH及②控制温度目的是_________ 。
(5)检验溶液X中金属阳离子所加试剂是______ ,其现象是___________ 。
(6)溶液X转化为溶液Y需加入一种常见物质是____________ 。
(7)在反应釜中FeS、O2及稀H2SO4反应生成硫酸铁等物质,则反应的离子方程式是________________________________________________________ 。

请通过分析回答下列相关问题:
(1)操作Ⅰ的名称是
(2)灼烧产生的尾气对大气有污染,因此工业生产中必须进行回收处理,下列方法可行的是
A.直接用水吸收 B. 用氨水吸收
C. 用浓硫酸吸收 D. 与空气混合用石灰石粉末悬浊液吸收
(3)操作Ⅲ经蒸发浓缩、
(4)在由溶液X制聚铁胶体过程中①调节pH及②控制温度目的是
(5)检验溶液X中金属阳离子所加试剂是
(6)溶液X转化为溶液Y需加入一种常见物质是
(7)在反应釜中FeS、O2及稀H2SO4反应生成硫酸铁等物质,则反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某班同学用实验室中的硫酸亚铁固体和硫酸铁进行实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)甲同学取一定量硫酸亚铁固体,配制FeSO4溶液,取少量溶液于试管,加入2滴KSCN溶液,溶液________ ,甲同学认为硫酸亚铁固体已全部变质。
(2)乙同学认为甲同学的结论不够严谨,他取2mL甲同学配成的FeSO4溶液,加入少量的酸性高锰酸钾溶液,_______ ,乙同学认为硫酸亚铁固体部分变质,理由_____________ (用离子方程式结合文字说明回答)。
(3)甲同学继续探究Fe2+的性质,接着他向盛有H2O2溶液的试管中加入几滴甲同学配成的FeSO4溶液,发生反应的离子方程式为________ ;一段时间后,发现溶液中有气泡出现,产生气泡的原因是_______ 。
(4)丙同学取一定量硫酸铁固体,配制Fe2(SO4)3溶液,取少量溶液于试管,加入铜粉,反应中氧化性:Fe3+_____ Cu2+(填“>”或“<”)。
(5)丁同学向混有少量泥沙的浑浊水中加入Fe2(SO4)3溶液,振荡,然后将试管静置一段时间,观察试管中发生的现象是_______ 。
(1)甲同学取一定量硫酸亚铁固体,配制FeSO4溶液,取少量溶液于试管,加入2滴KSCN溶液,溶液
(2)乙同学认为甲同学的结论不够严谨,他取2mL甲同学配成的FeSO4溶液,加入少量的酸性高锰酸钾溶液,
(3)甲同学继续探究Fe2+的性质,接着他向盛有H2O2溶液的试管中加入几滴甲同学配成的FeSO4溶液,发生反应的离子方程式为
(4)丙同学取一定量硫酸铁固体,配制Fe2(SO4)3溶液,取少量溶液于试管,加入铜粉,反应中氧化性:Fe3+
(5)丁同学向混有少量泥沙的浑浊水中加入Fe2(SO4)3溶液,振荡,然后将试管静置一段时间,观察试管中发生的现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】亚氯酸钠(NaClO2)具有强氧化性,受热易分解,可作漂白剂、食品消毒剂等。
Ⅰ.亚氯酸钠的制备
以氯酸钠等为原料制备亚氯酸钠的工艺流程如下:
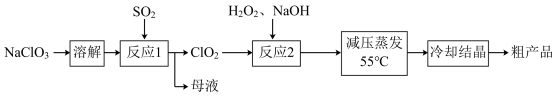
(1)提高“反应1”反应速率的措施有__________________ (答出一条即可)。母液中溶质的主要成分是___________ (填化学式)。
(2)每有1mol SO2参加反应,理论上可生成ClO2的物质的量为________ mol。
(3) “反应2”的化学方程式为_____________________________________ 。
(4)采取“减压蒸发”而不用“常压蒸发”,原因是____________________ 。
(5)“反应2”中使用H2O2而不用其他物质的原因是____________________ 。
Ⅱ.亚氯酸钠的应用
(6)用亚氯酸钠作水处理剂,水中可能残留少量亚氯酸钠,可以加入硫酸亚铁除去残留的亚氯酸盐,硫酸亚铁除可与亚氯酸钠反应外,还可以起到的作用是____________ 。
(7)实验室可用亚氯酸钠和氯酸钠在酸性条件下反应制备ClO2气体。写出上述反应的离子方程式为____________________________ 。
Ⅰ.亚氯酸钠的制备
以氯酸钠等为原料制备亚氯酸钠的工艺流程如下:

(1)提高“反应1”反应速率的措施有
(2)每有1mol SO2参加反应,理论上可生成ClO2的物质的量为
(3) “反应2”的化学方程式为
(4)采取“减压蒸发”而不用“常压蒸发”,原因是
(5)“反应2”中使用H2O2而不用其他物质的原因是
Ⅱ.亚氯酸钠的应用
(6)用亚氯酸钠作水处理剂,水中可能残留少量亚氯酸钠,可以加入硫酸亚铁除去残留的亚氯酸盐,硫酸亚铁除可与亚氯酸钠反应外,还可以起到的作用是
(7)实验室可用亚氯酸钠和氯酸钠在酸性条件下反应制备ClO2气体。写出上述反应的离子方程式为
您最近一年使用:0次



