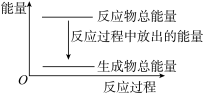
以NA代表阿伏加 德罗常数,则关于热化学方程式C2H2(g)+  O2(g) →2CO2(g)+H2O(l) ;ΔH=-1 300 kJ·mol-1的说法中,正确的是( )
O2(g) →2CO2(g)+H2O(l) ;ΔH=-1 300 kJ·mol-1的说法中,正确的是( )
 O2(g) →2CO2(g)+H2O(l) ;ΔH=-1 300 kJ·mol-1的说法中,正确的是( )
O2(g) →2CO2(g)+H2O(l) ;ΔH=-1 300 kJ·mol-1的说法中,正确的是( )| A.当5NA个电子转移时,该反应放出1 300 kJ的能量 |
| B.当1NA个水分子生成且为液体时,吸收1 300 kJ的能量 |
| C.当2NA个碳氧共用电子对生成时,放出1 300 kJ的能量 |
| D.当8NA个碳氧共用电子对生成时,放出1 300 kJ的能量 |
更新时间:2020-01-02 17:19:18
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.1.0 mol NO和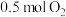 混合充分反应后,气体分子总数为 混合充分反应后,气体分子总数为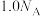 |
B.对于反应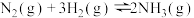 ΔH=-92.4 kJ/mol,当放出92.4 kJ热量时,生成 ΔH=-92.4 kJ/mol,当放出92.4 kJ热量时,生成 的数目小于 的数目小于 |
C.常温下,1 L pH=1的 溶液由水电离出 溶液由水电离出 的数目为 的数目为 |
D.12 g石墨含有的共价键数目为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法中错误的是
A.云变成雨的过程中, 减小 减小 |
| B.吸热反应在一定条件下也能自发进行 |
| C.化学反应达到平衡状态时,体系中各物质的反应速率均等于零 |
| D.热化学方程式中的系数表示物质的量,因此可以是分数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】用CH4催化还原NOx可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g)ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g)ΔH=-1 160 kJ·mol-1
下列说法不正确的是( )
①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g)ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g)ΔH=-1 160 kJ·mol-1
下列说法不正确的是( )
| A.反应①②均为放热反应 |
| B.等物质的量的甲烷分别发生反应①②,转移电子数相同 |
| C.由反应①可推知:CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(l) ΔH=-a kJ·mol-1,a<574 |
| D.若用标准状况下4.48 L CH4还原NO2至N2,放出的热量为173.4 kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】氢化热是指一定条件下,1mol不饱和化合物加氢时放出的热量。表中是环己烯( )、环己二烯(
)、环己二烯( )和苯的氢化热数据:
)和苯的氢化热数据:
根据表中数据推断正确的是( )
 )、环己二烯(
)、环己二烯( )和苯的氢化热数据:
)和苯的氢化热数据:| 物质 |  +H2 +H2 |  +2H2 +2H2 |  +3H2 +3H2 |
| 氢化热(kJ/mol) | 119.7 | 232.7 | 208.4 |
根据表中数据推断正确的是( )
| A.环己二烯与H2的反应最剧烈 |
| B.环己烯、环己二烯和苯有相同的官能团 |
| C.三种化合物中环己二烯的稳定性最强 |
D.上述条件下,1mol 转变 转变 为时放出热量 为时放出热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知:2X(g)+Y(g) 2Z(s) ΔH=-akJ·mol-1。T°C,将2mol X(g)和1mol Y(g)加入体积为1L的密闭容器中进行反应,10min后达到平衡,生成0.2mol Z,共放出热量b kJ,下列说法不正确的是
2Z(s) ΔH=-akJ·mol-1。T°C,将2mol X(g)和1mol Y(g)加入体积为1L的密闭容器中进行反应,10min后达到平衡,生成0.2mol Z,共放出热量b kJ,下列说法不正确的是
 2Z(s) ΔH=-akJ·mol-1。T°C,将2mol X(g)和1mol Y(g)加入体积为1L的密闭容器中进行反应,10min后达到平衡,生成0.2mol Z,共放出热量b kJ,下列说法不正确的是
2Z(s) ΔH=-akJ·mol-1。T°C,将2mol X(g)和1mol Y(g)加入体积为1L的密闭容器中进行反应,10min后达到平衡,生成0.2mol Z,共放出热量b kJ,下列说法不正确的是| A.其他条件不变,若压缩容器,反应速率增大 |
| B.在0~10min内,X的反应速率为0.02mol·L-1·min-1 |
| C.达到化学平衡状态时,X、Y的转化率相等 |
D.在0~10min内,Y的反应速率可表示为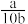 mol·L-1·min-1 mol·L-1·min-1 |
您最近一年使用:0次