为了降低电子垃圾对环境构成的影响,将一批废弃的线路板简单处理后,得到含 、
、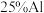 、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:

 第
第 步Cu与混酸反应的离子方程式为
步Cu与混酸反应的离子方程式为______  得到滤渣1的主要成分为
得到滤渣1的主要成分为______ 。
 第
第 步中加入
步中加入 的作用是
的作用是______ ,使用 的优点是
的优点是______ ;调溶液pH的目的是______ 。
 简述第
简述第 步由滤液2得到
步由滤液2得到 的方法是
的方法是______ 。
 由滤渣2制取
由滤渣2制取 ,设计了以下三种方案:
,设计了以下三种方案:
甲:滤渣 酸浸液
酸浸液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O
乙:滤渣 酸浸液
酸浸液 滤液
滤液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O
丙:滤渣2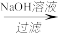 滤液
滤液 溶液
溶液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O
上述三种方案中,______ 方案不可行,原因是______ ;从原子利用率角度考虑,______ 方案更合理。
 用滴定法测定
用滴定法测定 含量.取a g试样配成100mL溶液,每次取
含量.取a g试样配成100mL溶液,每次取 ,消除干扰离子后,用c
,消除干扰离子后,用c
 标准溶液滴定至终点,平均消耗EDTA溶液b
标准溶液滴定至终点,平均消耗EDTA溶液b  滴定反应如下:
滴定反应如下: 写出计算
写出计算 质量分数的表达式
质量分数的表达式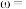
______ 。
 、
、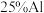 、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
| 方法Ⅰ | 用炭粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法:  |
| 方法Ⅲ | 用肼 还原新制 还原新制 |
 第
第 步Cu与混酸反应的离子方程式为
步Cu与混酸反应的离子方程式为 得到滤渣1的主要成分为
得到滤渣1的主要成分为 第
第 步中加入
步中加入 的作用是
的作用是 的优点是
的优点是 简述第
简述第 步由滤液2得到
步由滤液2得到 的方法是
的方法是 由滤渣2制取
由滤渣2制取 ,设计了以下三种方案:
,设计了以下三种方案:甲:滤渣
 酸浸液
酸浸液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O乙:滤渣
 酸浸液
酸浸液 滤液
滤液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O丙:滤渣2
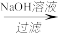 滤液
滤液 溶液
溶液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O上述三种方案中,
 用滴定法测定
用滴定法测定 含量.取a g试样配成100mL溶液,每次取
含量.取a g试样配成100mL溶液,每次取 ,消除干扰离子后,用c
,消除干扰离子后,用c
 标准溶液滴定至终点,平均消耗EDTA溶液b
标准溶液滴定至终点,平均消耗EDTA溶液b  滴定反应如下:
滴定反应如下: 写出计算
写出计算 质量分数的表达式
质量分数的表达式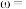
更新时间:2020-01-06 18:16:42
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】明矾石的主要成分是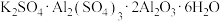 ,还含有少量
,还含有少量 杂质。利用明矾石制备
杂质。利用明矾石制备 和
和 晶体的流程如图:
晶体的流程如图:
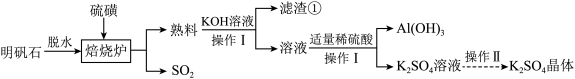
已知:焙烧炉中发生反应的化学方程式为 ,回答下列问题:
,回答下列问题:
(1)“滤渣①”的主要成分为_______ ,“操作Ⅰ”的名称为_______ ,实验室进行“操作Ⅱ”时,需要使用下列仪器中的_______ 。
a.坩埚 b.蒸发皿 c.铁架台(带铁圈) d.玻璃棒 e.烧杯
(2)“熟料”与 溶液反应的离子方程式为
溶液反应的离子方程式为_______ 。
(3)生成的 需进一步洗涤干燥,证明
需进一步洗涤干燥,证明 沉淀已洗涤干净的实验操作和现象是
沉淀已洗涤干净的实验操作和现象是_______ 。
(4)若“焙烧”过程中恰好消耗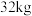 硫黄,则理论上最终可得到
硫黄,则理论上最终可得到_______  氢氧化铝。
氢氧化铝。
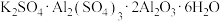 ,还含有少量
,还含有少量 杂质。利用明矾石制备
杂质。利用明矾石制备 和
和 晶体的流程如图:
晶体的流程如图:
已知:焙烧炉中发生反应的化学方程式为
 ,回答下列问题:
,回答下列问题:(1)“滤渣①”的主要成分为
a.坩埚 b.蒸发皿 c.铁架台(带铁圈) d.玻璃棒 e.烧杯
(2)“熟料”与
 溶液反应的离子方程式为
溶液反应的离子方程式为(3)生成的
 需进一步洗涤干燥,证明
需进一步洗涤干燥,证明 沉淀已洗涤干净的实验操作和现象是
沉淀已洗涤干净的实验操作和现象是(4)若“焙烧”过程中恰好消耗
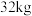 硫黄,则理论上最终可得到
硫黄,则理论上最终可得到 氢氧化铝。
氢氧化铝。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】废水中过量的氨氮( 和
和 )会导致水体富营养化。某科研小组用
)会导致水体富营养化。某科研小组用 氧化法处理氨氮废水。已知:①
氧化法处理氨氮废水。已知:① 的氧化性比
的氧化性比 强;②
强;② 比
比 更易被氧化;③国家相关标准要求经处理过的氨氮废水
更易被氧化;③国家相关标准要求经处理过的氨氮废水 要控制在6~9。
要控制在6~9。
(1) 时,
时, 可与
可与 反应生成
反应生成 等无污染物质,该反应的离子方程式为
等无污染物质,该反应的离子方程式为___________ 。
(2)进水 对氨氮去除率和出水pH的影响分别如图1和图2所示:
对氨氮去除率和出水pH的影响分别如图1和图2所示:

图1 图2
①进水 在1.25~2.75范围内时,氨氮去除率随
在1.25~2.75范围内时,氨氮去除率随 的升高迅速下降的原因是
的升高迅速下降的原因是__________ 。
②进水 在2.75~6范围内时,氨氮去除率随
在2.75~6范围内时,氨氮去除率随 的升高而上升的原因是
的升高而上升的原因是___________ 。
③进水 应控制在
应控制在____________ 左右为宜。
(3)为研究空气对 氢化氨氮的影响,其他条件不变,仅增加单位时间内通入空气的量,发现氨氮去除率几乎不变。其原因可能是
氢化氨氮的影响,其他条件不变,仅增加单位时间内通入空气的量,发现氨氮去除率几乎不变。其原因可能是______ (填序号)
a. 的氧化性比
的氧化性比 弱
弱
b. 氧化氨氮速率比
氧化氨氮速率比 慢
慢
c. 在废水中溶解度比较小
在废水中溶解度比较小
d.空气中的 进入废水中
进入废水中
 和
和 )会导致水体富营养化。某科研小组用
)会导致水体富营养化。某科研小组用 氧化法处理氨氮废水。已知:①
氧化法处理氨氮废水。已知:① 的氧化性比
的氧化性比 强;②
强;② 比
比 更易被氧化;③国家相关标准要求经处理过的氨氮废水
更易被氧化;③国家相关标准要求经处理过的氨氮废水 要控制在6~9。
要控制在6~9。(1)
 时,
时, 可与
可与 反应生成
反应生成 等无污染物质,该反应的离子方程式为
等无污染物质,该反应的离子方程式为(2)进水
 对氨氮去除率和出水pH的影响分别如图1和图2所示:
对氨氮去除率和出水pH的影响分别如图1和图2所示:
图1 图2
①进水
 在1.25~2.75范围内时,氨氮去除率随
在1.25~2.75范围内时,氨氮去除率随 的升高迅速下降的原因是
的升高迅速下降的原因是②进水
 在2.75~6范围内时,氨氮去除率随
在2.75~6范围内时,氨氮去除率随 的升高而上升的原因是
的升高而上升的原因是③进水
 应控制在
应控制在(3)为研究空气对
 氢化氨氮的影响,其他条件不变,仅增加单位时间内通入空气的量,发现氨氮去除率几乎不变。其原因可能是
氢化氨氮的影响,其他条件不变,仅增加单位时间内通入空气的量,发现氨氮去除率几乎不变。其原因可能是a.
 的氧化性比
的氧化性比 弱
弱b.
 氧化氨氮速率比
氧化氨氮速率比 慢
慢c.
 在废水中溶解度比较小
在废水中溶解度比较小d.空气中的
 进入废水中
进入废水中
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】Ⅰ.完成下列问题
(1)有下列物质①Cu②液氨③ ④
④ ⑤
⑤ ⑥熔融NaCl⑦
⑥熔融NaCl⑦ ⑧
⑧ ⑨
⑨ 属于弱电解质的是
属于弱电解质的是_______ (填序号)。
(2)常温下,相同物质的量浓度的上述⑦ ⑧
⑧ ⑨
⑨ 三种溶液,
三种溶液, 由大到小的顺序是
由大到小的顺序是_______ (填序号)。
Ⅱ.电离平衡常数是衡量弱电解质电离程度强弱的量,下表中给出几种弱电解质的电离平衡常数。
(3)从表中数据可以判断:在相同温度下,将pH相同的HCN、 、
、 溶液分别稀释100倍,pH变化最小的是
溶液分别稀释100倍,pH变化最小的是_______ (填化学式)。
(4)盐类水解程度的强弱同样与弱电解质的电离程度有一定联系,结合表中数据回答下列问题:
①25℃时,有等浓度的a.NaCN溶液b. 溶液c.
溶液c. 溶液,三种溶液的pH由大到小的顺序为
溶液,三种溶液的pH由大到小的顺序为_______ 。(填溶液前序号)
②25℃时,pH=10的 溶液中,由水电离出来的
溶液中,由水电离出来的
_______ mol/L。
③浓度相同的NaCN溶液与 溶液相比,
溶液相比,
_______ 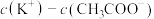 。(填“>”“<”或“=”)
。(填“>”“<”或“=”)
(5)结合表中数据,向NaCN溶液中通入少量 ,所发生反应的化学方程式
,所发生反应的化学方程式_______ 。
(1)有下列物质①Cu②液氨③
 ④
④ ⑤
⑤ ⑥熔融NaCl⑦
⑥熔融NaCl⑦ ⑧
⑧ ⑨
⑨ 属于弱电解质的是
属于弱电解质的是(2)常温下,相同物质的量浓度的上述⑦
 ⑧
⑧ ⑨
⑨ 三种溶液,
三种溶液, 由大到小的顺序是
由大到小的顺序是Ⅱ.电离平衡常数是衡量弱电解质电离程度强弱的量,下表中给出几种弱电解质的电离平衡常数。
| 化学式 |  | HCN |  |  |
| 电离平衡常数(25℃) | 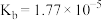 |  |  |   |
 、
、 溶液分别稀释100倍,pH变化最小的是
溶液分别稀释100倍,pH变化最小的是(4)盐类水解程度的强弱同样与弱电解质的电离程度有一定联系,结合表中数据回答下列问题:
①25℃时,有等浓度的a.NaCN溶液b.
 溶液c.
溶液c. 溶液,三种溶液的pH由大到小的顺序为
溶液,三种溶液的pH由大到小的顺序为②25℃时,pH=10的
 溶液中,由水电离出来的
溶液中,由水电离出来的
③浓度相同的NaCN溶液与
 溶液相比,
溶液相比,
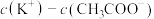 。(填“>”“<”或“=”)
。(填“>”“<”或“=”)(5)结合表中数据,向NaCN溶液中通入少量
 ,所发生反应的化学方程式
,所发生反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】铌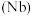 、钽
、钽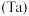 为同族元素,在航空航天、武器装备等领域发挥着重要作用.以含铌、钽的尾矿(主要成分
为同族元素,在航空航天、武器装备等领域发挥着重要作用.以含铌、钽的尾矿(主要成分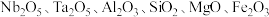 等)为原料制备
等)为原料制备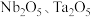 的工艺流程如下:
的工艺流程如下: ;
; 。
。
②“转化”步骤中 分别转化成氟铌酸根
分别转化成氟铌酸根 、氟钽酸根
、氟钽酸根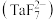 。
。
回答下列问题:
(1)“滤液1”中的主要成分为_______________________ (填化学式);
(2)“盐酸预洗”的目的是_______________________ ;
(3)①“转化”步骤中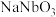 转化为
转化为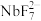 的离子方程式为
的离子方程式为_______________________ ;
②“转化”步骤在 、硫酸酸化下完成,反应速率方程为:
、硫酸酸化下完成,反应速率方程为: .
. 的作用是
的作用是_______________________ ;不能用盐酸代替 的理由是:
的理由是:_______________________ ;
(4)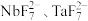 能被不同的有机溶剂选择性地萃取而与杂质分离,水相1和水相2中加入硫酸可以回收利用
能被不同的有机溶剂选择性地萃取而与杂质分离,水相1和水相2中加入硫酸可以回收利用________ (填化学式),“调节 ”步骤得到的沉淀是铌、钽的氢氧化物,煅烧氢氧化钽发生的反应方程式为
”步骤得到的沉淀是铌、钽的氢氧化物,煅烧氢氧化钽发生的反应方程式为_________ 。
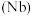 、钽
、钽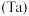 为同族元素,在航空航天、武器装备等领域发挥着重要作用.以含铌、钽的尾矿(主要成分
为同族元素,在航空航天、武器装备等领域发挥着重要作用.以含铌、钽的尾矿(主要成分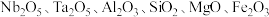 等)为原料制备
等)为原料制备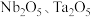 的工艺流程如下:
的工艺流程如下: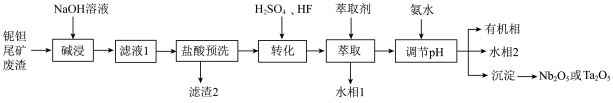
 ;
; 。
。②“转化”步骤中
 分别转化成氟铌酸根
分别转化成氟铌酸根 、氟钽酸根
、氟钽酸根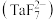 。
。回答下列问题:
(1)“滤液1”中的主要成分为
(2)“盐酸预洗”的目的是
(3)①“转化”步骤中
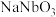 转化为
转化为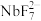 的离子方程式为
的离子方程式为②“转化”步骤在
 、硫酸酸化下完成,反应速率方程为:
、硫酸酸化下完成,反应速率方程为: .
. 的作用是
的作用是 的理由是:
的理由是:(4)
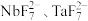 能被不同的有机溶剂选择性地萃取而与杂质分离,水相1和水相2中加入硫酸可以回收利用
能被不同的有机溶剂选择性地萃取而与杂质分离,水相1和水相2中加入硫酸可以回收利用 ”步骤得到的沉淀是铌、钽的氢氧化物,煅烧氢氧化钽发生的反应方程式为
”步骤得到的沉淀是铌、钽的氢氧化物,煅烧氢氧化钽发生的反应方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】四钼酸铵是钼深加工的重要中间产品具有广泛的用途。一种以钼精矿(主要含 ,还有
,还有 、
、 的化合物及
的化合物及 等)为原料制备四钼酸铵的工艺流程如下图所示。
等)为原料制备四钼酸铵的工艺流程如下图所示。

回答下列问题:
(1)“焙烧”产生的气体用_______ 吸收后可制取氮肥。
(2)“浸出”时, 转化为
转化为 。提高单位时间内钼浸出率的措施有
。提高单位时间内钼浸出率的措施有_______ (任写两种)。温度对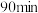 内钼浸出率的影响如图所示。当浸出温度超过
内钼浸出率的影响如图所示。当浸出温度超过 后,钼的浸出率反而降低,主要原因是温度升高使水大量蒸发,导致
后,钼的浸出率反而降低,主要原因是温度升高使水大量蒸发,导致_______ 。

(3)“净化”时,加(NH4)2S净化,滤渣为_______ 。
(4)“净化”后,溶液中若有低价钼(以 表示),可加入适量
表示),可加入适量 将其氧化为
将其氧化为 ,反应的离子方程式为
,反应的离子方程式为_______ 。
(5)“沉淀”时,加入 的目的是
的目的是_______ 。
(6)高温下用H2还原(NH4)2Mo4O13可制得金属钼,反应的化学方程式为_______ 。【已知:(NH4)2Mo4O13受热分解生成 】
】
 ,还有
,还有 、
、 的化合物及
的化合物及 等)为原料制备四钼酸铵的工艺流程如下图所示。
等)为原料制备四钼酸铵的工艺流程如下图所示。
回答下列问题:
(1)“焙烧”产生的气体用
(2)“浸出”时,
 转化为
转化为 。提高单位时间内钼浸出率的措施有
。提高单位时间内钼浸出率的措施有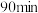 内钼浸出率的影响如图所示。当浸出温度超过
内钼浸出率的影响如图所示。当浸出温度超过 后,钼的浸出率反而降低,主要原因是温度升高使水大量蒸发,导致
后,钼的浸出率反而降低,主要原因是温度升高使水大量蒸发,导致
(3)“净化”时,加(NH4)2S净化,滤渣为
(4)“净化”后,溶液中若有低价钼(以
 表示),可加入适量
表示),可加入适量 将其氧化为
将其氧化为 ,反应的离子方程式为
,反应的离子方程式为(5)“沉淀”时,加入
 的目的是
的目的是(6)高温下用H2还原(NH4)2Mo4O13可制得金属钼,反应的化学方程式为
 】
】
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】2019年诺贝尔化学奖授予约翰·古迪纳夫、斯坦利·威廷汉和吉野彰,表彰他们对锂离子电池研究的贡献。磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。采用湿法治金工艺回收废旧磷酸亚铁锂电池正极片(除LiFePO4外,还含有Al箔、少量不溶于酸碱的导电剂)中的资源,部分流程如图:

(1)从“正极”可以回收的金属有___________ 。
(2)“碱溶”时Al箔溶解的离子方程式_________ 。
(3)“酸浸”时产生标准状况下2.24L NO时,则被氧化的LiFePO4为______ mol。(其他杂质不与HNO3反应)
(4)实验测得滤液②中c(Li+)=4 mol·L-1,加入等体积的Na2CO3溶液后,Li+的沉降率到99%,则滤液③中c(CO32-)=________ mol·L-1。 [Ksp(Li2CO3)=1.6×10-3]
(5)磷酸亚铁锂电池总反应为:LiFePO4+6C Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。充电时,Li+移向
Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。充电时,Li+移向_______ (填“阳极”或“阴极”);放电时,正极反应式为_______ 。
(6)磷酸亚铁锂电池中铁的含量可通过如下方法测定:称取1.40g试样用盐酸溶解,在溶液中加入稍过量的SnCl2溶液,再加入HgCl2饱和溶液,用二苯胺磺酸钠作指示剂,用0.030 mol·L-1重铬酸钾溶液滴定至溶液由浅绿色变为蓝紫色,消耗重铬酸钾溶液40.00mL。
已知:2Fe3++Sn2++6Cl-=SnCl62-+2Fe2+
4Cl-+Sn2++2HgCl2=SnCl62-+Hg2Cl2
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
① 实验中加入HgCl2饱和溶液的目的是__________ 。
② 磷酸亚铁锂电池中铁的含量为_______ 。

(1)从“正极”可以回收的金属有
(2)“碱溶”时Al箔溶解的离子方程式
(3)“酸浸”时产生标准状况下2.24L NO时,则被氧化的LiFePO4为
(4)实验测得滤液②中c(Li+)=4 mol·L-1,加入等体积的Na2CO3溶液后,Li+的沉降率到99%,则滤液③中c(CO32-)=
(5)磷酸亚铁锂电池总反应为:LiFePO4+6C
 Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。充电时,Li+移向
Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。充电时,Li+移向(6)磷酸亚铁锂电池中铁的含量可通过如下方法测定:称取1.40g试样用盐酸溶解,在溶液中加入稍过量的SnCl2溶液,再加入HgCl2饱和溶液,用二苯胺磺酸钠作指示剂,用0.030 mol·L-1重铬酸钾溶液滴定至溶液由浅绿色变为蓝紫色,消耗重铬酸钾溶液40.00mL。
已知:2Fe3++Sn2++6Cl-=SnCl62-+2Fe2+
4Cl-+Sn2++2HgCl2=SnCl62-+Hg2Cl2
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
① 实验中加入HgCl2饱和溶液的目的是
② 磷酸亚铁锂电池中铁的含量为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】氯化铈是冶炼稀土金属、稀土合金的重要原料。为节约和充分利用资源,以某废料(主要含 ,还含少量的
,还含少量的 )为原料,通过如图1所示工艺流程制备氯化铈。
)为原料,通过如图1所示工艺流程制备氯化铈。

已知:a、 具有强氧化性,通常情况下不和无机酸反应。
具有强氧化性,通常情况下不和无机酸反应。
b、常温下, ,
, 。
。
回答下列问题:
(1)为加快“酸浸1”的速率,可采取的措施是___________ (写一条即可)。
(2)“浸液A”中存在的金属阳离子为___________ (填离子符号),“浸渣A”的主要成分为___________ (填化学式),“浸渣B”的主要用途为___________ (写出一种)。
(3)“酸浸2”中 的浸出率与
的浸出率与 、温度的变化关系如图2所示,应选择的适宜条件是___________(填标号)。
、温度的变化关系如图2所示,应选择的适宜条件是___________(填标号)。

(4)“酸溶”过程中加入盐酸后,通常还需加入 ,其主要目的为
,其主要目的为___________ 。
(5)“沉铈2”过程中生成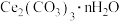 的离子方程式为
的离子方程式为___________ 。若 恰好沉淀完全
恰好沉淀完全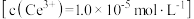 ,此时测得溶液的
,此时测得溶液的 ,则溶液中
,则溶液中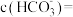
___________  。
。
 ,还含少量的
,还含少量的 )为原料,通过如图1所示工艺流程制备氯化铈。
)为原料,通过如图1所示工艺流程制备氯化铈。
已知:a、
 具有强氧化性,通常情况下不和无机酸反应。
具有强氧化性,通常情况下不和无机酸反应。b、常温下,
 ,
, 。
。回答下列问题:
(1)为加快“酸浸1”的速率,可采取的措施是
(2)“浸液A”中存在的金属阳离子为
(3)“酸浸2”中
 的浸出率与
的浸出率与 、温度的变化关系如图2所示,应选择的适宜条件是___________(填标号)。
、温度的变化关系如图2所示,应选择的适宜条件是___________(填标号)。
A. | B. | C.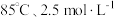 | D.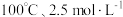 |
 ,其主要目的为
,其主要目的为(5)“沉铈2”过程中生成
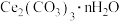 的离子方程式为
的离子方程式为 恰好沉淀完全
恰好沉淀完全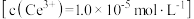 ,此时测得溶液的
,此时测得溶液的 ,则溶液中
,则溶液中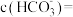
 。
。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】微型实验具有设计简单、节约药品等优点,某化学活动小组利用所学知识设计氯气制备和性质实验如下。回答下列问题:
I.氯气的制备:
(1)若实验室用2KMn04+16HCl(浓)=2KCl+2MnCl2+5Cl+8H2O制取少量氯气,则反应的最佳装置应选用下图中____________ 。
(2)利用下图装置收集纯净的氯气,其连接顺序为:发生装置
________ (按气流方向,用字母表示)。
(3)A、B两组同学分别用两种方法制取氯气,A组用含146g HCl的浓盐酸与足量的二氧化锰反应;B组用87g二氧化锰与足量的浓盐酸反应,则所得氯气的物质的量的关系为A______ B(填“>”、“<”或“=”)
Ⅱ.氯气微型实验:
(1)根据图示,完成下表
(2)仔细观察上述装置,利用该套装置_____ (填“能”或“不能”)证明溴单质的氧化性大于碘,若能应如何操作(若不能请解释为什么?)_________ 。
I.氯气的制备:
(1)若实验室用2KMn04+16HCl(浓)=2KCl+2MnCl2+5Cl+8H2O制取少量氯气,则反应的最佳装置应选用下图中
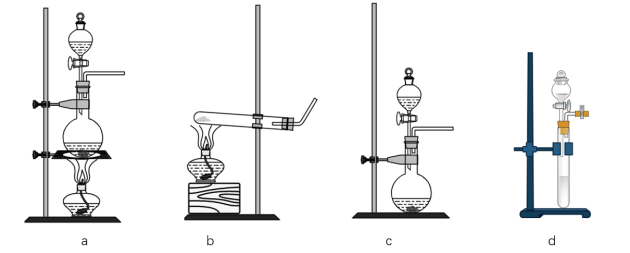
(2)利用下图装置收集纯净的氯气,其连接顺序为:发生装置

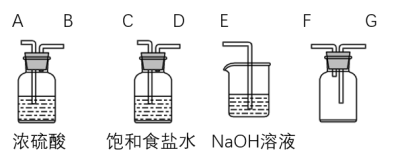
(3)A、B两组同学分别用两种方法制取氯气,A组用含146g HCl的浓盐酸与足量的二氧化锰反应;B组用87g二氧化锰与足量的浓盐酸反应,则所得氯气的物质的量的关系为A
Ⅱ.氯气微型实验:
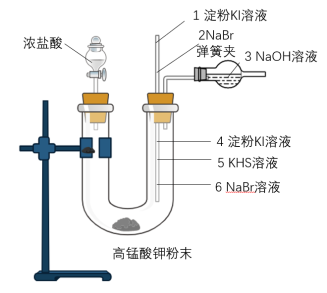
(1)根据图示,完成下表
| 位置 | 实验现象 | 解释原因 |
| 6 | 溶液变黄色 | 反应的离子方程式 |
| 5 | Cl2+HS-=2Cl-+S↓+H+ | |
| 4 | 氯气的氧化性大于碘单质 |
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】铍可应用于飞机、火箭制造业和原子能工业。素有“中国铍业一枝花”之称的湖南水口山六厂改进国外生产工艺,以硅铍石(主要成分为 、
、 、
、 、
、 、
、 )为原料提取铍,具体流程如下:
)为原料提取铍,具体流程如下:
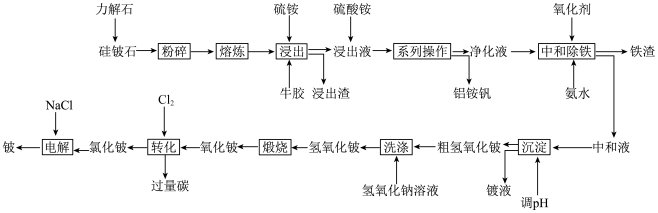
已知:①铍和铝在元素周期表中处于对角线位置,电负性相近,其单质及化合物在结构与性质等方面具有相似性。
②铝铵钒在不同温度下的溶解度:
回答下列问题:
(1)流程中“系列操作”为___________ 。
(2)将“中和液”沉淀时,调节溶液的 不能过大或过小。
不能过大或过小。 过大时发生反应的离子方程式为
过大时发生反应的离子方程式为___________ 。
(3)已知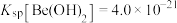 ,
,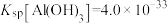 。若
。若 浓度为0.40
浓度为0.40 的中和液开始沉淀时,溶液中
的中和液开始沉淀时,溶液中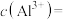
___________  。
。
(4)若在实验室洗涤粗 ,操作为
,操作为___________ ;洗涤时加入 溶液除去表面吸附的少量氢氧化铝,反应的离子方程式为
溶液除去表面吸附的少量氢氧化铝,反应的离子方程式为___________ 。
(5)氧化铍转化为氯化铍的化学方程式为___________ 。
(6) 的电子式为
的电子式为___________ ;电解时须加入氯化钠的作用是___________ 。
 、
、 、
、 、
、 、
、 )为原料提取铍,具体流程如下:
)为原料提取铍,具体流程如下:
已知:①铍和铝在元素周期表中处于对角线位置,电负性相近,其单质及化合物在结构与性质等方面具有相似性。
②铝铵钒在不同温度下的溶解度:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 |
| 溶解度/g | 2.10 | 5.00 | 7.74 | 10.9 | 14.9 | 26.7 |
(1)流程中“系列操作”为
(2)将“中和液”沉淀时,调节溶液的
 不能过大或过小。
不能过大或过小。 过大时发生反应的离子方程式为
过大时发生反应的离子方程式为(3)已知
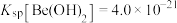 ,
,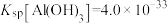 。若
。若 浓度为0.40
浓度为0.40 的中和液开始沉淀时,溶液中
的中和液开始沉淀时,溶液中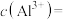
 。
。(4)若在实验室洗涤粗
 ,操作为
,操作为 溶液除去表面吸附的少量氢氧化铝,反应的离子方程式为
溶液除去表面吸附的少量氢氧化铝,反应的离子方程式为(5)氧化铍转化为氯化铍的化学方程式为
(6)
 的电子式为
的电子式为
您最近一年使用:0次



