2020届高三化学二轮选修大题必练 — ——以“化工流程”为载体的综合实验
全国
高三
专题练习
2020-01-11
62次
整体难度:
适中
考查范围:
认识化学科学、化学反应原理、常见无机物及其应用、化学实验基础、有机化学基础
2020届高三化学二轮选修大题必练 — ——以“化工流程”为载体的综合实验
全国
高三
专题练习
2020-01-11
62次
整体难度:
适中
考查范围:
认识化学科学、化学反应原理、常见无机物及其应用、化学实验基础、有机化学基础
一、解答题 添加题型下试题
解答题-工业流程题
|
较难(0.4)
1. 工业生产中产生的 、NO直接排放将对大气造成严重污染,利用电化学原理吸收
、NO直接排放将对大气造成严重污染,利用电化学原理吸收 和NO,同时获得
和NO,同时获得 和
和 产品的工艺流程图如下
产品的工艺流程图如下 为铈元素
为铈元素 。
。

请回答下列问题.
 若装置Ⅱ中反应生成的含氮化合物的物质的量比为1:1,则该反应的离子方程式
若装置Ⅱ中反应生成的含氮化合物的物质的量比为1:1,则该反应的离子方程式____ 。
 含硫各微粒
含硫各微粒 、
、 和
和 存在于
存在于 与NaOH溶液反应后的溶液中,它们的物质的量分数
与NaOH溶液反应后的溶液中,它们的物质的量分数 与溶液pH的关系如图所示。
与溶液pH的关系如图所示。
 下列说法中正确的是
下列说法中正确的是______  填标号
填标号 。
。
A. 溶液中滴加氯水可以使
溶液中滴加氯水可以使 的值变大
的值变大
B. 时,溶液中
时,溶液中
C. 时的溶液中
时的溶液中
D.由图中数据,可以估算出 的第二级电离平衡常数
的第二级电离平衡常数
E.由图中数据, 和
和 时的溶液中水的电离程度相同
时的溶液中水的电离程度相同
 若利用氨水吸收二氧化硫,其相关反应的主要热化学方程式如下:
若利用氨水吸收二氧化硫,其相关反应的主要热化学方程式如下:







反应
___  。
。
 取装置Ⅰ中的吸收液VmL,用
取装置Ⅰ中的吸收液VmL,用 的酸性高锰酸钾溶液滴定.吸收液溶液应装在
的酸性高锰酸钾溶液滴定.吸收液溶液应装在______  填“酸式”或“碱式”
填“酸式”或“碱式” 滴定管中,判断滴定终点的方法
滴定管中,判断滴定终点的方法______ 。
 装置Ⅲ的作用之一是再生
装置Ⅲ的作用之一是再生 ,其原理如图所示,图中B为电源的
,其原理如图所示,图中B为电源的______  填“正”或“负”
填“正”或“负” 极,左侧反应室中发生的主要电极反应式为
极,左侧反应室中发生的主要电极反应式为______ 。

 已知进入装置Ⅳ的溶液中
已知进入装置Ⅳ的溶液中 的浓度为
的浓度为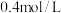 ,要使
,要使 该溶液中的
该溶液中的 完全转化为
完全转化为 ,该过程中转移电子数目为
,该过程中转移电子数目为______ 。
 、NO直接排放将对大气造成严重污染,利用电化学原理吸收
、NO直接排放将对大气造成严重污染,利用电化学原理吸收 和NO,同时获得
和NO,同时获得 和
和 产品的工艺流程图如下
产品的工艺流程图如下 为铈元素
为铈元素 。
。
请回答下列问题.
 若装置Ⅱ中反应生成的含氮化合物的物质的量比为1:1,则该反应的离子方程式
若装置Ⅱ中反应生成的含氮化合物的物质的量比为1:1,则该反应的离子方程式 含硫各微粒
含硫各微粒 、
、 和
和 存在于
存在于 与NaOH溶液反应后的溶液中,它们的物质的量分数
与NaOH溶液反应后的溶液中,它们的物质的量分数 与溶液pH的关系如图所示。
与溶液pH的关系如图所示。
 下列说法中正确的是
下列说法中正确的是 填标号
填标号 。
。A.
 溶液中滴加氯水可以使
溶液中滴加氯水可以使 的值变大
的值变大B.
 时,溶液中
时,溶液中
C.
 时的溶液中
时的溶液中
D.由图中数据,可以估算出
 的第二级电离平衡常数
的第二级电离平衡常数
E.由图中数据,
 和
和 时的溶液中水的电离程度相同
时的溶液中水的电离程度相同 若利用氨水吸收二氧化硫,其相关反应的主要热化学方程式如下:
若利用氨水吸收二氧化硫,其相关反应的主要热化学方程式如下:






反应

 。
。 取装置Ⅰ中的吸收液VmL,用
取装置Ⅰ中的吸收液VmL,用 的酸性高锰酸钾溶液滴定.吸收液溶液应装在
的酸性高锰酸钾溶液滴定.吸收液溶液应装在 填“酸式”或“碱式”
填“酸式”或“碱式” 滴定管中,判断滴定终点的方法
滴定管中,判断滴定终点的方法 装置Ⅲ的作用之一是再生
装置Ⅲ的作用之一是再生 ,其原理如图所示,图中B为电源的
,其原理如图所示,图中B为电源的 填“正”或“负”
填“正”或“负” 极,左侧反应室中发生的主要电极反应式为
极,左侧反应室中发生的主要电极反应式为
 已知进入装置Ⅳ的溶液中
已知进入装置Ⅳ的溶液中 的浓度为
的浓度为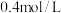 ,要使
,要使 该溶液中的
该溶液中的 完全转化为
完全转化为 ,该过程中转移电子数目为
,该过程中转移电子数目为
您最近一年使用:0次
解答题-工业流程题
|
较难(0.4)
2. 石棉尾矿主要含有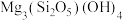 和少量的
和少量的 、
、 以石棉尾矿为镁源制备碳酸镁晶体
以石棉尾矿为镁源制备碳酸镁晶体 的工艺如下:
的工艺如下:

已知“焙烧”过程中的主反应为:
(1)写出焙烧产物 的电子式
的电子式______ 。
(2)为提高水浸速率,可采取的措施为______  任写一条
任写一条 ,“浸渣”的主要成分为
,“浸渣”的主要成分为____ 。
(3)“调节pH除杂”时,需将pH调至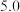 ,则除去的杂质离子是
,则除去的杂质离子是______ ,此时溶液中的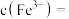
______  已知
已知 。
。
(4)“沉镁”过程中反应的离子方程式为______ 。
“沉镁”时若温度超过 ,将产生较多的碱式碳酸镁杂质,原因是
,将产生较多的碱式碳酸镁杂质,原因是______
(5)流程中可以循环利用的物质是______  填化学式
填化学式 。
。
(6)某小组同学称取
 进行热重分析,并绘制剩余固体质量随温度变化的曲线如图所示,则
进行热重分析,并绘制剩余固体质量随温度变化的曲线如图所示,则
______ 。
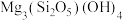 和少量的
和少量的 、
、 以石棉尾矿为镁源制备碳酸镁晶体
以石棉尾矿为镁源制备碳酸镁晶体 的工艺如下:
的工艺如下:
已知“焙烧”过程中的主反应为:

(1)写出焙烧产物
 的电子式
的电子式(2)为提高水浸速率,可采取的措施为
 任写一条
任写一条 ,“浸渣”的主要成分为
,“浸渣”的主要成分为(3)“调节pH除杂”时,需将pH调至
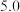 ,则除去的杂质离子是
,则除去的杂质离子是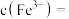
 已知
已知 。
。(4)“沉镁”过程中反应的离子方程式为
“沉镁”时若温度超过
 ,将产生较多的碱式碳酸镁杂质,原因是
,将产生较多的碱式碳酸镁杂质,原因是(5)流程中可以循环利用的物质是
 填化学式
填化学式 。
。
(6)某小组同学称取

 进行热重分析,并绘制剩余固体质量随温度变化的曲线如图所示,则
进行热重分析,并绘制剩余固体质量随温度变化的曲线如图所示,则
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
3. 铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下。
(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①该过程中涉及某氧化还原反应如下,请完成:_______ Fe2++ClO-+=Fe(OH)3↓+C1-+。
②检验滤液B中是否还含有铁元素的方法为:___________ (注明试剂、现象)。
③将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为___________ (填代号)。
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
④由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、冷却结晶、__________ (填操作名称)、洗涤。
(2)已知H2O2是一种弱酸,在强碱性溶液中主要以HO2-形式存在。目前研究比较热门的Al-H2O2燃料电池,其原理如右图所示,电池总反应如下:2Al+3HO2-=2AlO2-+OH-+H2O
①正极反应式为__________ 。
②Al电极易被NaOH溶液腐蚀,这是该电池目前未能推广使用的原因之一,电极被腐蚀的离子方程式为______________ 。
(3)钢材镀铝可以防止钢材腐蚀,在镀铝电解池中电解液采用熔融盐(成分NaCl、KCl,电镀时氯元素和铝元素主要以AlCl4-形式存在)。不采用氯化铝溶液的原因是____________ 。
(4)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为___________ (填代号)。
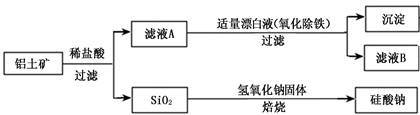
(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①该过程中涉及某氧化还原反应如下,请完成:
②检验滤液B中是否还含有铁元素的方法为:
③将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
④由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、冷却结晶、
(2)已知H2O2是一种弱酸,在强碱性溶液中主要以HO2-形式存在。目前研究比较热门的Al-H2O2燃料电池,其原理如右图所示,电池总反应如下:2Al+3HO2-=2AlO2-+OH-+H2O

①正极反应式为
②Al电极易被NaOH溶液腐蚀,这是该电池目前未能推广使用的原因之一,电极被腐蚀的离子方程式为
(3)钢材镀铝可以防止钢材腐蚀,在镀铝电解池中电解液采用熔融盐(成分NaCl、KCl,电镀时氯元素和铝元素主要以AlCl4-形式存在)。不采用氯化铝溶液的原因是
(4)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为

您最近一年使用:0次
解答题-工业流程题
|
较难(0.4)
4. 为了降低电子垃圾对环境构成的影响,将一批废弃的线路板简单处理后,得到含 、
、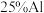 、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:

 第
第 步Cu与混酸反应的离子方程式为
步Cu与混酸反应的离子方程式为______  得到滤渣1的主要成分为
得到滤渣1的主要成分为______ 。
 第
第 步中加入
步中加入 的作用是
的作用是______ ,使用 的优点是
的优点是______ ;调溶液pH的目的是______ 。
 简述第
简述第 步由滤液2得到
步由滤液2得到 的方法是
的方法是______ 。
 由滤渣2制取
由滤渣2制取 ,设计了以下三种方案:
,设计了以下三种方案:
甲:滤渣 酸浸液
酸浸液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O
乙:滤渣 酸浸液
酸浸液 滤液
滤液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O
丙:滤渣2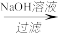 滤液
滤液 溶液
溶液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O
上述三种方案中,______ 方案不可行,原因是______ ;从原子利用率角度考虑,______ 方案更合理。
 用滴定法测定
用滴定法测定 含量.取a g试样配成100mL溶液,每次取
含量.取a g试样配成100mL溶液,每次取 ,消除干扰离子后,用c
,消除干扰离子后,用c
 标准溶液滴定至终点,平均消耗EDTA溶液b
标准溶液滴定至终点,平均消耗EDTA溶液b  滴定反应如下:
滴定反应如下: 写出计算
写出计算 质量分数的表达式
质量分数的表达式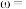
______ 。
 、
、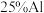 、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
| 方法Ⅰ | 用炭粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法:  |
| 方法Ⅲ | 用肼 还原新制 还原新制 |
 第
第 步Cu与混酸反应的离子方程式为
步Cu与混酸反应的离子方程式为 得到滤渣1的主要成分为
得到滤渣1的主要成分为 第
第 步中加入
步中加入 的作用是
的作用是 的优点是
的优点是 简述第
简述第 步由滤液2得到
步由滤液2得到 的方法是
的方法是 由滤渣2制取
由滤渣2制取 ,设计了以下三种方案:
,设计了以下三种方案:甲:滤渣
 酸浸液
酸浸液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O乙:滤渣
 酸浸液
酸浸液 滤液
滤液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O丙:滤渣2
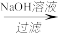 滤液
滤液 溶液
溶液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O上述三种方案中,
 用滴定法测定
用滴定法测定 含量.取a g试样配成100mL溶液,每次取
含量.取a g试样配成100mL溶液,每次取 ,消除干扰离子后,用c
,消除干扰离子后,用c
 标准溶液滴定至终点,平均消耗EDTA溶液b
标准溶液滴定至终点,平均消耗EDTA溶液b  滴定反应如下:
滴定反应如下: 写出计算
写出计算 质量分数的表达式
质量分数的表达式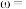
您最近一年使用:0次
解答题-工业流程题
|
较难(0.4)
5. 工业上以铬铁矿 主要成分为
主要成分为 ,还含有
,还含有 、
、 等杂质
等杂质 为主要原料生产红矾钠晶体
为主要原料生产红矾钠晶体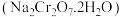 ,其主要工艺流程如图:
,其主要工艺流程如图:

已知: 在碱性条件下能将
在碱性条件下能将 氧化为
氧化为 。
。
 固体A为
固体A为 ______ 。
 实验室中操作
实验室中操作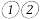 的名称为
的名称为_____________ 。
 固体C中含有的物质是
固体C中含有的物质是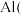
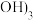 和
和 ,则
,则 的作用是
的作用是 ______ 。
已知: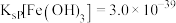 ,
, ,当
,当 时
时 开始沉淀.室温下,Ⅱ中需调节溶液pH范围为
开始沉淀.室温下,Ⅱ中需调节溶液pH范围为 ___  杂质离子浓度小于
杂质离子浓度小于 视为沉淀完全
视为沉淀完全 。
。
 写出Ⅲ中发生反应的离子方程式
写出Ⅲ中发生反应的离子方程式 ______ 。
 Ⅳ中酸化是用硫酸而不用盐酸酸化,理由是
Ⅳ中酸化是用硫酸而不用盐酸酸化,理由是 ______  结合化学方程式回答
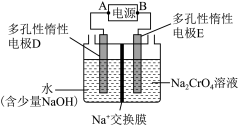
结合化学方程式回答 ;工业上也可设计如图示装置,用锂离子电池
;工业上也可设计如图示装置,用锂离子电池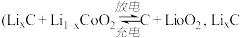 为难电离锂碳化合物
为难电离锂碳化合物 为电源,电解
为电源,电解 溶液制取
溶液制取 ,该装置工作时E电极的名称是
,该装置工作时E电极的名称是 ___ 极;电源的A极的电极反应式为 ______  当电解过程中转移了
当电解过程中转移了 电子时,理论上右侧溶液的质量减少
电子时,理论上右侧溶液的质量减少 ______ g。
 主要成分为
主要成分为 ,还含有
,还含有 、
、 等杂质
等杂质 为主要原料生产红矾钠晶体
为主要原料生产红矾钠晶体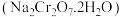 ,其主要工艺流程如图:
,其主要工艺流程如图:
已知:
 在碱性条件下能将
在碱性条件下能将 氧化为
氧化为 。
。 固体A为
固体A为  实验室中操作
实验室中操作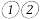 的名称为
的名称为 固体C中含有的物质是
固体C中含有的物质是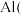
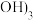 和
和 ,则
,则 的作用是
的作用是 已知:
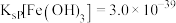 ,
, ,当
,当 时
时 开始沉淀.室温下,Ⅱ中需调节溶液pH范围为
开始沉淀.室温下,Ⅱ中需调节溶液pH范围为  杂质离子浓度小于
杂质离子浓度小于 视为沉淀完全
视为沉淀完全 。
。 写出Ⅲ中发生反应的离子方程式
写出Ⅲ中发生反应的离子方程式  Ⅳ中酸化是用硫酸而不用盐酸酸化,理由是
Ⅳ中酸化是用硫酸而不用盐酸酸化,理由是  结合化学方程式回答
结合化学方程式回答 ;工业上也可设计如图示装置,用锂离子电池
;工业上也可设计如图示装置,用锂离子电池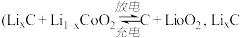 为难电离锂碳化合物
为难电离锂碳化合物 为电源,电解
为电源,电解 溶液制取
溶液制取 ,该装置工作时E电极的名称是
,该装置工作时E电极的名称是  当电解过程中转移了
当电解过程中转移了 电子时,理论上右侧溶液的质量减少
电子时,理论上右侧溶液的质量减少 
您最近一年使用:0次
解答题-工业流程题
|
较难(0.4)
6. 以菱镁矿 主要成分为
主要成分为 ,含少量
,含少量
 为原料制备高纯氧化镁的实验流程如下:
为原料制备高纯氧化镁的实验流程如下:

 滤液P中含有的阳离子有
滤液P中含有的阳离子有 ______ 。
 过程Ⅱ中发生的氧化还原反应的离子方程式是
过程Ⅱ中发生的氧化还原反应的离子方程式是 ______ 。
 已知:
已知:
过程Ⅲ中加入 调节溶液pH约为4,其目的是
调节溶液pH约为4,其目的是 ______ 。
 过程Ⅳ在
过程Ⅳ在 煅烧
煅烧 ,发生多个反应,产物除MgO外,还有
,发生多个反应,产物除MgO外,还有 、
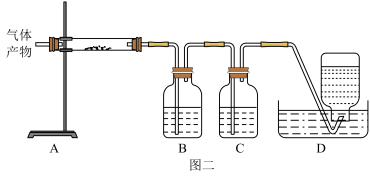
、 、CO、S等气体产物,利用右图装置判断煅烧产生的气体。
、CO、S等气体产物,利用右图装置判断煅烧产生的气体。
 中试管壁附着有淡黄色固体,该固体的化学式是
中试管壁附着有淡黄色固体,该固体的化学式是 ______ 。
 中盛放的溶液是
中盛放的溶液是 填字母
填字母
______ 。
 溶液
溶液  溶液
溶液  稀硝酸
稀硝酸  溶液
溶液
 写出
写出 煅烧
煅烧 ,产生气体产物是S 和CO的化学方程式
,产生气体产物是S 和CO的化学方程式 ______ 。
 主要成分为
主要成分为 ,含少量
,含少量
 为原料制备高纯氧化镁的实验流程如下:
为原料制备高纯氧化镁的实验流程如下: 

 滤液P中含有的阳离子有
滤液P中含有的阳离子有  过程Ⅱ中发生的氧化还原反应的离子方程式是
过程Ⅱ中发生的氧化还原反应的离子方程式是  已知:
已知:  |  |  | |
| 开始沉淀的pH |  | 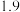 | 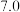 |
| 沉淀完全的pH | 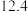 |  |  |
过程Ⅲ中加入
 调节溶液pH约为4,其目的是
调节溶液pH约为4,其目的是  过程Ⅳ在
过程Ⅳ在 煅烧
煅烧 ,发生多个反应,产物除MgO外,还有
,发生多个反应,产物除MgO外,还有 、
、 、CO、S等气体产物,利用右图装置判断煅烧产生的气体。
、CO、S等气体产物,利用右图装置判断煅烧产生的气体。 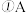 中试管壁附着有淡黄色固体,该固体的化学式是
中试管壁附着有淡黄色固体,该固体的化学式是 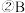 中盛放的溶液是
中盛放的溶液是 填字母
填字母
 溶液
溶液  溶液
溶液  稀硝酸
稀硝酸  溶液
溶液  写出
写出 煅烧
煅烧 ,产生气体产物是S 和CO的化学方程式
,产生气体产物是S 和CO的化学方程式
您最近一年使用:0次



