利用如图装置可以验证非金属性的变化规律。
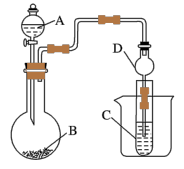
(1)仪器A的名称为________ ,干燥管D的作用是________________ 。
(2)已知在常温下,高锰酸钾和浓盐酸反应能生成氯气。实验室中现有药品Na2S溶液、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫的;装置A、B、C中所装药品分别为________ 、________ 、________ ,装置C中的实验现象为_________________ ,离子方程式为______ 。
(3)若要证明非金属性:S>C>Si,则A中加________ 、B中加Na2CO3、C中加________ 。

(1)仪器A的名称为
(2)已知在常温下,高锰酸钾和浓盐酸反应能生成氯气。实验室中现有药品Na2S溶液、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫的;装置A、B、C中所装药品分别为
(3)若要证明非金属性:S>C>Si,则A中加
19-20高一上·云南玉溪·期末 查看更多[14]
云南省玉溪市民族中学2021-2022学年高一上学期期末考试化学试题云南省曲靖市富源县第六中学2019-2020学年高一上学期期末考试化学试题贵州省罗甸县第一中学2019-2020学年高一上学期期末考试化学试题云南省昭通市彝良县一中2019—2020学年高一上学期期末考试化学试题云南省丽江市永胜县第二中学2019—2020学年高一上学期期末考试化学试题云南省普洱市景东县第二中学2019—2020学年高一上学期期末考试化学试题云南省普洱市镇沅县第一中学2019—2020学年高一上学期期末考试化学试题云南省普洱市江城县第一中学2019—2020学年高一上学期期末考试化学试题贵州省麻江县第一中学2019-2020学年高一上学期期末考试化学试题云南省盈江县民族完全中学2019-2020学年高一上学期期末考试化学试题云南省云龙县第二中学2019-2020学年高一上学期期末考试化学试题云南省迪庆州维西县第二中学2019-2020学年高一上学期期末考试化学试题云南省玉溪市通海二中2019-2020学年高一上学期期末考试化学试题云南省通海三中2019-2020学年高一上学期期末考试化学试题
更新时间:2020-01-10 10:14:50
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下表为元素周期表的一部分,参照元素①~⑧在表中的位置,用化学用语回答下列问题:

(1)④、⑤、⑦形成的简单离子的半径由大到小的顺序是____________________ 。
(2)含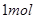 ⑦的最高价氧化物对应水化物的稀溶液与足量⑤的最高价氧化物对应水化物的稀溶液反应放出热量
⑦的最高价氧化物对应水化物的稀溶液与足量⑤的最高价氧化物对应水化物的稀溶液反应放出热量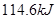 ,此反应的热化学方程式为
,此反应的热化学方程式为____________________ 。
(3)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为______________________________ 。
N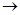 ⑥的单质的化学方程式为
⑥的单质的化学方程式为________________________________________ 。
M溶液中离子浓度由大到小的顺序为________________________________________ 。
(4)设计实验探究⑧、⑨两种元素非金属性的相对强弱。
可选用的试剂有:氯水、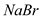 溶液、
溶液、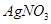 溶液、
溶液、 。
。
请完成实验报告单:

(1)④、⑤、⑦形成的简单离子的半径由大到小的顺序是
(2)含
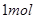 ⑦的最高价氧化物对应水化物的稀溶液与足量⑤的最高价氧化物对应水化物的稀溶液反应放出热量
⑦的最高价氧化物对应水化物的稀溶液与足量⑤的最高价氧化物对应水化物的稀溶液反应放出热量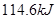 ,此反应的热化学方程式为
,此反应的热化学方程式为(3)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为
N
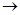 ⑥的单质的化学方程式为
⑥的单质的化学方程式为M溶液中离子浓度由大到小的顺序为
(4)设计实验探究⑧、⑨两种元素非金属性的相对强弱。
可选用的试剂有:氯水、
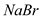 溶液、
溶液、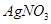 溶液、
溶液、 。
。请完成实验报告单:
| 实验内容 | 现象 |
步骤一:试管1:取少量氯水:试管2:取少量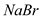 溶液,滴加少量氯水。 溶液,滴加少量氯水。 | 试管2中的现象是: |
| 步骤二:分别向试管1、试管2中加入试剂 | 试管2中的现象是 |
| ①试管1的作用是 ②实验结论是 | |
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】化学是一门以实验为基础的学科,实验是检验化学理论正确与否的试金石。根据下列问题设计合适的实验:
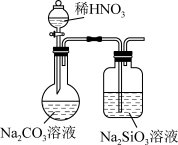
(1)某同学为验证元素N、C、Si的非金属性依次减弱,设计了如图所示装置(已略去夹持装置),有同学认为这个装置不一定能证明C与Si的非金属性强弱,原因是___________ ,改进的方法为______________________ 。
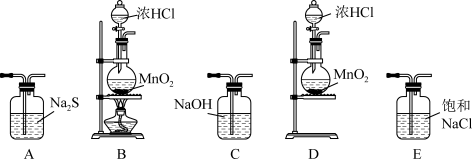
(2)若要证明非金属性:Cl>S,从下图 (仅略去夹持装置)中选取装置并按气流方向从左至右的连接顺序为___________ ,实验过程中可观察到的主要现象为___________ 。
(3)根据(2)的实验方案,某同学认为把Cl2通入NaBr溶液中可证明非金属性:Cl>Br。这种方案__________ (填“能”或“不能”)达到预期目的,用化学方程式解释其原因:___________ 。
(1)某同学为验证元素N、C、Si的非金属性依次减弱,设计了如图所示装置(已略去夹持装置),有同学认为这个装置不一定能证明C与Si的非金属性强弱,原因是

(2)若要证明非金属性:Cl>S,从下图 (仅略去夹持装置)中选取装置并按气流方向从左至右的连接顺序为

(3)根据(2)的实验方案,某同学认为把Cl2通入NaBr溶液中可证明非金属性:Cl>Br。这种方案
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某同学做同主族元素性质相似性、递变性实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
请你帮助该同学整理并完成实验报告。
(1)实验目的:_____________________ 。
(2)实验用品:
①试剂:金属钠、金属钾、新制氯水、溴水、0.1mol·L-1溴化钠溶液、0.1 mol·L-1碘化钠溶液、四氯化碳等;
②仪器:________ 、________ 、________ 、镊子、小刀、玻璃片等。
(3)实验内容(填写与实验方案对应的实验现象的标号和化学方程式):________
(4)实验结论:__________________
| 实验方案 | 实验现象 |
| ①将氯水滴加到溴化钠溶液中,振荡后加入适量CCl4液体,振荡,静置 | A.浮在水面上,熔成小球,不定向移动,随之消失 |
| ②将一小块金属钠放入冷水中 | B.分层,上层无色,下层紫红色 |
| ③将溴水滴加到NaI溶液中,振荡后加入适量CCl4液体,振荡,静置 | C.浮在水面上,熔成小球,不定向移动,并伴有轻微的爆炸声,很快消失 |
| ④将一小块金属钾放入冷水中 | D.分层,上层无色,下层棕红色 |
(1)实验目的:
(2)实验用品:
①试剂:金属钠、金属钾、新制氯水、溴水、0.1mol·L-1溴化钠溶液、0.1 mol·L-1碘化钠溶液、四氯化碳等;
②仪器:
(3)实验内容(填写与实验方案对应的实验现象的标号和化学方程式):
| 实验方案 | 实验现象 | 化学方程式 |
| ① | ||
| ② | ||
| ③ | ||
| ④ |
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。某研究小组用粗铜(含杂质Fe)按下述流程制备氯化铜晶体(CuCl2·2H2O)。
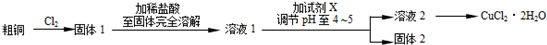
(1)实验室采用如下图所示的装置,可将粗铜与Cl2反应转化为固体1(部分仪器和夹持装置已略去)。

①仪器A的名称是_________ 。
②装置B中发生反应的离子方程式是_________ 。
③有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要(填“是”或“否”)_____________ 。
④ NaOH溶液的作用_______________________
(2)试剂X用于调节pH以除去杂质, X可选用下列试剂中的(填序号)______ 。
a.NaOH b.NH3·H2O c.CuO d.Cu2(OH) 2CO3 e.CuSO4
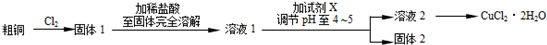
(1)实验室采用如下图所示的装置,可将粗铜与Cl2反应转化为固体1(部分仪器和夹持装置已略去)。

①仪器A的名称是
②装置B中发生反应的离子方程式是
③有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要(填“是”或“否”)
④ NaOH溶液的作用
(2)试剂X用于调节pH以除去杂质, X可选用下列试剂中的(填序号)
a.NaOH b.NH3·H2O c.CuO d.Cu2(OH) 2CO3 e.CuSO4
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】苯甲酸可用于医药、染料载体、增塑剂、果汁饮料的保香剂和食品防腐剂等的生产。某化学兴趣小组欲在实验室制备苯甲酸、回收二氧化锰并测定其纯度,进行如下实验:
苯甲酸实验室制备原理为: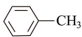 +2KMnO4
+2KMnO4
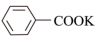 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O
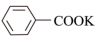

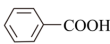
实验装置如图所示。
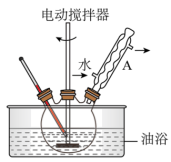
已知:甲苯的密度是0.872g·L-1;苯甲酸微溶于冷水,溶于热水。
实验步骤:
Ⅰ.在50mL三颈烧瓶中加入1.5mL甲苯、20mL水和5.0g高锰酸钾,油浴加热至反应结束。
Ⅱ.将反应液趁热减压过滤,得到滤渣1,滤液呈紫色,加入少量亚硫酸钠使紫色褪去,进行二次减压过滤,得到滤渣2;将滤液放入冰水浴中,然后加酸酸化,有晶体析出,减压过滤,洗涤、干燥,得到苯甲酸晶体。
Ⅲ.回收二氧化锰:将滤渣2和滤纸一并转移到坩埚中,加热灼烧,所得固体与干燥后的滤渣1合并,称重得2.5 g固体。
Ⅳ.二氧化锰纯度的测定:称取0.5g回收的二氧化锰,放于烧杯中,再加入25 mL 0.3 mol·L-1草酸钠溶液及50 mL12 mol·L-1硫酸,加热至二氧化碳不再产生,稀释至250 mL,加热至近沸。趁热以浓度为0.05mol·L-1的高锰酸钾标准液滴定过量的草酸钠,消耗高锰酸钾的体积为16.0mL。
已知:MnO2 + +4H+=Mn2++2CO2↑+2H2O
+4H+=Mn2++2CO2↑+2H2O
回答下列问题:
(1)仪器A的名称为___________ ,
(2)步骤Ⅰ中,判断反应结束的现象是___________ 。
(3)步骤Ⅱ中加酸酸化,加的酸可以是___________ (填序号)。
①稀硫酸 ②盐酸
滤液放入冰水浴的原因是___________ 。
(4)滤渣2的主要成分为MnO(OH)2,请写出生成MnO(OH)2的离子方程式:___________ 。
(5)二氧化锰的纯度为___________ %。
苯甲酸实验室制备原理为:
 +2KMnO4
+2KMnO4
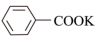 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O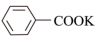


实验装置如图所示。

已知:甲苯的密度是0.872g·L-1;苯甲酸微溶于冷水,溶于热水。
实验步骤:
Ⅰ.在50mL三颈烧瓶中加入1.5mL甲苯、20mL水和5.0g高锰酸钾,油浴加热至反应结束。
Ⅱ.将反应液趁热减压过滤,得到滤渣1,滤液呈紫色,加入少量亚硫酸钠使紫色褪去,进行二次减压过滤,得到滤渣2;将滤液放入冰水浴中,然后加酸酸化,有晶体析出,减压过滤,洗涤、干燥,得到苯甲酸晶体。
Ⅲ.回收二氧化锰:将滤渣2和滤纸一并转移到坩埚中,加热灼烧,所得固体与干燥后的滤渣1合并,称重得2.5 g固体。
Ⅳ.二氧化锰纯度的测定:称取0.5g回收的二氧化锰,放于烧杯中,再加入25 mL 0.3 mol·L-1草酸钠溶液及50 mL12 mol·L-1硫酸,加热至二氧化碳不再产生,稀释至250 mL,加热至近沸。趁热以浓度为0.05mol·L-1的高锰酸钾标准液滴定过量的草酸钠,消耗高锰酸钾的体积为16.0mL。
已知:MnO2 +
 +4H+=Mn2++2CO2↑+2H2O
+4H+=Mn2++2CO2↑+2H2O 回答下列问题:
(1)仪器A的名称为
(2)步骤Ⅰ中,判断反应结束的现象是
(3)步骤Ⅱ中加酸酸化,加的酸可以是
①稀硫酸 ②盐酸
滤液放入冰水浴的原因是
(4)滤渣2的主要成分为MnO(OH)2,请写出生成MnO(OH)2的离子方程式:
(5)二氧化锰的纯度为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】FeCl2是一种常用的还原剂、媒染剂。某化学实验小组在实验室里用如下方法来制备无水FeCl2。有关物质的性质如下:
(1)用H2还原无水FeCl3制取FeCl2。有关装置如图:
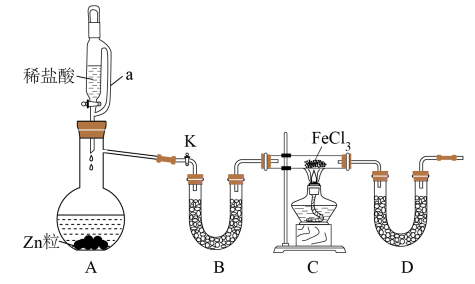
①a的作用是__ ;B中盛放的试剂是__ 。
②H2还原无水FeCl3制取FeCl2的化学方程式为__ 。
③装置D的作用__ 。
④该制备装置的缺点为__ 。
(2)要检验C中的FeCl3是否完全反应的实验操作是__ 。
(3)某学生取C中少量固体溶于水时发现试管中残留少了固体,你认为该固体为_ ;检验该固体可用于试剂__ 。
(4)实验小组同学通过查阅资料,发现利用反应2FeCl3+C6H5Cl=2FeCl2+C6H4Cl2+HCl↑,可制取无水FeCl2,设计装置如图。

①该反应的还原剂是__ ;
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经过滤、用___ 洗涤和干燥后,得到粗产品。
| FeCl3 | FeCl2 | |
| 溶解性 | 不溶于苯、氯苯等,易溶于乙醇,易吸水 | |
| 熔点/℃ | 300℃以上易升华 | 670 |
| 沸点/℃ | 1023 | |

①a的作用是
②H2还原无水FeCl3制取FeCl2的化学方程式为
③装置D的作用
④该制备装置的缺点为
(2)要检验C中的FeCl3是否完全反应的实验操作是
(3)某学生取C中少量固体溶于水时发现试管中残留少了固体,你认为该固体为
(4)实验小组同学通过查阅资料,发现利用反应2FeCl3+C6H5Cl=2FeCl2+C6H4Cl2+HCl↑,可制取无水FeCl2,设计装置如图。

①该反应的还原剂是
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经过滤、用
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】高纯 在感光、电子和信息、电镀等行业中有着广泛的用途。由粗银制备高纯
在感光、电子和信息、电镀等行业中有着广泛的用途。由粗银制备高纯 的流程图如下:
的流程图如下:
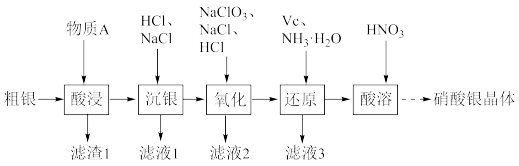
(1)物质A的化学式为___________ 。
(2)沉银的离子方程式为___________ ,若沉银得到的固体颗粒越小,则过滤速率___________ ;若沉银得到的固体颗粒结块,则产品纯度___________ 。
(3)“氧化”工序中,盐酸浓度控制在1.5mol/L左右,如果超过规定浓度,则NaClO3消耗量会超过理论值,原因是___________ ;工艺中“氧化”工序的主要目的为___________ 。
(4)利用Vc、NH3·H2O把银还原,操作中Vc、NH3·H2O加入顺序为:先向氯化银固体中加入___________ ,后加入___________ ,其中还原剂是___________ 。
(5)“酸溶”工序中选择用浓硝酸而不用稀硝酸溶解银,主要目的是___________ (填序号)。
A.防止产生污染性气体 B.减少硝酸消耗
C.增加反应速率 D减少“ 晶体析出”时蒸发的水量
晶体析出”时蒸发的水量
(6)为了进一步提高 纯度,需要对
纯度,需要对 晶体进行
晶体进行___________ (填操作方法)
 在感光、电子和信息、电镀等行业中有着广泛的用途。由粗银制备高纯
在感光、电子和信息、电镀等行业中有着广泛的用途。由粗银制备高纯 的流程图如下:
的流程图如下:
(1)物质A的化学式为
(2)沉银的离子方程式为
(3)“氧化”工序中,盐酸浓度控制在1.5mol/L左右,如果超过规定浓度,则NaClO3消耗量会超过理论值,原因是
(4)利用Vc、NH3·H2O把银还原,操作中Vc、NH3·H2O加入顺序为:先向氯化银固体中加入
(5)“酸溶”工序中选择用浓硝酸而不用稀硝酸溶解银,主要目的是
A.防止产生污染性气体 B.减少硝酸消耗
C.增加反应速率 D减少“
 晶体析出”时蒸发的水量
晶体析出”时蒸发的水量(6)为了进一步提高
 纯度,需要对
纯度,需要对 晶体进行
晶体进行
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】用0.20 mol/L盐酸作标准液,中和滴定法测定某烧碱的纯度。若烧碱中不含有与盐酸反应的杂质,试根据实验回答:
(1)准确称取5.0 g烧碱样品,所用主要仪器有托盘天平、砝码、药匙、_______ 。
(2)将样品配成250 mL待测液,需要的主要仪器有烧杯、玻璃棒、胶头滴管、_______ 。
(3)取10.00 mL待测液,需要的仪器有_______ 、锥形瓶。
(4)该实验滴定时_______ 手旋转_______ 式滴定管的玻璃活塞,_______ 手不停地摇动锥形瓶,两眼注视_______ ,直到滴定终点。
(5)根据下表数据,计算被测烧碱溶液的浓度是_______ 。
(6)根据上述各数据,计算烧碱的纯度_______ 。
(1)准确称取5.0 g烧碱样品,所用主要仪器有托盘天平、砝码、药匙、
(2)将样品配成250 mL待测液,需要的主要仪器有烧杯、玻璃棒、胶头滴管、
(3)取10.00 mL待测液,需要的仪器有
(4)该实验滴定时
(5)根据下表数据,计算被测烧碱溶液的浓度是
| 滴定次数 | 待测溶液体积/mL | 盐酸标准溶液体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
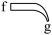
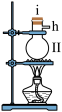
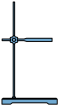
【推荐3】将图中所列仪器组装为一套实验室蒸馏工业酒精的装置,并进行蒸馏。
(1)图中Ⅰ、Ⅱ、Ⅲ三种仪器的名称是__ 、__ 、__ 。
(2)将以上仪器按(一)→(六)顺序,用字母a,b,c…表示连接顺序。
e接( ) ,( ) 接( ) ,( ) 接( ) ,( ) 接( ) 。
(3)Ⅰ仪器中c口是__ ,d口是__ 。(填“进水口”或“出水口”)
(4)蒸馏时,温度计水银球应放在__ 位置。
(5)在Ⅱ中注入工业酒精后,加几片碎瓷片的目的是__ 。
(6)给Ⅱ加热,收集到沸点最低的馏分是__ 。收集到78℃左右的馏分是__ 。
| (三) | (一) | (五) | (二) | (六) | (四) |
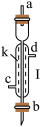 |  |  |  | 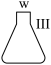 |  |
(2)将以上仪器按(一)→(六)顺序,用字母a,b,c…表示连接顺序。
e接
(3)Ⅰ仪器中c口是
(4)蒸馏时,温度计水银球应放在
(5)在Ⅱ中注入工业酒精后,加几片碎瓷片的目的是
(6)给Ⅱ加热,收集到沸点最低的馏分是
您最近半年使用:0次



