(1)常温下,将___ 通入到NaOH溶液中,可获得___ 为有效成分的漂白液(填化学式);
(2)NaHCO3俗名是___ ,常温时,NaHCO3的溶解度___ Na2CO3(填“大于”或“小于”);
(3)配制FeSO4溶液时需加入硫酸抑制水解,还需加入___ 防止Fe2+被氧化成Fe3+;
(4)加热铝箔时,熔化的铝未滴落,是因为氧化铝的熔点___ 铝的熔点(填“高于”或“低于”)。
(2)NaHCO3俗名是
(3)配制FeSO4溶液时需加入硫酸抑制水解,还需加入
(4)加热铝箔时,熔化的铝未滴落,是因为氧化铝的熔点
更新时间:2020-01-14 12:59:51
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】医疗机构常用质量分数为7.45% 的次氯酸钠消毒液(密度为1.00 g·cm−3)进行消毒,回答下列问题:
(1)该消毒液的物质的量浓度为_______ mol·L−1(保留到小数点后2位)。
(2)次氯酸钠消毒液使用时需要稀释。某化学实验小组用上述消毒液配制95mL 0.7mol·L−1的溶液。
①需用量筒量取该次氯酸钠消毒液_______ mL;量取时若仰视,所配溶液的浓度将_______ (填“偏高”、“偏低”或“无影响”)。
②定容时加蒸馏水,若不慎超过刻度线,应采取的处理方法是_______ 。
(3)资料显示,次氯酸钠消毒液不能与洁厕灵(含盐酸)混合使用,对此某小组开展如下研究。

能观察到两表面皿之间出现黄绿色气体,写出该反应的离子方程式_______ ;蘸有NaOH溶液的脱脂棉吸收黄绿色气体的离子方程式是_______ 。
(1)该消毒液的物质的量浓度为
(2)次氯酸钠消毒液使用时需要稀释。某化学实验小组用上述消毒液配制95mL 0.7mol·L−1的溶液。
①需用量筒量取该次氯酸钠消毒液
②定容时加蒸馏水,若不慎超过刻度线,应采取的处理方法是
(3)资料显示,次氯酸钠消毒液不能与洁厕灵(含盐酸)混合使用,对此某小组开展如下研究。

能观察到两表面皿之间出现黄绿色气体,写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求完成下列问题:
(1)请写出NaCl的电子式___________ ,甲烷的结构式___________ 。
(2)用反应方程式表示制备漂白粉的原理为:___________ 。
(3)漂白粉的有效成分是___________ ,小苏打的化学式为___________ 。
(4)除去FeCl3溶液中FeCl2的原理,用离子方程式表示___________ 。
(1)请写出NaCl的电子式
(2)用反应方程式表示制备漂白粉的原理为:
(3)漂白粉的有效成分是
(4)除去FeCl3溶液中FeCl2的原理,用离子方程式表示
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某学习小组的同学用MnO2和浓盐酸反应来制备纯净的氯气并验证其有无漂白性,设计装置如图:

(1)A装置中反应的化学方程式:____________________________ ;D装置中现象:___________________ ;该套装置存在的缺陷:_________________________________ 。
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是_______________________ (用离子方程式表示)。
(3)若将Cl2通入热的烧碱溶液中,可以发生如下两个反应:
Cl2+2NaOH=NaCl+NaClO+H2O和3Cl2+6NaOH=5NaCl+NaClO3+3H2O。
从氧化还原角度分析Cl2表现了_______________ 。当混合液中Cl-和ClO 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为__________________ 。
(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是___________ ,CuO的作用是_____________ ,写出总反应的化学方程式,并用单线桥法标出该反应的电子转移情况______________________________ 。


(1)A装置中反应的化学方程式:
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是
(3)若将Cl2通入热的烧碱溶液中,可以发生如下两个反应:
Cl2+2NaOH=NaCl+NaClO+H2O和3Cl2+6NaOH=5NaCl+NaClO3+3H2O。
从氧化还原角度分析Cl2表现了
 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】二氧化碳的循环对生活、生产和环境有着重要的影响。
Ⅰ、传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生 ,从而使面团疏松,同时生成乳酸和醋酸等酸性物质,再加入
,从而使面团疏松,同时生成乳酸和醋酸等酸性物质,再加入 可调节面团酸度。
可调节面团酸度。
(1)等质量的碳酸钠和碳酸氢钠,消耗酸更多的是______ 。
(2)若面团发得不好,面团内的气孔少,会略有酸味。厨师会选择向面团中添加 ,而不再用
,而不再用 ,继续揉面后,上锅蒸也能蒸出松软的馒头。请解释添加
,继续揉面后,上锅蒸也能蒸出松软的馒头。请解释添加 的两个作用
的两个作用______ 。
(3)已知磷的含氧酸盐难分解,复合膨松剂发酵的效果更明显。某品牌复合膨松剂的说明书如图所示。其中葡萄糖酸-δ-内酯和淀粉是助剂(防止膨松剂分解、吸潮结块而失效)。推测焦磷酸二氢二钠的作用是______ 。
Ⅱ、二氧化碳的捕捉与封存是未来实现低碳经济转型的重要途径。
(4)科学家设计出烧碱溶液捕捉 法,原理如图所示
法,原理如图所示
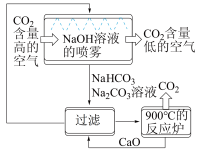
①该过程中能实现NaOH溶液再生的反应为 和
和______ 。
②若喷洒完100mL5mol/L的NaOH溶液后,测得吸收液中的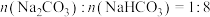 ,则被吸收的
,则被吸收的 在标况下的体积为
在标况下的体积为______ L。
③下列溶液中,也能用作“捕捉”二氧化碳试剂的是______ (填序号)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.稀硫酸
溶液 D.稀硫酸
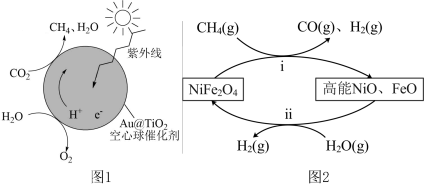
(5)Au@ 蛋黄型空心球催化剂技术实现了
蛋黄型空心球催化剂技术实现了 封存和能量储存双重效果,其原理如图1所示。制得的甲烷(
封存和能量储存双重效果,其原理如图1所示。制得的甲烷( )通过两步法可制取
)通过两步法可制取 ,原理如图2所示。
,原理如图2所示。
①已知 中H为+1价,则空心球催化剂技术中获得的
中H为+1价,则空心球催化剂技术中获得的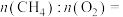
______ 。
②若不考虑过程中原料损失,则16g 通过两步法最多可制得
通过两步法最多可制得 的物质的量为
的物质的量为______ mol。
Ⅰ、传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生
 ,从而使面团疏松,同时生成乳酸和醋酸等酸性物质,再加入
,从而使面团疏松,同时生成乳酸和醋酸等酸性物质,再加入 可调节面团酸度。
可调节面团酸度。(1)等质量的碳酸钠和碳酸氢钠,消耗酸更多的是
(2)若面团发得不好,面团内的气孔少,会略有酸味。厨师会选择向面团中添加
 ,而不再用
,而不再用 ,继续揉面后,上锅蒸也能蒸出松软的馒头。请解释添加
,继续揉面后,上锅蒸也能蒸出松软的馒头。请解释添加 的两个作用
的两个作用(3)已知磷的含氧酸盐难分解,复合膨松剂发酵的效果更明显。某品牌复合膨松剂的说明书如图所示。其中葡萄糖酸-δ-内酯和淀粉是助剂(防止膨松剂分解、吸潮结块而失效)。推测焦磷酸二氢二钠的作用是
| 【名称】xx复合膨松剂 【保质期】24个月 【净含量】1kg 【使用量】面粉用量的0.5%~2.5% 【配料】碳酸氢钠、焦磷酸二氢二钠、碳酸钙、葡萄糖酸-δ-内酯、淀粉 【适用范围】适用于各类馒头、包子等发酵面制品以及面包、糕点等的制作 【保存方法】阴凉干燥处存储 |
Ⅱ、二氧化碳的捕捉与封存是未来实现低碳经济转型的重要途径。
(4)科学家设计出烧碱溶液捕捉
 法,原理如图所示
法,原理如图所示
①该过程中能实现NaOH溶液再生的反应为
 和
和②若喷洒完100mL5mol/L的NaOH溶液后,测得吸收液中的
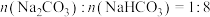 ,则被吸收的
,则被吸收的 在标况下的体积为
在标况下的体积为③下列溶液中,也能用作“捕捉”二氧化碳试剂的是
A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.稀硫酸
溶液 D.稀硫酸(5)Au@
 蛋黄型空心球催化剂技术实现了
蛋黄型空心球催化剂技术实现了 封存和能量储存双重效果,其原理如图1所示。制得的甲烷(
封存和能量储存双重效果,其原理如图1所示。制得的甲烷( )通过两步法可制取
)通过两步法可制取 ,原理如图2所示。
,原理如图2所示。
①已知
 中H为+1价,则空心球催化剂技术中获得的
中H为+1价,则空心球催化剂技术中获得的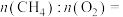
②若不考虑过程中原料损失,则16g
 通过两步法最多可制得
通过两步法最多可制得 的物质的量为
的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】学习化学应该明确“从生活中来,到生活中去”道理。在生产生活中,我们会遇到各种各样的化学反应。
(1)请你写出发酵粉中的主要钠盐的化学式______________ 。
(2)请你写出下列反应的化学方程式。(注意反应条件并配平)
工业上用氯气和消石灰(氢氧化钙乳浊液)反应制取漂白粉(主要成分是氯化钙和次氯酸钙)________________________________________ 。
(3)请你写出下列反应的离子方程式。
胃舒平含有氢氧化铝,可用来治疗胃酸(盐酸)过多____________ 。
将铁加入硫酸铜溶液中炼铜(湿法炼铜)_________________ 。
(1)请你写出发酵粉中的主要钠盐的化学式
(2)请你写出下列反应的化学方程式。(注意反应条件并配平)
工业上用氯气和消石灰(氢氧化钙乳浊液)反应制取漂白粉(主要成分是氯化钙和次氯酸钙)
(3)请你写出下列反应的离子方程式。
胃舒平含有氢氧化铝,可用来治疗胃酸(盐酸)过多
将铁加入硫酸铜溶液中炼铜(湿法炼铜)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】金属钠还可以用于钛、锆、铌、钽等金属的冶炼。如Na与 反应产生Ti。
反应产生Ti。
(1)把钠投入 溶液中,不能置换出Ti单质,原因是:
溶液中,不能置换出Ti单质,原因是:_____ 。
以下是Ti及其他2种金属的相关性质:
(2)钛是制造飞机的材料之一、根据表中数据,解释为何用钛来制造飞机_____ 。
(3)钢是主要含铁的合金。汽车车身可以用铝或钢制造。已知铁在潮湿的空气中会迅速腐蚀,而铝不会。
①请解释铝耐腐蚀的原因_____ 。(用方程式表示)
②根据表中数据,描述用铝来取代钢制造汽车车身的一项优点是_____ ,缺点是_____ 。
 反应产生Ti。
反应产生Ti。(1)把钠投入
 溶液中,不能置换出Ti单质,原因是:
溶液中,不能置换出Ti单质,原因是:以下是Ti及其他2种金属的相关性质:
| 金属 | 熔点(℃) | 密度( ) ) | 相对强度 | 相对硬度 | 每吨价格(元) |
| 铝 | 660 | 2.7 | 11 | 2.8 | 11400 |
| 铁 | 1538 | 7.9 | 20 | 4.5 | 4000 |
| 钛 | 1668 | 4.5 | 40 | 6.0 | 160000 |
(3)钢是主要含铁的合金。汽车车身可以用铝或钢制造。已知铁在潮湿的空气中会迅速腐蚀,而铝不会。
①请解释铝耐腐蚀的原因
②根据表中数据,描述用铝来取代钢制造汽车车身的一项优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铝是地壳中含量最多的金属元素,在自然界主要以化合态形式存在。
(1)食品包装中经常用到铝箔,铝能制成铝箔是因为铝的____________ 性;工业上制造热交换器、散热器是利用了铝的____________ 性。
(2)铝条投入氢氧化钠溶液中,加热片刻后取出洗净,立即浸入硝酸汞溶液中,此时反应的化学方程式是________________________________________________ ;
取出铝条用滤纸吸干,在空气中铝条表面慢慢长出整齐的________________________ (现象),该物质是________________________ (写化学式).
某研究性学习小组对铝热反应实验展开研究。现行高中化学教材中对“铝热反应”的现象有这样的描述:反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中” 。查阅《化学手册》可知,Al、 Al2O3、 Fe、Fe2O3的熔点、沸点数据如下:
(3)某同学推测,铝热反应所得到的熔融物应是铁铝合金。请设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是________________ ,反应的离子方程式________________ ;
(4)实验室溶解该熔融物,在下列试剂中最适宜的试剂是______________ (填序号).
A. 浓硫酸 B. 稀硫酸 C. 浓硝酸 D. 氢氧化钠溶液
(1)食品包装中经常用到铝箔,铝能制成铝箔是因为铝的
(2)铝条投入氢氧化钠溶液中,加热片刻后取出洗净,立即浸入硝酸汞溶液中,此时反应的化学方程式是
取出铝条用滤纸吸干,在空气中铝条表面慢慢长出整齐的
某研究性学习小组对铝热反应实验展开研究。现行高中化学教材中对“铝热反应”的现象有这样的描述:反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中” 。查阅《化学手册》可知,Al、 Al2O3、 Fe、Fe2O3的熔点、沸点数据如下:
| Al | Al2O3 | Fe | Fe2O3 | |
| 熔点 | 660 | 2054 | 1535 | 1462 |
| 沸点 | 2467 | 2980 | 2750 | - |
(3)某同学推测,铝热反应所得到的熔融物应是铁铝合金。请设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是
(4)实验室溶解该熔融物,在下列试剂中最适宜的试剂是
A. 浓硫酸 B. 稀硫酸 C. 浓硝酸 D. 氢氧化钠溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据所学知识回答下列问题:
(1)常温下镁、铝都具有较强的抗腐蚀性,主要原因是__ 。
(2)标准状况下,4.48L氨气与同条件下__ gH2S含有相同的氢原子数。
(3)标准状况下,6.72L由CO和CO2组成的混合气体的质量为12g,则CO和CO2的物质的量之比是__ 。
(4)将14g由Na2O和Na2O2组成的混合物加入足量的水中充分反应后,生成标准状况下1.12L气体,所得溶液的体积为500mL。则原混合物中Na2O的物质的量为__ mol;所得溶液中溶质的物质的量浓度为__ mol•L-1。
(5)实验室需配制500mL0.1mol•L-1FeSO4溶液,实际应称量绿矾(FeSO4•7H2O)的质量为__ g。配制时,其正确的操作顺序是__ (填标号,每个标号只能用一次)。
①用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
②将准确称量的绿矾倒入烧杯中,再加适量水溶解
③将已冷却的溶液沿玻璃棒注入容量瓶中
④将容量瓶盖紧,振荡,反复上下颠倒,摇匀
⑤改用胶头滴管加水,使溶液凹面恰好与刻度线相切
⑥继续往容量瓶内小心加水,直到液面接近刻度线下1~2cm处
(1)常温下镁、铝都具有较强的抗腐蚀性,主要原因是
(2)标准状况下,4.48L氨气与同条件下
(3)标准状况下,6.72L由CO和CO2组成的混合气体的质量为12g,则CO和CO2的物质的量之比是
(4)将14g由Na2O和Na2O2组成的混合物加入足量的水中充分反应后,生成标准状况下1.12L气体,所得溶液的体积为500mL。则原混合物中Na2O的物质的量为
(5)实验室需配制500mL0.1mol•L-1FeSO4溶液,实际应称量绿矾(FeSO4•7H2O)的质量为
①用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
②将准确称量的绿矾倒入烧杯中,再加适量水溶解
③将已冷却的溶液沿玻璃棒注入容量瓶中
④将容量瓶盖紧,振荡,反复上下颠倒,摇匀
⑤改用胶头滴管加水,使溶液凹面恰好与刻度线相切
⑥继续往容量瓶内小心加水,直到液面接近刻度线下1~2cm处
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】判断正误。
1.用铁制容器可以运输浓硝酸和浓H2SO4。_____
2.铁在潮湿的空气中生成的铁锈主要成分是Fe2O3,铁在纯氧中燃烧的产物是Fe3O4,Fe在高温下与水蒸气反应生成Fe2O3。_____
3.铁与硫蒸气反应生成的是Fe2S3,铁与碘蒸气反应生成FeI3。_____
4.配制FeSO4溶液时,加入稀硫酸防止Fe2+水解,加入铁粉防止Fe2+被氧化。_____
5.氢氧化铁与HI溶液仅发生中和反应。_____
6.FeCl3、FeCl2和Fe(OH)3都可以通过化合反应制取。_____
7.Fe3O4是混合物。_____
8.FeO和稀HNO3的反应离子方程式:FeO+2H+=Fe2++H2O。_____
9.稀H2SO4和Ba(OH)2溶液反应离子方程式:H++SO +Ba2++OH-=BaSO4↓+H2O。
+Ba2++OH-=BaSO4↓+H2O。_____
10.向FeI2中通入少量Cl2的离子方程式:2Fe2++Cl2=2Fe3++2Cl-。_____
1.用铁制容器可以运输浓硝酸和浓H2SO4。
2.铁在潮湿的空气中生成的铁锈主要成分是Fe2O3,铁在纯氧中燃烧的产物是Fe3O4,Fe在高温下与水蒸气反应生成Fe2O3。
3.铁与硫蒸气反应生成的是Fe2S3,铁与碘蒸气反应生成FeI3。
4.配制FeSO4溶液时,加入稀硫酸防止Fe2+水解,加入铁粉防止Fe2+被氧化。
5.氢氧化铁与HI溶液仅发生中和反应。
6.FeCl3、FeCl2和Fe(OH)3都可以通过化合反应制取。
7.Fe3O4是混合物。
8.FeO和稀HNO3的反应离子方程式:FeO+2H+=Fe2++H2O。
9.稀H2SO4和Ba(OH)2溶液反应离子方程式:H++SO
 +Ba2++OH-=BaSO4↓+H2O。
+Ba2++OH-=BaSO4↓+H2O。10.向FeI2中通入少量Cl2的离子方程式:2Fe2++Cl2=2Fe3++2Cl-。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某班同学通过实验探究 、
、 的性质。回答下列问题:
的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成 的溶液。在
的溶液。在 溶液中需加入少量铁屑,其目的是
溶液中需加入少量铁屑,其目的是___________ 。
(2)甲组同学取 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴 溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与氯水反应的离子方程式为
溶液与氯水反应的离子方程式为___________ 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在 溶液中先加入
溶液中先加入 煤油,再于液面下依次加入几滴氯水和1滴
煤油,再于液面下依次加入几滴氯水和1滴 溶液,溶液变红。煤油的作用是
溶液,溶液变红。煤油的作用是___________ 。
(4)丙组同学取 溶液,加入
溶液,加入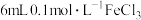 溶液混合。分别取
溶液混合。分别取 此溶液于3支试管中进行如下实验:
此溶液于3支试管中进行如下实验:
①第一支试管中加入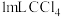 充分振荡、静置,
充分振荡、静置, 层显紫色;
层显紫色;
②第二支试管中加入1滴 溶液,生成蓝色沉淀;
溶液,生成蓝色沉淀;
③第三支试管中加入1滴 溶液,溶液变红。
溶液,溶液变红。
实验②检验的离子是___________ (填离子符号);实验①和③说明:在 过量的情况下,溶液中仍含有
过量的情况下,溶液中仍含有___________ (填离子符号),由此可以证明该氧化还原反应为___________ 。
(5)丁组同学向盛有 溶液的试管中加入几滴酸化的
溶液的试管中加入几滴酸化的 溶液,溶液变成棕黄色,发生反应的离子方程式为
溶液,溶液变成棕黄色,发生反应的离子方程式为___________ ;如果向 溶液中滴加
溶液中滴加 溶液,现象是
溶液,现象是___________ ;沉淀变色的原因是___________ (用化学方程式解释)。
 、
、 的性质。回答下列问题:
的性质。回答下列问题:(1)分别取一定量氯化铁、氯化亚铁固体,均配制成
 的溶液。在
的溶液。在 溶液中需加入少量铁屑,其目的是
溶液中需加入少量铁屑,其目的是(2)甲组同学取
 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴 溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与氯水反应的离子方程式为
溶液与氯水反应的离子方程式为(3)乙组同学认为甲组的实验不够严谨,该组同学在
 溶液中先加入
溶液中先加入 煤油,再于液面下依次加入几滴氯水和1滴
煤油,再于液面下依次加入几滴氯水和1滴 溶液,溶液变红。煤油的作用是
溶液,溶液变红。煤油的作用是(4)丙组同学取
 溶液,加入
溶液,加入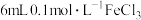 溶液混合。分别取
溶液混合。分别取 此溶液于3支试管中进行如下实验:
此溶液于3支试管中进行如下实验:①第一支试管中加入
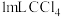 充分振荡、静置,
充分振荡、静置, 层显紫色;
层显紫色;②第二支试管中加入1滴
 溶液,生成蓝色沉淀;
溶液,生成蓝色沉淀;③第三支试管中加入1滴
 溶液,溶液变红。
溶液,溶液变红。实验②检验的离子是
 过量的情况下,溶液中仍含有
过量的情况下,溶液中仍含有(5)丁组同学向盛有
 溶液的试管中加入几滴酸化的
溶液的试管中加入几滴酸化的 溶液,溶液变成棕黄色,发生反应的离子方程式为
溶液,溶液变成棕黄色,发生反应的离子方程式为 溶液中滴加
溶液中滴加 溶液,现象是
溶液,现象是
您最近一年使用:0次




