下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将浓硫酸滴到纸上 | 纸张变黑 | 浓硫酸具有吸水性 |
| B | 测定等浓度的Na2CO3和Na2SO3的溶液的pH | 前者pH比后者的大 | 非金属性:S>C |
| C | 向2.0ml浓度均为0.1mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01mol·L-1AgNO3溶液,振荡 | 沉淀呈黄色 | Ksp(AgCl)>Ksp(AgI) |
| D | 将镁条点燃后迅速伸入集满CO2的集气瓶 | 集气瓶中有浓烟和黑色颗粒 | CO2具有还原性 |
| A.A | B.B | C.C | D.D |
更新时间:2020-01-13 19:33:22
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】根据下列实验操作和现象所得出的结论错误的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状碳 | 浓硫酸具有脱水性和强氧化性 |
| B | 向盛Na2SiO3溶液的试管中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 | 2 min后,试管里出现凝胶 | 非金属性:Cl>Si |
| C | 向盛有铜片的容器中加入浓硝酸 | 产生大量红棕色气体,溶液变为蓝绿色 | 浓硝酸具有强氧化性和酸性 |
| D | 向NaAlO2溶液中持续通入气体Y | 出现白色沉淀 | Y可能是CO2气体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列陈述Ⅰ、Ⅱ正确并且有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A. | Fe3+ 有氧化性 | FeCl 溶液可用于回收旧电路板中的铜 溶液可用于回收旧电路板中的铜 |
| B. | SiO2有导电性 | SiO 可用于制备光导纤维 可用于制备光导纤维 |
| C. | 氯水、SO2都有漂白性 | 氯水与SO2混合使用漂白效果更好 |
| D. | 铝制容器表面有氧化膜保护 | 可用铝制容器盛装稀硫酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】X、Y、Z、W四种物质存在如图所示的转化关系:
下列说法错误的是
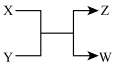
下列说法错误的是
| A.若X为镁,Z为氧化镁,则Y可能为二氧化碳 |
| B.若X为硫酸铜溶液,Z为红色固体物质,则Y可能为钾 |
| C.若X、Z均为非金属单质,则Y可能为二氧化硅 |
| D.若X、Z均为金属单质,则Y可能为二氧化锰 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在托盘天平的两盘上,分别放有两个质量相同的烧杯,各盛有6 mol·L-1HCl 100 mL,使天平达到平衡。分别向两烧杯中加入不超过5 g 的镁和铝,若要使其充分反应后天平仍保持平衡,则加入的镁与铝的质量之比为( )
| A.1∶1 | B.24∶27 | C.12∶9 | D.32∶33 |
您最近一年使用:0次
【推荐1】室温下,向含 和
和 的溶液中滴加
的溶液中滴加 溶液,混合液中
溶液,混合液中 和
和 的关系如图所示。已知:
的关系如图所示。已知: ;
;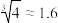 。下列说法正确的是
。下列说法正确的是
 和
和 的溶液中滴加
的溶液中滴加 溶液,混合液中
溶液,混合液中 和
和 的关系如图所示。已知:
的关系如图所示。已知: ;
;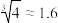 。下列说法正确的是
。下列说法正确的是
A.直线Ⅰ、Ⅱ、Ⅲ分别代表 和 和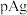 的关系 的关系 |
B.d点直线Ⅱ和直线Ⅲ对应的两种沉淀的 相同 相同 |
C.向 的混合溶液中逐滴滴加 的混合溶液中逐滴滴加 溶液,先生成 溶液,先生成 沉淀 沉淀 |
D. 的平衡常数 的平衡常数 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列实验操作、现象及所得出的结论或解释均正确的是
| 选项 | 实验操作 | 现象 | 结论或解释 |
| A | 向盐酸中滴加Na2SO3溶液 | 产生使品红溶液褪色的气体 | 非金属性:Cl>S |
| B | 向废FeCl3蚀刻液X中加入少量的铁粉,振荡 | 未出现红色固体 | X中一定不含Cu2+ |
| C | 用c(Fe3+)相同的Fe2(SO4)3和FeCl3溶液,分别清洗做完银镜反应的试管 | FeCl3溶液清洗得较干净 | Fe3++Ag Fe2++Ag+是可逆反应,且AgCl更难溶于水 Fe2++Ag+是可逆反应,且AgCl更难溶于水 |
| D | 用3 mL稀硫酸与纯锌粒反应,再加入几滴 Cu(NO3)2浓溶液 | 迅速产生无色气体 | 形成Zn-Cu原电池加快了制取H2的速率 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】科研小组用氧化—沉淀法从废电池浸出液中去除铁:用MnO2氧化废电池浸出液中的Fe2+,再加适量Na2CO3调pH使Fe3+转化为Fe(OH)3沉淀的同时并产生气体。研究发现pH对Fe2+的氧化率和铁去除率的影响如图1和图2所示。
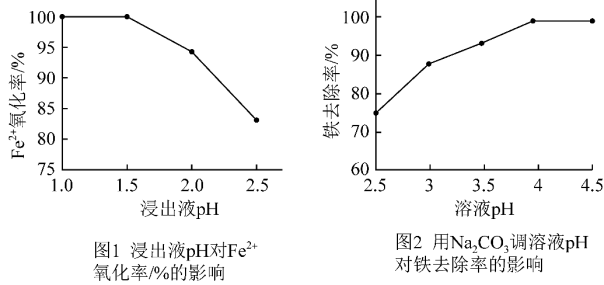
已知:i. pH越大,c(H+)越小;ii.酸性条件下MnO2被还原为Mn2+。下列说法不合理的是

已知:i. pH越大,c(H+)越小;ii.酸性条件下MnO2被还原为Mn2+。下列说法不合理的是
| A.由图1可知,Fe2+氧化率随浸出液c(H+)增大而增大 |
B.Fe2+氧化率达95%以上时反应的离子方程式为: |
C.Fe3+转变为沉淀的离子方程式为: |
| D.推测若用氨水调溶液pH也可以使Fe3+转化为Fe(OH)3沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】X、Y、Z、M、Q为原子序数依次增大的短周期主族元素,其最外层电子数之和为19,Z的原子序数是X与Y的原子序数之和,M与X同主族,X与Q可形成原子个数比为2:1的18e–分子。下列说法正确的是
| A.简单气态氢化物的稳定性:Y<Z<Q |
| B.简单离子半径:Q>M>Z>Y |
| C.含Z、M、Q三种元素的化合物超过3种 |
| D.X与其他四种元素形成的二元化合物含有相同的化学键 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】最近,科学家发现对LiTFSI(一种亲水有机盐)进行掺杂和改进,能显著提高锂离子电池传输电荷的能力。LiTFSI的结构如图所示,其中A、B、C、D为同一短周期元素,C与E位于同一主族。下列叙述正确的是
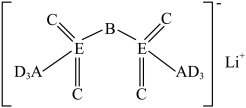

| A.简单气态氢化物的稳定性: C>E> D |
| B.第一电离能:E >D>C |
| C.电负性:D>C>E |
| D.该化合物中只有A、C、D元素原子的最外层满足8电子稳定结构 |
您最近一年使用:0次

 常用于制备其它超硬、耐高温的氮化物,实验室通过CuO氧化NH3制得N2,然后与镁反应得到Mg3N2。已知
常用于制备其它超硬、耐高温的氮化物,实验室通过CuO氧化NH3制得N2,然后与镁反应得到Mg3N2。已知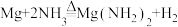 ,Mg3N2是一种浅黄色粉末,易水解。下列说法错误的是
,Mg3N2是一种浅黄色粉末,易水解。下列说法错误的是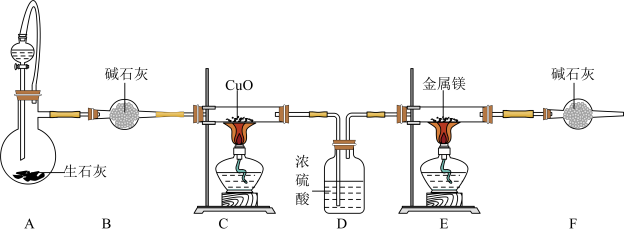
 的作用只是吸收装置
的作用只是吸收装置 中产生的水蒸气
中产生的水蒸气 处酒精灯
处酒精灯


