烟气脱硫能有效减少二氧化硫的排放。实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝[Al2(SO4)3·Al2O3]溶液,并用于烟气脱硫研究。

(1)酸浸时反应的化学方程式为_______________________________________________ ;滤渣Ⅰ的主要成分为________ (填化学式)。
(2)滤渣Ⅱ的主要成分为________ (填化学式);制备碱式硫酸铝[Al2(SO4)3·Al2O3]溶液的化学方程式为_________________________________________________________________ 。
(3)吸收烟气中SO2的化学方程式为Al2(SO4)3·Al2O3+3SO2=Al2(SO4)3·Al2(SO3)3。通入空气氧化,发生反应的化学方程式为_______________________________________________________ 。

(1)酸浸时反应的化学方程式为
(2)滤渣Ⅱ的主要成分为
(3)吸收烟气中SO2的化学方程式为Al2(SO4)3·Al2O3+3SO2=Al2(SO4)3·Al2(SO3)3。通入空气氧化,发生反应的化学方程式为
更新时间:2020-01-30 12:03:23
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】【举一反三】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:

(1)若A是淡黄色固体,C、D是氧化物,C是造成酸雨的主要物质,但C也有其广泛的用途,写出其中的两个用途:_____________________________ 。
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出该反应的化学方程式:_____________________________ 。
(3)若D物质具有两性,②、③反应均要用强碱溶液,④反应时通入过量的一种引起温室效应的主要气体。判断单质A的元素在周期表中的位置:___________________________ 。
(4)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中除钠、氧外的元素为同一主族,且溶液均显碱性。写出②反应的化学方程式:_______________________________ 。
D的化学式是________ 。
(5)若A是应用最广泛的金属。④反应用到A,②、⑤反应均用到同一种非金属单质。C的溶液用于蚀刻印刷铜电路板,写出该反应的离子方程式:_________________________ 。

(1)若A是淡黄色固体,C、D是氧化物,C是造成酸雨的主要物质,但C也有其广泛的用途,写出其中的两个用途:
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出该反应的化学方程式:
(3)若D物质具有两性,②、③反应均要用强碱溶液,④反应时通入过量的一种引起温室效应的主要气体。判断单质A的元素在周期表中的位置:
(4)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中除钠、氧外的元素为同一主族,且溶液均显碱性。写出②反应的化学方程式:
D的化学式是
(5)若A是应用最广泛的金属。④反应用到A,②、⑤反应均用到同一种非金属单质。C的溶液用于蚀刻印刷铜电路板,写出该反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下列A~I九种中学化学常见的物质之间的转化关系如图所示。已知A为固态非金属单质,B 在实验室常用作气体干燥剂,D为常见液体,常温下C、E、F都是无色气体,E能使酸性高锰酸钾溶液褪色,G是侯氏制碱法的最终产品。
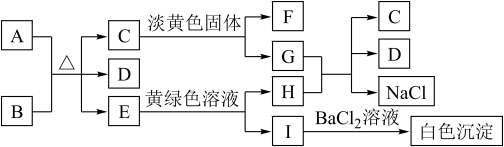
回答下列问题:
(1)F的分子式是_______ ,组成单质A的元素在周期表中的位置是_______ ,图中淡黄色固体中的阴、阳离子个数比为_______ 。
(2)A与B反应的化学方程式是:_______ 。
(3)E转变为H和I的离子方程式是:_______ ,体现了E的_______ 性。
(4)简述检验H溶于水电离所产生的阴离子的操作方法、实验现象和结论:_______ 。

回答下列问题:
(1)F的分子式是
(2)A与B反应的化学方程式是:
(3)E转变为H和I的离子方程式是:
(4)简述检验H溶于水电离所产生的阴离子的操作方法、实验现象和结论:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】为了探究某盐 (仅含三种短周期元素,摩尔质量介于
(仅含三种短周期元素,摩尔质量介于 )的组成和性质,设计并完成了如下实验。已知:
)的组成和性质,设计并完成了如下实验。已知: 、
、 、
、 均为纯净物,
均为纯净物, 、
、 组成元素相同。请回答:
组成元素相同。请回答:

(1)组成 的
的 种元素是
种元素是___________ (填元素符号), 的化学式是
的化学式是___________ 。
(2)写出固体 与
与 反应的离子方程式
反应的离子方程式___________ 。
(3) 溶液在空气中易被氧化。某课题小组测得
溶液在空气中易被氧化。某课题小组测得 溶液在空气中
溶液在空气中 变化,如图所示:
变化,如图所示:

①写出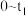 段发生反应的化学方程式
段发生反应的化学方程式___________ 。
②设计实验检验 时刻后溶液中的主要阴离子
时刻后溶液中的主要阴离子___________ 。
(4)有同学预测 也能与稀硫酸反应,现象与固体
也能与稀硫酸反应,现象与固体 和稀硫酸反应相同。你是否支持他的观点并说明理由
和稀硫酸反应相同。你是否支持他的观点并说明理由___________ 。
 (仅含三种短周期元素,摩尔质量介于
(仅含三种短周期元素,摩尔质量介于 )的组成和性质,设计并完成了如下实验。已知:
)的组成和性质,设计并完成了如下实验。已知: 、
、 、
、 均为纯净物,
均为纯净物, 、
、 组成元素相同。请回答:
组成元素相同。请回答:
(1)组成
 的
的 种元素是
种元素是 的化学式是
的化学式是(2)写出固体
 与
与 反应的离子方程式
反应的离子方程式(3)
 溶液在空气中易被氧化。某课题小组测得
溶液在空气中易被氧化。某课题小组测得 溶液在空气中
溶液在空气中 变化,如图所示:
变化,如图所示:
①写出
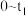 段发生反应的化学方程式
段发生反应的化学方程式②设计实验检验
 时刻后溶液中的主要阴离子
时刻后溶液中的主要阴离子(4)有同学预测
 也能与稀硫酸反应,现象与固体
也能与稀硫酸反应,现象与固体 和稀硫酸反应相同。你是否支持他的观点并说明理由
和稀硫酸反应相同。你是否支持他的观点并说明理由
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】烟气脱硫能有效减少二氧化硫的排放。实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝[Al2(SO4)x(OH)6—2x]溶液,并用于烟气脱硫研究。
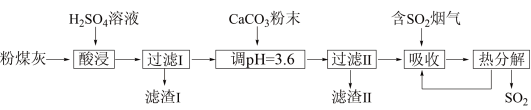
(1)酸浸时反应的化学方程式为_________________ ;滤渣Ⅰ的主要成分为_____ (填化学式)。
(2)加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为Al2(SO4)x(OH)6—2x。滤渣Ⅱ的主要成分为______ (填化学式);若溶液的pH偏高,将会导致溶液中铝元素的含量降低,其原因是_____________________ (用离子方程式表示)。
(3)上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量,其主要原因是_______ ;与吸收SO2前的溶液相比,热分解后循环利用的溶液的pH将_______ (填“增大”、“减小”或“不变”)。

(1)酸浸时反应的化学方程式为
(2)加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为Al2(SO4)x(OH)6—2x。滤渣Ⅱ的主要成分为
(3)上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量,其主要原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知蓝铜矿的主要成分是2CuCO3·Cu(OH)2,受热易分解。铝土矿的主要成分是Al2O3、Fe2O3、SiO2。经过一定条件的转化二者均可转化为金属单质,根据下列框图转化回答问题:
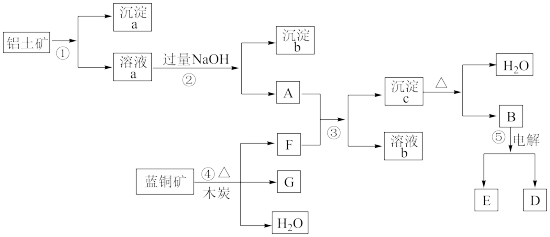
(1)写出①的离子方程式:______________________ 、_____________________ 。
(2)经过④、⑤步反应得到铜和金属铝,写出反应的化学方程式:
________________________________ 、_________________________________ 。
(3)若过量F与A反应,溶液b的成分是:_____________ (写化学式)。

(1)写出①的离子方程式:
(2)经过④、⑤步反应得到铜和金属铝,写出反应的化学方程式:
(3)若过量F与A反应,溶液b的成分是:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】聚合氯化铝晶体是介于AlCl3和Al(OH)3之间的一种水溶性无机高分子聚合物,其制备原料主要是铝加工行业的废渣——铝灰,它主要含Al2O3、Al,还有SiO2等杂质。聚合氯化铝生产的工艺流程如下:

(1)反应中副产品a是________ (用化学式表示)。
(2)升高pH至4.0~5.0的目的是______________________ 。
(3)生产过程中可循环使用的物质是________ (用化学式表示)。
(4)为使得到的晶体较纯净,生产过程中使pH升高的C物质可选用________ (填编号)。
a.NaOH b.Al c.氨水 d.Al2O3 e.NaAlO2
(5)由相关资料可知,聚合氯化铝晶体的化学式可表示为[Al2(OH)nCl6-n·xH2O]m,实验室测定n的值:
①称取a g晶体,制成粉末,加热至质量不再变化为止,称量为b g。此过程可能用到的下列仪器有________ 。
a.蒸发皿 b.坩埚 c.研钵 d.试管
②另取a g晶体,进行如下操作:用A试剂溶解→加足量AgNO3溶液→C操作→烘干→称量为c g。A试剂为________ (填试剂名称),C操作为________ (填操作名称),n=________ (用含b、c的代数式表示)。

(1)反应中副产品a是
(2)升高pH至4.0~5.0的目的是
(3)生产过程中可循环使用的物质是
(4)为使得到的晶体较纯净,生产过程中使pH升高的C物质可选用
a.NaOH b.Al c.氨水 d.Al2O3 e.NaAlO2
(5)由相关资料可知,聚合氯化铝晶体的化学式可表示为[Al2(OH)nCl6-n·xH2O]m,实验室测定n的值:
①称取a g晶体,制成粉末,加热至质量不再变化为止,称量为b g。此过程可能用到的下列仪器有
a.蒸发皿 b.坩埚 c.研钵 d.试管
②另取a g晶体,进行如下操作:用A试剂溶解→加足量AgNO3溶液→C操作→烘干→称量为c g。A试剂为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某实验小组用工业上废弃固体(主要成分 和
和 )合物制取粗铜和
)合物制取粗铜和 晶体,设计的操作流程如下:
晶体,设计的操作流程如下:

(1)③实验过程中,过滤操作用到的玻璃仪器有___________ 。
(2)③④操作中会有一种气体生成,若在实验室制备该气体,可选择下列哪些装置___________ (填字母)。

(3)溶液 在空气中放置有可能变质,如何检验溶液
在空气中放置有可能变质,如何检验溶液 是否变质:
是否变质:___________ 。
(4)溶液 加稀硫酸酸化后加强氧化剂
加稀硫酸酸化后加强氧化剂 ,试剂
,试剂 最好选择下列哪种试剂
最好选择下列哪种试剂___________ (填字母)。
a. b.
b. c.
c.
试剂 在酸性条件下与溶液
在酸性条件下与溶液 反应的离子方程式为
反应的离子方程式为___________ 。
(5)由溶液C经___________ 、___________ 、过滤等操作得 晶体。
晶体。
 和
和 )合物制取粗铜和
)合物制取粗铜和 晶体,设计的操作流程如下:
晶体,设计的操作流程如下:
(1)③实验过程中,过滤操作用到的玻璃仪器有
(2)③④操作中会有一种气体生成,若在实验室制备该气体,可选择下列哪些装置

(3)溶液
 在空气中放置有可能变质,如何检验溶液
在空气中放置有可能变质,如何检验溶液 是否变质:
是否变质:(4)溶液
 加稀硫酸酸化后加强氧化剂
加稀硫酸酸化后加强氧化剂 ,试剂
,试剂 最好选择下列哪种试剂
最好选择下列哪种试剂a.
 b.
b. c.
c.
试剂
 在酸性条件下与溶液
在酸性条件下与溶液 反应的离子方程式为
反应的离子方程式为(5)由溶液C经
 晶体。
晶体。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】海洋植物如海带、海藻中含有丰富的碘元素。碘元素以碘离子的形式存在。实验室从海带中提取碘的流程如下:
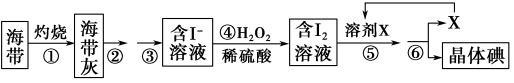
(1)实验时灼烧海带通常应在
(2)步骤④中反应的离子方程式是
(3)提取碘的过程中,⑤中可供选择的有机溶剂是
A.四氯化碳 B.酒精
加入后的现象为
(4)⑥中从碘的有机溶液得到单质碘的操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】在醚类中,正丁醚的溶解力强,对许多油脂、树脂、橡胶、有机酸酯、生物碱等都有很强的溶解力。实验室制备正丁醚的反应、装置示意图和实验步骤如下。

主反应:
副反应:
已知:正丁醚为无色液体,沸点为142℃,密度为0.769g·mL-1,不溶于水。
实验步骤:
①100mL三颈烧瓶中加入15.5mL(12.5g)正丁醇和2.2mL浓硫酸,混合均匀,再加入几粒沸石。
②在三颈烧瓶的一个瓶口装上温度计,另一个瓶口装上分水器,分水器上端接仪器A。
③在分水器中放置2mL水,然后将三颈烧瓶放在石棉网上用小火加热,回流。
④继续加热到三颈烧瓶内温度升高到134~135℃(约需20min),待分水器中的水面不再变化时,表示反应已基本完成。
⑤冷却反应物,将它连同分水器里的水一起倒入盛有25mL水的分液漏斗中,充分振荡,静置,分离出正丁醚粗品。
⑥用两份8mL50%硫酸洗涤两次,再用10mL水洗涤一次,然后用无水氯化钙干燥。
⑦将干燥后的粗产品倒入蒸馏烧瓶中,蒸馏收集139~142℃馏分,得到正丁醚8.5g。
回答下列问题:
(1)仪器A的名称是___________ 。
(2)加入沸石的主要作用是___________ ;加热一段时间后发现忘记加沸石,应采取的操作是___________ (填标号)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中分水器的主要作用是___________ 。
(4)分液漏斗在使用前须清洗干净并检漏,若发现玻璃塞处漏水则可采取的措施为___________ ;在本实验分离过程中,产物应该从分液漏斗的___________ (填“上口倒出”或“下口放出”)。
(5)本实验步骤⑥中用水洗涤的主要目的是___________ 。
(6)本实验所得到的正丁醚产率为___________ (计算结果保留3位有效数字)。

主反应:

副反应:

已知:正丁醚为无色液体,沸点为142℃,密度为0.769g·mL-1,不溶于水。
实验步骤:
①100mL三颈烧瓶中加入15.5mL(12.5g)正丁醇和2.2mL浓硫酸,混合均匀,再加入几粒沸石。
②在三颈烧瓶的一个瓶口装上温度计,另一个瓶口装上分水器,分水器上端接仪器A。
③在分水器中放置2mL水,然后将三颈烧瓶放在石棉网上用小火加热,回流。
④继续加热到三颈烧瓶内温度升高到134~135℃(约需20min),待分水器中的水面不再变化时,表示反应已基本完成。
⑤冷却反应物,将它连同分水器里的水一起倒入盛有25mL水的分液漏斗中,充分振荡,静置,分离出正丁醚粗品。
⑥用两份8mL50%硫酸洗涤两次,再用10mL水洗涤一次,然后用无水氯化钙干燥。
⑦将干燥后的粗产品倒入蒸馏烧瓶中,蒸馏收集139~142℃馏分,得到正丁醚8.5g。
回答下列问题:
(1)仪器A的名称是
(2)加入沸石的主要作用是
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中分水器的主要作用是
(4)分液漏斗在使用前须清洗干净并检漏,若发现玻璃塞处漏水则可采取的措施为
(5)本实验步骤⑥中用水洗涤的主要目的是
(6)本实验所得到的正丁醚产率为
您最近一年使用:0次



