烟气脱硫能有效减少二氧化硫的排放。实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝[Al2(SO4)x(OH)6—2x]溶液,并用于烟气脱硫研究。
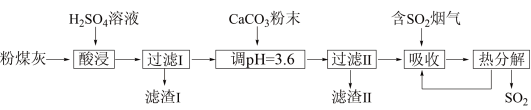
(1)酸浸时反应的化学方程式为_________________ ;滤渣Ⅰ的主要成分为_____ (填化学式)。
(2)加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为Al2(SO4)x(OH)6—2x。滤渣Ⅱ的主要成分为______ (填化学式);若溶液的pH偏高,将会导致溶液中铝元素的含量降低,其原因是_____________________ (用离子方程式表示)。
(3)上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量,其主要原因是_______ ;与吸收SO2前的溶液相比,热分解后循环利用的溶液的pH将_______ (填“增大”、“减小”或“不变”)。

(1)酸浸时反应的化学方程式为
(2)加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为Al2(SO4)x(OH)6—2x。滤渣Ⅱ的主要成分为
(3)上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量,其主要原因是
2014·江苏·高考真题 查看更多[11]
重庆市2023-2024学年高三下学期2月月度质量检测化学试题江苏省马坝高级中学2022-2023学年高三上学期9月份质量检测化学试题江苏省启东中学2017-2018学年高一(创新2班)上学期期中考试化学试题江苏省淮安市涟水县第一中学2021届高三上学期10月月考化学试题(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第2讲 铝及其化合物(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第2讲 镁、铝及其重要化合物【教学案】2017届重庆市第八中学高三上学期定时训练6化学试卷2016届江苏省运河中学高三上学期第一次调研化学试卷2015届安徽省芜湖一中高三上学期期末理综化学试卷2014年全国普通高等学校招生统一考试理科综合能力测试化学(江苏卷)江西省景德镇市第一中学2016-2017学年高一(16班)下学期期中考试化学试题
更新时间:2019-01-30 18:14:09
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某同学设计了如下装置用于制取SO2和验证SO2的性质。

试回答以下问题:
(1)装置A 中用于添加浓硫酸的仪器名称为____ ,其中反应的化学方程式为________ 。
(2)导管①的作用是________ 。
(3)装置D中可观察到的现象是_______ ,体现出 SO2 ______ 性。
(4)E装置的作用是_______ ,发生反应的离子方程式为__________ 。

试回答以下问题:
(1)装置A 中用于添加浓硫酸的仪器名称为
(2)导管①的作用是
(3)装置D中可观察到的现象是
(4)E装置的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某无色溶液可能含有下列钠盐中的几种:(A)氯化钠,(B)硫化钠,(C)亚硫酸钠,(D)硫代硫酸钠Na2S2O3+H2SO4="==" Na2SO4+SO2↑+S↓+H2O),(E)硫酸钠,(F)碳酸钠;向此溶液中加入适量稀硫酸,有浅黄色的沉淀析出,同时有气体生成,此气体能使硫酸铜溶液产生黑色沉淀,也能使澄清石灰水变浑浊,不能使品红溶液褪色.根据上述实验现象,回答下列问题:
根据上述实验现象回答下列问题
(1)不能使品红试液褪色,说明该气体中不含____________ (填分子式).
(2)此无色溶液中至少可能存在哪几种钠盐?请写出全部可能的情况(填写相应的字母).
第一种情况是________________ ,第二种情况是__________________ ,第三种情况是________________ ,第四种情况是__________________ .
(可不填满,也可补充)
根据上述实验现象回答下列问题
(1)不能使品红试液褪色,说明该气体中不含
(2)此无色溶液中至少可能存在哪几种钠盐?请写出全部可能的情况(填写相应的字母).
第一种情况是
(可不填满,也可补充)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】硫酸是重要的化工原料,用于生产化肥、农药、炸药、染料和盐类等。
某实验小组采用下图装置模拟硫酸工业的接触室,并测定 催化氧化为
催化氧化为 的转化率。
的转化率。

已知:
(1)反应开始时,打开 ,关闭
,关闭 ,使
,使 和氧气一起通过装置
和氧气一起通过装置 进入
进入 中发生反应,反应后的气体进入装置
中发生反应,反应后的气体进入装置 ,装置
,装置 的作用为
的作用为___________ ;若将装置 换为如图所示装置,实验测得
换为如图所示装置,实验测得 的转化率会偏大,原因为
的转化率会偏大,原因为___________ (用化学反应方程式解释)。

(2)装置F中___________ 现象说明气体吸收完全。
(3)实验结束后的操作顺序为___________ (填序号)。
①待 充分反应后,熄灭
充分反应后,熄灭 处的酒精灯
处的酒精灯
②停止通入
③停止滴加浓硫酸,关闭 ,打开
,打开
(4)装置B中发生的离子反应方程式为___________ ,装置B中试剂可替换为___________ (填字母)。
A.水 B. 溶液
溶液
C. 溶液 D.饱和
溶液 D.饱和 溶液
溶液
(5)反应结束后测得装置 质量增加mg,装置
质量增加mg,装置 质量增加ng,则该条件下
质量增加ng,则该条件下 的转化率为
的转化率为___________ (用字母表示)。
某实验小组采用下图装置模拟硫酸工业的接触室,并测定
 催化氧化为
催化氧化为 的转化率。
的转化率。
已知:
 |  | |
| 熔点/℃ | 16.8 | -72.7 |
| 沸点/℃ | 44.8 | -10 |
 ,关闭
,关闭 ,使
,使 和氧气一起通过装置
和氧气一起通过装置 进入
进入 中发生反应,反应后的气体进入装置
中发生反应,反应后的气体进入装置 ,装置
,装置 的作用为
的作用为 换为如图所示装置,实验测得
换为如图所示装置,实验测得 的转化率会偏大,原因为
的转化率会偏大,原因为
(2)装置F中
(3)实验结束后的操作顺序为
①待
 充分反应后,熄灭
充分反应后,熄灭 处的酒精灯
处的酒精灯②停止通入

③停止滴加浓硫酸,关闭
 ,打开
,打开
(4)装置B中发生的离子反应方程式为
A.水 B.
 溶液
溶液C.
 溶液 D.饱和
溶液 D.饱和 溶液
溶液(5)反应结束后测得装置
 质量增加mg,装置
质量增加mg,装置 质量增加ng,则该条件下
质量增加ng,则该条件下 的转化率为
的转化率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】粉煤灰是火电厂的大宗固废。以某电厂的粉煤灰为原料(主要含 、
、 和CaO等)提铝的工艺流程如下:
和CaO等)提铝的工艺流程如下:

回答下列问题:
(1)“浸出”时适当升温的主要目的是___________ , 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(2)“浸渣”的主要成分有___________ 。
(3)“沉铝”时,体系中三种物质的溶解度曲线如图所示,加入 沉铝的目的是
沉铝的目的是___________ 。

(4)“焙烧”时,主要反应的化学方程式为___________ 。
(5)“水浸”后得到的“滤液2”可返回___________ 工序循环使用。
(6)实验测得,5.0g粉煤灰( 的质量分数为30%)经浸出、干燥后得到3.0g“浸渣”(
的质量分数为30%)经浸出、干燥后得到3.0g“浸渣”( 的质量分数为8%),
的质量分数为8%), 的浸出率为
的浸出率为___________ 。
 、
、 和CaO等)提铝的工艺流程如下:
和CaO等)提铝的工艺流程如下:
回答下列问题:
(1)“浸出”时适当升温的主要目的是
 发生反应的离子方程式为
发生反应的离子方程式为(2)“浸渣”的主要成分有
(3)“沉铝”时,体系中三种物质的溶解度曲线如图所示,加入
 沉铝的目的是
沉铝的目的是
(4)“焙烧”时,主要反应的化学方程式为
(5)“水浸”后得到的“滤液2”可返回
(6)实验测得,5.0g粉煤灰(
 的质量分数为30%)经浸出、干燥后得到3.0g“浸渣”(
的质量分数为30%)经浸出、干燥后得到3.0g“浸渣”( 的质量分数为8%),
的质量分数为8%), 的浸出率为
的浸出率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】以冶铝的废弃物铝灰为原料制取超细α-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如图:
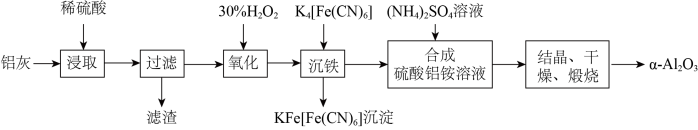
(1)铝灰中氧化铝与硫酸反应的化学方程式为___ 。
(2)图中“滤渣”的主要成分为___ (填化学式)。加30%的H2O2溶液发生的离子反应方程式为2Fe2++H2O2+2H+=2Fe3++2H2O。
(3)验证“沉铁”后,溶液中是否还含有铁离子的操作方法为___ 。
(4)煅烧硫酸铝铵晶体,发生的主要反应为4[NH4Al(SO4)2·12H2O]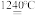 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O。将产生的气体通过如图所示的装置。
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O。将产生的气体通过如图所示的装置。
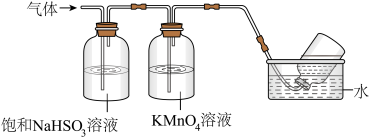
①集气瓶中收集到的气体是___ (填化学式)。
②足量饱和NaHSO3溶液吸收的物质除大部分H2O(g)外还有__ (填化学式)。
③KMnO4溶液褪色(MnO4-还原为Mn2+),发生的离子反应方程式为___ 。

(1)铝灰中氧化铝与硫酸反应的化学方程式为
(2)图中“滤渣”的主要成分为
(3)验证“沉铁”后,溶液中是否还含有铁离子的操作方法为
(4)煅烧硫酸铝铵晶体,发生的主要反应为4[NH4Al(SO4)2·12H2O]
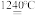 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O。将产生的气体通过如图所示的装置。
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O。将产生的气体通过如图所示的装置。
①集气瓶中收集到的气体是
②足量饱和NaHSO3溶液吸收的物质除大部分H2O(g)外还有
③KMnO4溶液褪色(MnO4-还原为Mn2+),发生的离子反应方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知X、Y、Z、R、W为原子序数依次增大的五种元素,X是原子序数最小的元素;Y元素原子最外层电子数是其内层电子总数的2倍;Z元素原子最外层电子数比其次外层电子数多4;R元素原子最外层有3个电子,其阳离子与Z的阴离子原子核外电子总数相同;W元素原子K层和M层电子总数比其L层电子数多1。回答下列问题:
(1)R元素原子的结构示意图为___________ 。
(2)仅由X、Z、R三种元素形成的化合物的化学式为___________ 。
(3)仅由X与Z元素所形成的化合物的分子式为___________ 和___________ 。
(4)相同条件下﹐密度:
___________ (填“>”、“<”或“=”)YZ,判断的理由为___________ 。
(5)写出 在生活中的一种用途:
在生活中的一种用途:___________ 。
(6)化合物XW与 反应的化学方程式为
反应的化学方程式为___________ 。
(1)R元素原子的结构示意图为
(2)仅由X、Z、R三种元素形成的化合物的化学式为
(3)仅由X与Z元素所形成的化合物的分子式为
(4)相同条件下﹐密度:

(5)写出
 在生活中的一种用途:
在生活中的一种用途:(6)化合物XW与
 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
【推荐1】硫酸铝在造纸、水净化、土壤改良中有着广泛的应用,同时还是泡沫灭火器中的试剂。某化工厂利用含铝废料(成分为A12O3,SiO2及少量FeO∙xFe2O3)制备硫酸铝晶体的工艺流程如下图所示,回答相关问题。
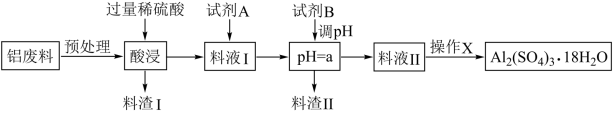
又知生成氢氧化物沉淀的PH如下表:
(1)料渣1的成分是_____________ ,操作X的内容是___________ 、洗涤、干燥等。
(2)试剂B最好是________________ ,a的范围是_________________ ,由表中数据求出Ksp[Fe(OH)3]<__________ (设沉淀完全时金属离子浓度小于1×10-5mol/L)。
(3)试剂A是一种液态绿色氧化剂,料液Ⅰ中反应的离子方程式______________________
(4)泡沫灭火器容器构造分为内外两层,内层是玻璃容器、外层是钢筒。则硫酸铝溶液应盛放在__________ 容器中。
(5)若将该生产流程改为制备铝,则需要在料液Ⅱ中通入足量的氨气,然后过滤、洗涤灼烧,再电解得到铝,请写出通入足量的氨气发生反应的离子方程式______________ ,电解生成铝的化学方程式_____________________

又知生成氢氧化物沉淀的PH如下表:
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.6 | 6.3 | 2.3 |
| 完全沉淀时 | 4.9 | 8.3 | 3.2 |
(1)料渣1的成分是
(2)试剂B最好是
(3)试剂A是一种液态绿色氧化剂,料液Ⅰ中反应的离子方程式
(4)泡沫灭火器容器构造分为内外两层,内层是玻璃容器、外层是钢筒。则硫酸铝溶液应盛放在
(5)若将该生产流程改为制备铝,则需要在料液Ⅱ中通入足量的氨气,然后过滤、洗涤灼烧,再电解得到铝,请写出通入足量的氨气发生反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】高锰酸钾消毒片主要成分为KMnO4,可外用消炎杀菌。用某软锰矿(主要成分是MnO2,还含有Al2O3、SiO2等杂质)制备KMnO4的流程图如下:

已知:K2MnO4固体和溶液均为墨绿色,溶液呈碱性且能发生可逆的歧化反应。
(1)“熔融煅烧”时,MnO2参与反应的化学方程式为________________________________ 。
(2)向“浸取液”中通入CO2,调节其pH,经“过滤”得滤渣I,滤渣I的成分为________ 。
(3)“操作I”中玻璃棒的作用是__________________ 。“操作II”时,当_________ 时,停止加热,自然冷却,抽滤后即可获得紫黑色KMnO4晶体。
(4)“歧化”时,加入冰醋酸的目的是____________________________________ (用必要的离子方程式和文字解释)。
(5)“歧化”时,下列酸可以用来代替冰醋酸的是_________ (填字母)。
a.浓盐酸 b.亚硫酸 c.稀硫酸 d.氢碘酸

已知:K2MnO4固体和溶液均为墨绿色,溶液呈碱性且能发生可逆的歧化反应。
(1)“熔融煅烧”时,MnO2参与反应的化学方程式为
(2)向“浸取液”中通入CO2,调节其pH,经“过滤”得滤渣I,滤渣I的成分为
(3)“操作I”中玻璃棒的作用是
(4)“歧化”时,加入冰醋酸的目的是
(5)“歧化”时,下列酸可以用来代替冰醋酸的是
a.浓盐酸 b.亚硫酸 c.稀硫酸 d.氢碘酸
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】铝渣主要成分为Al2O3,含少量Fe3O4、CuO、PbCO3、MnCO3。 以铝渣为原料制备半导体AlN的基本工艺流程如下图所示。
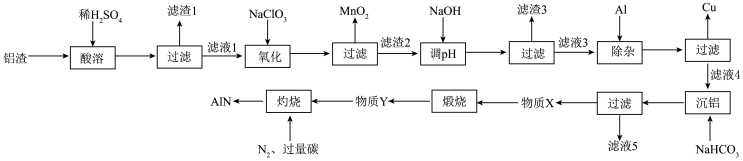
已知:I.“酸溶”时铝渣中金属元素的化合价均未发生变化。
II.“氧化”时锰以及部分铁元素化合价发生了变化。
回答下列问题:
(1)能够加快“酸溶”速率的措施有___________ (答一 条即可), 滤渣1的主要成分是___________ (填化学式) 。
(2)“氧化”时生成MnO2的离子方程式为___________ ;若 “氧化”过程中溶液中n(H+)未变,则铝渣中Fe3O4与MnCO3的物质的量之比为___________ 。
(3)常温下,Ksp[Al(OH)3] =4.0 ×10-33。“氧化” 后滤液2中c(Al3+)= 0.1 mol·L-1,若将滤液2的pH调至3.5,___________ (填 “会”或“不会”)产生Al(OH)3沉淀。
(4)“沉铝”时,反应的离子方程式为____________ ,写出该反应的一个用途___________ 。
(5)“灼烧”时得到AlN的化学方程式为___________ ; 该过程反应后期需通入一定量的空气,其目的是___________ (从提高 AlN纯度角度考虑)。

已知:I.“酸溶”时铝渣中金属元素的化合价均未发生变化。
II.“氧化”时锰以及部分铁元素化合价发生了变化。
回答下列问题:
(1)能够加快“酸溶”速率的措施有
(2)“氧化”时生成MnO2的离子方程式为
(3)常温下,Ksp[Al(OH)3] =4.0 ×10-33。“氧化” 后滤液2中c(Al3+)= 0.1 mol·L-1,若将滤液2的pH调至3.5,
(4)“沉铝”时,反应的离子方程式为
(5)“灼烧”时得到AlN的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】钼是一种过渡金属元素,通常用作合金及不锈钢的添加剂,这种元素可增强 合金的强度、硬度、可焊性及韧性,还可增强其耐高温及耐腐蚀性能。如图是化工生产中 制备金属钼的主要流程图。
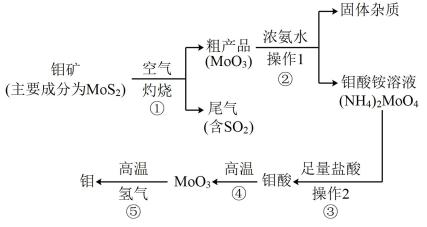
(1)写出在高温下发生反应①的化学方程_________________________________________
(2)生产中用足量的浓氨水吸收反应①的尾气合成肥料,写出该反应的离子方程式:______________________________
(3)如果在实验室模拟操作 1 和操作 2,则需要使用的主要玻璃仪器有______________________________
(4)某同学利用下图所示装置来制备氢气,利用氢气还原三氧化钼,根据要求回答问题:

① 请设计一个实验方案验证 H2的还原性并检验其氧化产物,其装置连接顺序是______________________________
② 在烧瓶 A 中加入少量硫酸铜的目的是_____
③ 两次使用 D 装置,其中所盛的药品依次是_____ 、_____

(1)写出在高温下发生反应①的化学方程
(2)生产中用足量的浓氨水吸收反应①的尾气合成肥料,写出该反应的离子方程式:
(3)如果在实验室模拟操作 1 和操作 2,则需要使用的主要玻璃仪器有
(4)某同学利用下图所示装置来制备氢气,利用氢气还原三氧化钼,根据要求回答问题:

① 请设计一个实验方案验证 H2的还原性并检验其氧化产物,其装置连接顺序是
② 在烧瓶 A 中加入少量硫酸铜的目的是
③ 两次使用 D 装置,其中所盛的药品依次是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】纯碱是重要的化工原料,在医药、冶金、化工、食品等领域被广泛使用。
(1)工业生产纯碱的第一步是除去饱和食盐水的中Mg2+、Ca2+离子,从成本角度考虑加入试剂的化学式为_____ 、_____ 。
某实验小组的同学模拟侯德榜制碱法制取纯碱,流程如图:

已知:几种盐的溶解度
(2)①写出装置I中反应的化学方程式_____ 。
②从平衡移动角度解释该反应发生的原因_____ 。
(3)写出装置II中发生反应的化学方程式_____ 。
(4)请结合化学用语说明装置III中加入磨细的食盐粉及NH3的作用_____ 。
(5)该流程中可循环利用的物质是_____ 。
(6)制出的纯碱中含有杂质NaCl,为测定其纯度,下列方案中不可行的是_____ 。
a.向m克纯碱样品中加入足量CaCl2溶液,测生成CaCO3的质量
b.向m克纯碱样品中加入足量稀H2SO4,干燥后测生成气体的体积
c.向m克纯碱样品中加入足量AgNO3溶液,测生成沉淀的质量
(1)工业生产纯碱的第一步是除去饱和食盐水的中Mg2+、Ca2+离子,从成本角度考虑加入试剂的化学式为
某实验小组的同学模拟侯德榜制碱法制取纯碱,流程如图:

已知:几种盐的溶解度
| NaCl | NH4HCO3 | NaHCO3 | NH4Cl | |
| 溶解度(20℃,100gH2O时) | 36.0 | 21.7 | 9.6 | 37.2 |
②从平衡移动角度解释该反应发生的原因
(3)写出装置II中发生反应的化学方程式
(4)请结合化学用语说明装置III中加入磨细的食盐粉及NH3的作用
(5)该流程中可循环利用的物质是
(6)制出的纯碱中含有杂质NaCl,为测定其纯度,下列方案中不可行的是
a.向m克纯碱样品中加入足量CaCl2溶液,测生成CaCO3的质量
b.向m克纯碱样品中加入足量稀H2SO4,干燥后测生成气体的体积
c.向m克纯碱样品中加入足量AgNO3溶液,测生成沉淀的质量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氮化铬(CrN)是一种耐磨性良好的新型材料,难溶于水。探究小组同学用如图所示装置(夹持装置略去)在实验室中制取氮化铬并测定所得氮化铬的纯度。

已知:实验室中常用NH4Cl溶液与NaNO2溶液反应制取N2;CrCl3能溶于水和乙醇,高温下能被氧气氧化。
回答下列问题:
(1)实验装置中盛放饱和氯化铵溶液的仪器名称是_______ ,实验准备就绪后,装置A和装置E应先加热的是_______ (填“装置A”或“装置E”),原因是_______ 。
(2)写出装置E中发生反应的化学方程式_______ 。实验过程中需间歇性微热b处导管的目的是_______ 。
(3)为了测所得CrN纯度,把7.0g所得产品中加入足量NaOH溶液,然后通入水蒸气将NH3全部蒸出,将NH3用60mL1lmol·L-1H2SO4溶液完全吸收,剩余的H2SO4用2mol·L-1NaOH滴定,消耗NaOH溶液10mL。
①滴定管使用的正确的操作顺序为:蒸馏水洗涤→标准液润洗→_______ →洗净→放回滴定管架(填字母)。
a.滴定结束后,记录刻度
b.调节液面至0刻度或0刻度略靠下,记录刻度
c.装入标准液并排净尖嘴处的气泡
d.将未滴定完的标准液回收
②所得产品中CrN的质量分数为_______ (用百分数表示,保留一位小数)。

已知:实验室中常用NH4Cl溶液与NaNO2溶液反应制取N2;CrCl3能溶于水和乙醇,高温下能被氧气氧化。
回答下列问题:
(1)实验装置中盛放饱和氯化铵溶液的仪器名称是
(2)写出装置E中发生反应的化学方程式
(3)为了测所得CrN纯度,把7.0g所得产品中加入足量NaOH溶液,然后通入水蒸气将NH3全部蒸出,将NH3用60mL1lmol·L-1H2SO4溶液完全吸收,剩余的H2SO4用2mol·L-1NaOH滴定,消耗NaOH溶液10mL。
①滴定管使用的正确的操作顺序为:蒸馏水洗涤→标准液润洗→
a.滴定结束后,记录刻度
b.调节液面至0刻度或0刻度略靠下,记录刻度
c.装入标准液并排净尖嘴处的气泡
d.将未滴定完的标准液回收
②所得产品中CrN的质量分数为
您最近一年使用:0次



