以冶铝的废弃物铝灰为原料制取超细α-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如图:
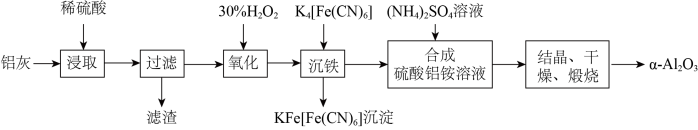
(1)铝灰中氧化铝与硫酸反应的化学方程式为___ 。
(2)图中“滤渣”的主要成分为___ (填化学式)。加30%的H2O2溶液发生的离子反应方程式为2Fe2++H2O2+2H+=2Fe3++2H2O。
(3)验证“沉铁”后,溶液中是否还含有铁离子的操作方法为___ 。
(4)煅烧硫酸铝铵晶体,发生的主要反应为4[NH4Al(SO4)2·12H2O]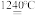 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O。将产生的气体通过如图所示的装置。
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O。将产生的气体通过如图所示的装置。
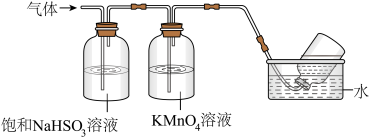
①集气瓶中收集到的气体是___ (填化学式)。
②足量饱和NaHSO3溶液吸收的物质除大部分H2O(g)外还有__ (填化学式)。
③KMnO4溶液褪色(MnO4-还原为Mn2+),发生的离子反应方程式为___ 。

(1)铝灰中氧化铝与硫酸反应的化学方程式为
(2)图中“滤渣”的主要成分为
(3)验证“沉铁”后,溶液中是否还含有铁离子的操作方法为
(4)煅烧硫酸铝铵晶体,发生的主要反应为4[NH4Al(SO4)2·12H2O]
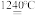 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O。将产生的气体通过如图所示的装置。
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O。将产生的气体通过如图所示的装置。
①集气瓶中收集到的气体是
②足量饱和NaHSO3溶液吸收的物质除大部分H2O(g)外还有
③KMnO4溶液褪色(MnO4-还原为Mn2+),发生的离子反应方程式为
更新时间:2020-05-12 14:20:47
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】粉煤灰是火电厂的大宗固废。以某电厂的粉煤灰为原料(主要含 、
、 和CaO等)提铝的工艺流程如下:
和CaO等)提铝的工艺流程如下:

回答下列问题:
(1)“浸出”时适当升温的主要目的是___________ , 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(2)“浸渣”的主要成分有___________ 。
(3)“沉铝”时,体系中三种物质的溶解度曲线如图所示,加入 沉铝的目的是
沉铝的目的是___________ 。

(4)“焙烧”时,主要反应的化学方程式为___________ 。
(5)“水浸”后得到的“滤液2”可返回___________ 工序循环使用。
(6)实验测得,5.0g粉煤灰( 的质量分数为30%)经浸出、干燥后得到3.0g“浸渣”(
的质量分数为30%)经浸出、干燥后得到3.0g“浸渣”( 的质量分数为8%),
的质量分数为8%), 的浸出率为
的浸出率为___________ 。
 、
、 和CaO等)提铝的工艺流程如下:
和CaO等)提铝的工艺流程如下:
回答下列问题:
(1)“浸出”时适当升温的主要目的是
 发生反应的离子方程式为
发生反应的离子方程式为(2)“浸渣”的主要成分有
(3)“沉铝”时,体系中三种物质的溶解度曲线如图所示,加入
 沉铝的目的是
沉铝的目的是
(4)“焙烧”时,主要反应的化学方程式为
(5)“水浸”后得到的“滤液2”可返回
(6)实验测得,5.0g粉煤灰(
 的质量分数为30%)经浸出、干燥后得到3.0g“浸渣”(
的质量分数为30%)经浸出、干燥后得到3.0g“浸渣”( 的质量分数为8%),
的质量分数为8%), 的浸出率为
的浸出率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】铝土矿的主要成分是Al2O3,含有杂SiO2,Fe2O3,MgO。工业上从铝土矿中提取铝可采用如下工艺流程(已知SiO2不与盐酸反应):
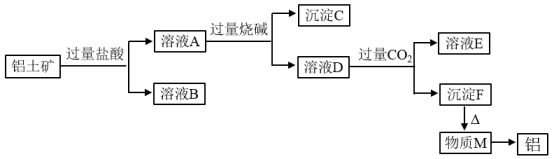
请回答下列问题:
(1)图中涉及分离溶液与沉淀的实验方法是______ (填操作名称)。
(2)沉淀B的成分是___________ (填化学式,下同),沉淀C的成分是________ ;溶液D中所含的酸根离子是________ 。
(3)沉淀F转化为物质M的化学方程式为______ ;溶液D中通入过量CO2生成沉淀F的离子方程式为___________ 。
(4)能否将向溶液D中通入过量CO2换成加入过量盐酸?_______ (填“能”或“不能”)其理由是________ 。

请回答下列问题:
(1)图中涉及分离溶液与沉淀的实验方法是
(2)沉淀B的成分是
(3)沉淀F转化为物质M的化学方程式为
(4)能否将向溶液D中通入过量CO2换成加入过量盐酸?
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】聚合氯化铝晶体是介于AlCl3和A1(OH)3之间的一种水溶性无机高分子聚合物,其制备原料主要是铝加工行业的废渣——铝灰,它主要含Al2O3、Al,还有SiO2等杂质。聚合氯化铝生产工艺流程如图:

(1)反应中副产品a是___ (用化学式表示);
(2)升高pH至4.0~4.5的目的是__ ;
(3)生产过程中可循环使用的物质是__ (用化学式表示);
(4)为使得到的晶体较纯净,生产过程中使pH升高的C物质可选用___ (填编号);
a.NaOH b.Al c.氨水 d.A12O3 e.NaAlO2

(1)反应中副产品a是
(2)升高pH至4.0~4.5的目的是
(3)生产过程中可循环使用的物质是
(4)为使得到的晶体较纯净,生产过程中使pH升高的C物质可选用
a.NaOH b.Al c.氨水 d.A12O3 e.NaAlO2
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上用铝土矿 主要成分为
主要成分为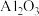 ,还有少量的
,还有少量的 ,
, 等杂质
等杂质 提取氧化铝作冶炼铝的原料,提取的操作过程如下:
提取氧化铝作冶炼铝的原料,提取的操作过程如下:
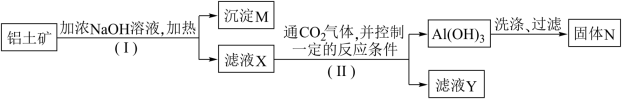
(1) 和II步骤中分离溶液和沉淀的操作是:
和II步骤中分离溶液和沉淀的操作是:__________________ ;
(2)沉淀M中除含有泥沙外,一定还含有____________ ,固体N是____________ ;
(3)滤液X中,含铝元素的溶质的化学式为________________ ,它属于_____  填“酸”、“碱”或“盐”
填“酸”、“碱”或“盐” 类物质;
类物质;
(4)实验室里常往 溶液中加入
溶液中加入________________  填“氨水”或“NaOH溶液”
填“氨水”或“NaOH溶液” 来制取
来制取 ,请写出该反应的方程式
,请写出该反应的方程式___________________________
 主要成分为
主要成分为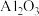 ,还有少量的
,还有少量的 ,
, 等杂质
等杂质 提取氧化铝作冶炼铝的原料,提取的操作过程如下:
提取氧化铝作冶炼铝的原料,提取的操作过程如下:
(1)
 和II步骤中分离溶液和沉淀的操作是:
和II步骤中分离溶液和沉淀的操作是:(2)沉淀M中除含有泥沙外,一定还含有
(3)滤液X中,含铝元素的溶质的化学式为
 填“酸”、“碱”或“盐”
填“酸”、“碱”或“盐” 类物质;
类物质;(4)实验室里常往
 溶液中加入
溶液中加入 填“氨水”或“NaOH溶液”
填“氨水”或“NaOH溶液” 来制取
来制取 ,请写出该反应的方程式
,请写出该反应的方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】以废旧锂离子电池的正极材料(主要含 ,还含Al、塑料等杂质)为原料提取草酸钴(
,还含Al、塑料等杂质)为原料提取草酸钴( )的流程如图。回答下列问题:
)的流程如图。回答下列问题:

已知每一步加入的试剂都是过量的。
(1)“灼烧”的目的是
(2)“碱浸”的离子方程式为
(3)“浸渣”的主要成分是
 ,“酸溶”的化学方程式为
,“酸溶”的化学方程式为(4)整个流程中有
(5)在空气中加热
 ,其失重图如图。a点对应固体的成分是
,其失重图如图。a点对应固体的成分是 段固体质量减小的原因是
段固体质量减小的原因是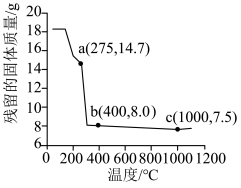
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】五氧化二钒(V2O5)广泛用于冶金、化工等行业。一种以含钒废料(含V2O5、MnO、SiO2、Al2O3)为原料制备V2O5的流程如下:

已知:V2O3难溶于水和碱,可溶于酸,灼烧可生成V2O5。
(1)为提高含钒废料的浸取率,可采取的措施为___________ 。
(2)“滤液1”中除了含有过量的NaOH,还含有的溶质为___________ (填化学式)。
(3)“烘干灼烧”的目的是___________ 。
(4)“沉锰”时需将温度控制在70℃左右,温度不能过高的原因为___________ ,“滤渣2”的主要成分是MnCO3,写出生成MnCO3的离子方程式:___________ 。
(5)“浓缩结晶”后获得NH4VO3晶体需进行的操作是___________ 。证明NH4VO3已洗涤干净的实验操作及现象为___________ 。
(6)在煅烧NH4VO3生成 V2O5的过程中无元素化合价变化,请写出反应的化学方程式:___________ 。

已知:V2O3难溶于水和碱,可溶于酸,灼烧可生成V2O5。
(1)为提高含钒废料的浸取率,可采取的措施为
(2)“滤液1”中除了含有过量的NaOH,还含有的溶质为
(3)“烘干灼烧”的目的是
(4)“沉锰”时需将温度控制在70℃左右,温度不能过高的原因为
(5)“浓缩结晶”后获得NH4VO3晶体需进行的操作是
(6)在煅烧NH4VO3生成 V2O5的过程中无元素化合价变化,请写出反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】Ⅰ.以黄铁矿(主要成分FeS2)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
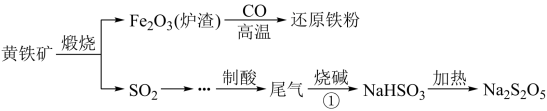
(1)黄铁矿中硫元素的化合价为___________ ;
(2)欲得到更纯的NaHSO3,反应①应通入___________ (填 “过量”或“不足量”)的SO2气体;
(3)因为Na2S2O5具有还原性,导致商品Na2S2O5中不可避免地存在Na2SO4,检验其中含有SO 的方法是
的方法是___________ 。
Ⅱ.黄铁矿煅烧后得到的炉渣(含Fe2O3、FeO、SiO2及Al2O3),还可以用来生产一种高效混凝剂聚合硫酸铁铝硅,工艺流程如下:

已知:mCaO·nAl2O3难溶于水。
(4)“过滤”所得滤渣为___________ (填化学式);
(5)“氧化”时发生反应的离子方程式为___________ ;
(6)“调节碱化度”时,mCaO·nAl2O3与溶液中H+反应的离子方程式为___________ 。

(1)黄铁矿中硫元素的化合价为
(2)欲得到更纯的NaHSO3,反应①应通入
(3)因为Na2S2O5具有还原性,导致商品Na2S2O5中不可避免地存在Na2SO4,检验其中含有SO
 的方法是
的方法是Ⅱ.黄铁矿煅烧后得到的炉渣(含Fe2O3、FeO、SiO2及Al2O3),还可以用来生产一种高效混凝剂聚合硫酸铁铝硅,工艺流程如下:

已知:mCaO·nAl2O3难溶于水。
(4)“过滤”所得滤渣为
(5)“氧化”时发生反应的离子方程式为
(6)“调节碱化度”时,mCaO·nAl2O3与溶液中H+反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】乙酸苯酯是一种有机化合物,分子式为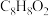 ,可用作溶剂和有机合成的中间体,实验室用如下方法制备乙酸苯酯:
,可用作溶剂和有机合成的中间体,实验室用如下方法制备乙酸苯酯:

a.将 苯酚加入适量质量分数约为
苯酚加入适量质量分数约为 的氢氧化钠溶液中,搅拌溶解配制成苯酚钠溶液。
的氢氧化钠溶液中,搅拌溶解配制成苯酚钠溶液。
b.将苯酚钠溶液全部转移至容器内,加入 乙酸酐(
乙酸酐( ),水浴加热,使反应体系保持微沸,回流搅拌4小时后停止加热,将混合液倒入
),水浴加热,使反应体系保持微沸,回流搅拌4小时后停止加热,将混合液倒入 水中,分液,再加入饱和碳酸钠溶液洗涤,再用水洗涤分液,收集有机层。在有机层中加入无水乙醚和少量无水氯化钙,静置片刻,过滤。将滤液进行蒸馏,得到乙酸苯酯
水中,分液,再加入饱和碳酸钠溶液洗涤,再用水洗涤分液,收集有机层。在有机层中加入无水乙醚和少量无水氯化钙,静置片刻,过滤。将滤液进行蒸馏,得到乙酸苯酯 。
。
已知,有关有机物的信息如下表:
回答下列问题:
(1)仪器a中支管甲的作用是___________ ,仪器b的冷凝水从___________ (填“上”或“下”)口进,仪器c的名称为___________ ;与直接加热相比,水浴加热的优点为___________ 。
(2)苯酚的俗名为___________ ,苯酚与 溶液反应的化学方程式为
溶液反应的化学方程式为___________ 。
(3)乙酸苯酯的结构简式为___________ ,加入饱和碳酸钠溶液洗涤的目的是___________ 。
(4)本实验中,乙酸苯酯的产率是___________ (保留两位有效数字)%。
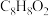 ,可用作溶剂和有机合成的中间体,实验室用如下方法制备乙酸苯酯:
,可用作溶剂和有机合成的中间体,实验室用如下方法制备乙酸苯酯:
a.将
 苯酚加入适量质量分数约为
苯酚加入适量质量分数约为 的氢氧化钠溶液中,搅拌溶解配制成苯酚钠溶液。
的氢氧化钠溶液中,搅拌溶解配制成苯酚钠溶液。b.将苯酚钠溶液全部转移至容器内,加入
 乙酸酐(
乙酸酐( ),水浴加热,使反应体系保持微沸,回流搅拌4小时后停止加热,将混合液倒入
),水浴加热,使反应体系保持微沸,回流搅拌4小时后停止加热,将混合液倒入 水中,分液,再加入饱和碳酸钠溶液洗涤,再用水洗涤分液,收集有机层。在有机层中加入无水乙醚和少量无水氯化钙,静置片刻,过滤。将滤液进行蒸馏,得到乙酸苯酯
水中,分液,再加入饱和碳酸钠溶液洗涤,再用水洗涤分液,收集有机层。在有机层中加入无水乙醚和少量无水氯化钙,静置片刻,过滤。将滤液进行蒸馏,得到乙酸苯酯 。
。已知,有关有机物的信息如下表:
| 化学式 | 密度/ | 沸点/ | 溶解性 |
| 苯酚 | 1.07 | 182 | 常温下微溶于水,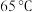 以上与水混溶,易溶于有机溶剂 以上与水混溶,易溶于有机溶剂 |
| 乙酸酐 | 1.08 | 140 | 易容于有机溶剂,与水反应生成乙酸 |
| 乙酸 | 1.05 | 118 | 易溶于水和乙醇 |
| 乙酸苯酯 | 1.08 | 196 | 能与乙醇、乙醚、氯仿和乙酸混溶,几乎不溶于水 |
| 乙醚 | 0.714 | 34.5 | 难溶于水 |
(1)仪器a中支管甲的作用是
(2)苯酚的俗名为
 溶液反应的化学方程式为
溶液反应的化学方程式为(3)乙酸苯酯的结构简式为
(4)本实验中,乙酸苯酯的产率是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】碘被称为“智力元素”,科学合理地补充碘可防治碘缺乏病,KI、KIO3曾先后用于加碘盐中。KI还可用于分析试剂、感光材料、制药等,其制备原理如下:
反应I : 3I2+ 6KOH= KIO3 +5KI+ 3H2O
反应II: 3H2S+KIO3=3S↓+KI+ 3H2O

请回答有关问题。
(1)启普发生器中发生反应的化学方程式是_______ ,装置中盛装30%氢氧化钾溶液的仪器名称是_______ ;
(2)关闭启普发生器活塞,先滴入30%的KOH溶液。待观察到三颈烧瓶中溶液颜色由棕黄色变为无色 ,停止滴入KOH溶液;然后_______ (填操作),待三颈烧瓶和烧杯中产生气泡的速率接近相等时停止通气。
(3)把三颈烧瓶中的溶液倒入烧杯中,加入碳酸钡,在过滤器中过滤,过滤得到的沉淀中除含有过量碳酸钡外,还含有硫酸钡和_______ (填名称)。合并滤液和洗涤液,蒸发至析出结晶,干燥得成品。
(4)实验室模拟工业制备KIO3流程如下:

几种物质的溶解度见下表:
①由上表数据分析可知,“操作a”是_______ ;
②用惰性电极电解KI溶液也能制备KIO3,与电解法相比,上述流程制备KIO3的缺点是_______
(5)某同学为了测定上述流程生产的KIO3样品的纯度,进行了下列操作:
取1.00 g样品溶于蒸馏水中并用硫酸酸化,再加入过量的KI和少量的淀粉溶液,逐滴滴加2.0 mol·L-1 Na2S2O3溶液,恰好完全反应时共消耗12. 60 mL Na2S2O3溶液。该样品中KIO3的质量分数为_______ (已知反应:I2+2Na2S2O3=2NaI+Na2S4O6)。
反应I : 3I2+ 6KOH= KIO3 +5KI+ 3H2O
反应II: 3H2S+KIO3=3S↓+KI+ 3H2O

请回答有关问题。
(1)启普发生器中发生反应的化学方程式是
(2)关闭启普发生器活塞,先滴入30%的KOH溶液。待观察到三颈烧瓶中溶液颜色由棕黄色变为无色 ,停止滴入KOH溶液;然后
(3)把三颈烧瓶中的溶液倒入烧杯中,加入碳酸钡,在过滤器中过滤,过滤得到的沉淀中除含有过量碳酸钡外,还含有硫酸钡和
(4)实验室模拟工业制备KIO3流程如下:

几种物质的溶解度见下表:
| KCl | KH(IO3)2 | KClO3 | |
| 25℃时的溶解度(g) | 20.8 | 0.8 | 7.5 |
| 80℃时的溶解度(g) | 37.1 | 12.4 | 16.2 |
②用惰性电极电解KI溶液也能制备KIO3,与电解法相比,上述流程制备KIO3的缺点是
(5)某同学为了测定上述流程生产的KIO3样品的纯度,进行了下列操作:
取1.00 g样品溶于蒸馏水中并用硫酸酸化,再加入过量的KI和少量的淀粉溶液,逐滴滴加2.0 mol·L-1 Na2S2O3溶液,恰好完全反应时共消耗12. 60 mL Na2S2O3溶液。该样品中KIO3的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】化学是最具有应用价值的学科,为人类生存与繁衍担当了巨大的“社会责任”。
Ⅰ.硝酸铵是一种常用的化肥,也是重要的化工原料。常见工业制备方法如下图所示:
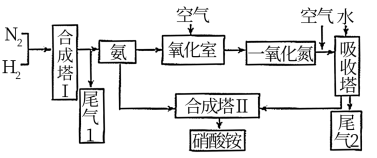
(1)氧化室中发生反应的化学方程式为:___________ 。
(2)尾气1的处理方法是:___________ 。
(3)在气体进入吸收塔前再次通入空气的目的是:___________ 。
Ⅱ.利用工业尾气(含硫氧化物与氮氧化物)制备 ,实现了“变废为宝”并保护了自然环境。下图是相关的工艺流程(Ce为铈元素):
,实现了“变废为宝”并保护了自然环境。下图是相关的工艺流程(Ce为铈元素):

请回答下列问题:
(4)气体1的化学式是:___________ 。
(5) 发生的反应类型是:
发生的反应类型是:___________ 。
(6)若溶液1呈酸性,则装置1中发生反应的离子方程式是:___________ 。
(7)最后要形成粗产品 晶体,实验操作依次为(不少于3个术语):
晶体,实验操作依次为(不少于3个术语):___________ 等。
Ⅰ.硝酸铵是一种常用的化肥,也是重要的化工原料。常见工业制备方法如下图所示:

(1)氧化室中发生反应的化学方程式为:
(2)尾气1的处理方法是:
(3)在气体进入吸收塔前再次通入空气的目的是:
Ⅱ.利用工业尾气(含硫氧化物与氮氧化物)制备
 ,实现了“变废为宝”并保护了自然环境。下图是相关的工艺流程(Ce为铈元素):
,实现了“变废为宝”并保护了自然环境。下图是相关的工艺流程(Ce为铈元素):
请回答下列问题:
(4)气体1的化学式是:
(5)
 发生的反应类型是:
发生的反应类型是:(6)若溶液1呈酸性,则装置1中发生反应的离子方程式是:
(7)最后要形成粗产品
 晶体,实验操作依次为(不少于3个术语):
晶体,实验操作依次为(不少于3个术语):
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】氨基甲酸铵(H2 NCOONH4)是一种白色晶体,是常见的实验药品,可由干燥的NH3和干燥的CO2在任何比例下反应得到每生成1.0g氨基甲酸铵放出2.05kJ的热量。回答下列问题:
(1)实验室可选用下列装置(I~V)制备干燥的NH3和CO2。

①用装置I、Ⅲ制备并纯化NH3时,接口a与________________ (填接口字母)相连,装置I中发生反应的化学方程式为________________________ 。
②制备并纯化CO2时,按气流从左至右的方向,各接口连接顺序为________________ (填接口字母)
(2)一种制备氨基甲酸铵的改进实验装置如下图所示:

①用仪器W代替分液漏斗的优点是________________________ ;用干冰装置代替(1)中制备并纯化CO2装置的优点是________________________ 。
②“薄膜反应器”中发生反应的热化学方程式为________________________ ;盛浓硫酸的装置的作用是________________________________ (列举2点)。
③体系中若有水蒸气,还可能生成的铵盐是________________________ (填化学式)。
(1)实验室可选用下列装置(I~V)制备干燥的NH3和CO2。

①用装置I、Ⅲ制备并纯化NH3时,接口a与
②制备并纯化CO2时,按气流从左至右的方向,各接口连接顺序为
(2)一种制备氨基甲酸铵的改进实验装置如下图所示:

①用仪器W代替分液漏斗的优点是
②“薄膜反应器”中发生反应的热化学方程式为
③体系中若有水蒸气,还可能生成的铵盐是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氧族元素(O、S、Se等)及其化合物在生产生活中发挥着巨大作用。
(1)实验室用70%H2SO4溶液和Na2SO3粉末在常温下反应制备SO2,装置如下图。

①将虚线框a内的仪器补充完整___________ (夹持装置可省略)。
②b为尾气吸收装置,其中的试剂为___________ 。
(2)生物浸出法可有效回收含硫矿石中的有色金属,某种生物浸出法中主要物质的转化路径如下图。

①步骤I反应的离子方程式为___________ 。
②生物浸出时的总反应的氧化剂是___________ 。
(3)硒是一种抗癌元素,湖北恩施称之为硒都,以工业硒为原料制备高纯硒的流程如下图。
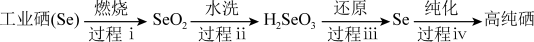
①下列说法正确的是___________ (填字母序号)。
a.过程i到过程iii均为氧化还原反应
b.H2SeO3既有氧化性,又有还原性
c.SeO2能与NaOH反应生成Na2SeO3和H2O
d.Se与H2化合比S与H2化合容易
②过程iii中使用的还原剂为N2H4·nH2O,对应产物是N2,理论上,过程i消耗的O2与过程iii消耗的N2H4·nH2O的物质的量之比为___________ (工业硒中杂质与O2的反应可忽略)。
(1)实验室用70%H2SO4溶液和Na2SO3粉末在常温下反应制备SO2,装置如下图。

①将虚线框a内的仪器补充完整
②b为尾气吸收装置,其中的试剂为
(2)生物浸出法可有效回收含硫矿石中的有色金属,某种生物浸出法中主要物质的转化路径如下图。

①步骤I反应的离子方程式为
②生物浸出时的总反应的氧化剂是
(3)硒是一种抗癌元素,湖北恩施称之为硒都,以工业硒为原料制备高纯硒的流程如下图。
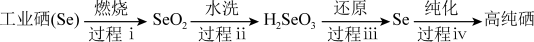
①下列说法正确的是
a.过程i到过程iii均为氧化还原反应
b.H2SeO3既有氧化性,又有还原性
c.SeO2能与NaOH反应生成Na2SeO3和H2O
d.Se与H2化合比S与H2化合容易
②过程iii中使用的还原剂为N2H4·nH2O,对应产物是N2,理论上,过程i消耗的O2与过程iii消耗的N2H4·nH2O的物质的量之比为
您最近一年使用:0次



