已知蓝铜矿的主要成分是2CuCO3·Cu(OH)2,受热易分解。铝土矿的主要成分是Al2O3、Fe2O3、SiO2。经过一定条件的转化二者均可转化为金属单质,根据下列框图转化回答问题:
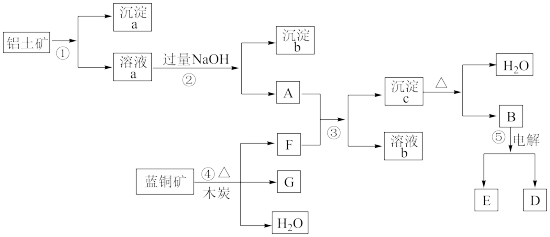
(1)写出①的离子方程式:______________________ 、_____________________ 。
(2)经过④、⑤步反应得到铜和金属铝,写出反应的化学方程式:
________________________________ 、_________________________________ 。
(3)若过量F与A反应,溶液b的成分是:_____________ (写化学式)。

(1)写出①的离子方程式:
(2)经过④、⑤步反应得到铜和金属铝,写出反应的化学方程式:
(3)若过量F与A反应,溶液b的成分是:
9-10高一下·广东梅州·期末 查看更多[1]
(已下线)09—10年梅州市曾宪梓中学高一下学期期末考试化学卷
更新时间:2016-12-09 00:45:31
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】固体化合物X由四种常见的元素组成,为探究其成分,某学生进行如下实验:
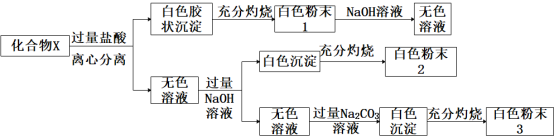
①20.8gX固体进行实验,得到白色粉末1质量12.0g,白色粉末2质量为6.0g;
②白色粉末2可用作耐高温材料,白色粉末3是一种常见干燥剂;请回答问题:
(1)X中金属元素的名称是______ 。
(2)化合物X与足量盐酸反应离子方程式______ 。
(3)在高温条件下,白色粉末2中某元素单质与白色粉末1反应,是工业制备另一种单质方法之一,写出该反应的化学方程式______ 。

①20.8gX固体进行实验,得到白色粉末1质量12.0g,白色粉末2质量为6.0g;
②白色粉末2可用作耐高温材料,白色粉末3是一种常见干燥剂;请回答问题:
(1)X中金属元素的名称是
(2)化合物X与足量盐酸反应离子方程式
(3)在高温条件下,白色粉末2中某元素单质与白色粉末1反应,是工业制备另一种单质方法之一,写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】将晶体X加热分解可得A、B、D、E、F和水六种产物,其中A、B、D都是中学化学中常见的氧化物,气体E是单质F所含元素的氢化物。
(1)A能溶于强酸、强碱,写出A与强碱溶液反应的离子方程式:____________________ 。
(2)B、D都是酸性氧化物且组成元素相同,D溶于水得强酸,则B、D分子中除氧元素外所含另一种元素在元素周期表中的位置是______________________ 。
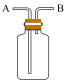
(3)E能使湿润的红色石蕊试纸变蓝,实验室制取E气体的化学方程式为___________ ,制得的气体可用如图所示装置收集,则气体应从______ (填“A”或“B”)通入。
(4)由各分解产物的物质的量之比推测X的组成类似于明矾,若向X的浓溶液中滴加浓NaOH溶液至过量,现象依次为__________ 、____________ 、________ 。
(5)取一定量的X晶体分解,若生成1 mol F,则必同时生成____________ (填化学式)________ mol。
(1)A能溶于强酸、强碱,写出A与强碱溶液反应的离子方程式:
(2)B、D都是酸性氧化物且组成元素相同,D溶于水得强酸,则B、D分子中除氧元素外所含另一种元素在元素周期表中的位置是
(3)E能使湿润的红色石蕊试纸变蓝,实验室制取E气体的化学方程式为

(4)由各分解产物的物质的量之比推测X的组成类似于明矾,若向X的浓溶液中滴加浓NaOH溶液至过量,现象依次为
(5)取一定量的X晶体分解,若生成1 mol F,则必同时生成
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有金属单质A、B、C、I和气体甲、乙、丙及物质D、E、F、G、H。其中B是地壳中含量最多的金属。它们之间能发生如图反应(图中有些反应的产物和条件没有全部标出),回答下列问题:
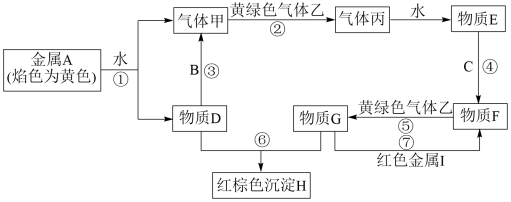
(1)H的化学式:____ ;实验室检验物质D中阳离子的方法是____ 。
(2)写出反应⑦的离子方程式:____ ,写出物质F在酸性条件下和双氧水发生的离子反应方程式____ 。
(3)若G只含有一种金属阳离子,请用离子方程式表示检验该金属阳离子的原理____ 。

(1)H的化学式:
(2)写出反应⑦的离子方程式:
(3)若G只含有一种金属阳离子,请用离子方程式表示检验该金属阳离子的原理
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】以冶铝的废弃物铝灰为原料制取超细α氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下图:
(1)写出铝灰与氢氧化钠溶液反应涉及的化学方程式:_______________________ 。
(2)加30%H2O2溶液发生的离子反应方程式为______________________________ 。
(3)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O] 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置。
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置。
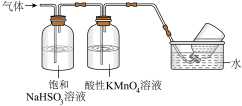
集气瓶中收集到的气体是_______ (填化学式)。
②酸性KMnO4溶液紫色变浅_______ (填“能”或“不能”)说明煅烧硫酸铝铵晶体产物中含有SO2气体?理由:______ 。
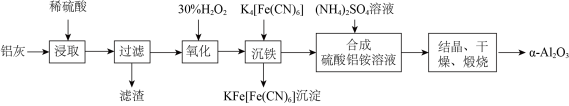
(1)写出铝灰与氢氧化钠溶液反应涉及的化学方程式:
(2)加30%H2O2溶液发生的离子反应方程式为
(3)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O]
 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置。
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置。
集气瓶中收集到的气体是
②酸性KMnO4溶液紫色变浅
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】煤矿筛选煤后废弃的煤矸石主要含有SiO2、Al2O3、Fe2O3。某实验常用煤矸石提取氧化铝,设计实验流程如图:
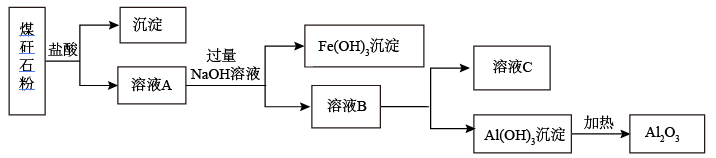
(1)将煤矸石粉碎的目的是_____________ 。
(2)步骤(Ⅰ)中溶液A和沉淀分离的操作名称是__________ ,沉淀的化学式为_____________ 。
(3)步骤(Ⅱ)中加入NaOH需过量的目的是______________ 。
(4)已知步骤(Ⅲ)中溶液C的溶质为NaHCO3,该反应的化学方程式为______________ 。
(5)步骤(Ⅳ)中Al(OH)3受热分解的化学方程式为______________ 。

(1)将煤矸石粉碎的目的是
(2)步骤(Ⅰ)中溶液A和沉淀分离的操作名称是
(3)步骤(Ⅱ)中加入NaOH需过量的目的是
(4)已知步骤(Ⅲ)中溶液C的溶质为NaHCO3,该反应的化学方程式为
(5)步骤(Ⅳ)中Al(OH)3受热分解的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铝土矿的主要成分是Al2O3,含有杂质SiO2、Fe2O3、MgO。工业上从铝土矿中提取Al可采用如图所示工艺流程:
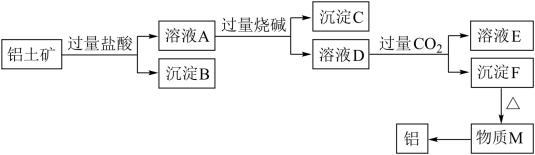
请回答下列问题:
(1)铝土矿加入盐酸后生成Al3+的离子方程式为_____________________________ 。
(2)沉淀B与烧碱反应的离子方程式为______________________________________ 。
(3)溶液D中通入过量CO2的离子方程式为_____________________________ 。
(4)“通入过量CO2”能否改用过量盐酸________ (填“能或否”),原因是_____________ 。
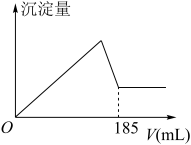
(5)向共含有0.05mol Al3+、Fe3+的溶液中滴入1mol/L NaOH 溶液,生成沉淀的量与加入NaOH 溶液的体积关系如图所示。 则溶液中Al3+的物质的量为_________ mol。

请回答下列问题:
(1)铝土矿加入盐酸后生成Al3+的离子方程式为
(2)沉淀B与烧碱反应的离子方程式为
(3)溶液D中通入过量CO2的离子方程式为
(4)“通入过量CO2”能否改用过量盐酸
(5)向共含有0.05mol Al3+、Fe3+的溶液中滴入1mol/L NaOH 溶液,生成沉淀的量与加入NaOH 溶液的体积关系如图所示。 则溶液中Al3+的物质的量为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、X均为中学化学常见的物质。它们之间存在如下图所示转化关系(图中反应条件略去)填写下列空白:
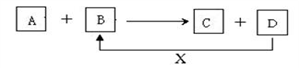
(1)若A为两性氢氧化物, B为NaOH溶液,写出反应A+B→C+D的离子方程式_________ ,并写出偏铝酸钠溶液中通入过量二氧化碳的离子方程式________________________
(2)若A为金属单质,B、C、D都是化合物,A与B发生的反应常用于刻制印刷电路板,该反应的离子方程式__________________ 。

(1)若A为两性氢氧化物, B为NaOH溶液,写出反应A+B→C+D的离子方程式
(2)若A为金属单质,B、C、D都是化合物,A与B发生的反应常用于刻制印刷电路板,该反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】工业上以铝土矿(主要成分为 ,含少量
,含少量 、FeO、
、FeO、 等杂质)为主要原料制备氧化铝,流程如下。
等杂质)为主要原料制备氧化铝,流程如下。 溶液浸取铝土矿中的铝元素和铁元素,
溶液浸取铝土矿中的铝元素和铁元素, 溶液的用量不宜过量太多,其原因是
溶液的用量不宜过量太多,其原因是___________ 。
(2)氧化:用 溶液将
溶液将 氧化为
氧化为 ,反应的离子方程式为
,反应的离子方程式为___________ 。
(3)沉淀:用1mol/L 溶液调节pH,将
溶液调节pH,将 、
、 转化为沉淀。溶液终点pH对铝、铁沉淀率的影响如图所示。
转化为沉淀。溶液终点pH对铝、铁沉淀率的影响如图所示。___________ 。
②实验室需要1mol/L 溶液450mL,配制时需要使用的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和
溶液450mL,配制时需要使用的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和___________ 。
③检验 沉淀完全的操作为:静置,
沉淀完全的操作为:静置,___________ 。
(4)碱溶:用NaOH溶液溶解沉淀,分离出 。
。
①该反应的离子方程式为:___________ 。
②下列措施中能提高单位时间内铝元素浸出率的有___________ (填序号)。
A.适当增大NaOH溶液浓度 B.适当加快搅拌速率 C.适当降低温度
(5)碳分:向“碱溶”后的溶液中通入足量 气体,生成
气体,生成 沉淀和
沉淀和 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
 ,含少量
,含少量 、FeO、
、FeO、 等杂质)为主要原料制备氧化铝,流程如下。
等杂质)为主要原料制备氧化铝,流程如下。
 溶液浸取铝土矿中的铝元素和铁元素,
溶液浸取铝土矿中的铝元素和铁元素, 溶液的用量不宜过量太多,其原因是
溶液的用量不宜过量太多,其原因是(2)氧化:用
 溶液将
溶液将 氧化为
氧化为 ,反应的离子方程式为
,反应的离子方程式为(3)沉淀:用1mol/L
 溶液调节pH,将
溶液调节pH,将 、
、 转化为沉淀。溶液终点pH对铝、铁沉淀率的影响如图所示。
转化为沉淀。溶液终点pH对铝、铁沉淀率的影响如图所示。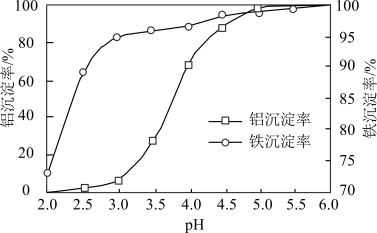
②实验室需要1mol/L
 溶液450mL,配制时需要使用的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和
溶液450mL,配制时需要使用的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和③检验
 沉淀完全的操作为:静置,
沉淀完全的操作为:静置,(4)碱溶:用NaOH溶液溶解沉淀,分离出
 。
。①该反应的离子方程式为:
②下列措施中能提高单位时间内铝元素浸出率的有
A.适当增大NaOH溶液浓度 B.适当加快搅拌速率 C.适当降低温度
(5)碳分:向“碱溶”后的溶液中通入足量
 气体,生成
气体,生成 沉淀和
沉淀和 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】某混合物甲中含有明矾[KA1(SO4)2·12H2O]、Al2O3和Fe2O3在一定条件下由甲可实现下图所示的物质之间的转化:
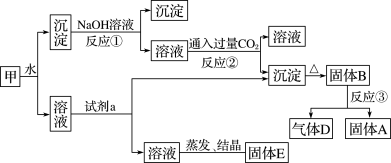
请回答下列问题:
(1)写出A、B、D的化学式:A________ 、B________ 、D___________ 。
(2)试剂a最好选用______ (填字母)
A. NaOH溶液 B.稀盐酸 C.二氧化碳 D.氨水
(3)写出反应①的离子方程式:_____________________________
(4)写出反应②中生成沉淀的化学方程式:___________________________ 。
(5)固体E可以作为复合性的化学肥料,E所含物质的化学式为_________________ 。

请回答下列问题:
(1)写出A、B、D的化学式:A
(2)试剂a最好选用
A. NaOH溶液 B.稀盐酸 C.二氧化碳 D.氨水
(3)写出反应①的离子方程式:
(4)写出反应②中生成沉淀的化学方程式:
(5)固体E可以作为复合性的化学肥料,E所含物质的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】氧化亚铜主要用于制造船底防污漆(用来杀死低级海生动物)、杀虫剂,以及各种铜盐、分析试剂、红色玻璃,还用于镀铜及镀铜合金溶液的配制。用某铜矿(主要含CuS、FeO)制备Cu2O的一种工艺流程如下图:
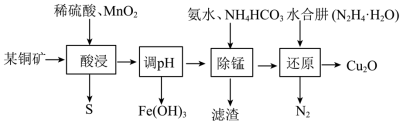
已知:常温下,相关金属离子生成氢氧化物沉淀的pH见表:
请回答下列问题:
(1)基态Cu原子价层电子的排布图为_______ 。
(2)滤渣的主要成分是_______ (填化学式)。
(3)“酸浸”中加入MnO2的作用是_______ ;写出其中生成单质S的化学方程式_______ 。
(4)“调pH”的范围是_______ 。
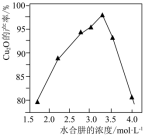
(5)“还原”前Cu元素以[Cu(NH3)4](OH)2的形式存在,水合肼被氧化的化学方程式为_______ ;一定体积下,保持其它条件不变,水合肼浓度对Cu2O的产率的影响如图所示。当水合肼浓度大于3.25mol·L-1时,[Cu(NH3)4]2+的转化率仍增大,但Cu2O的产率下降,其可能的原因是_______ 。

已知:常温下,相关金属离子生成氢氧化物沉淀的pH见表:
| 氢氧化物 | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀的pH | 4.8 | 1.9 | 7.5 | 8.8 |
| 沉淀完全的pH | 6.4 | 3.2 | 9.7 | 10.4 |
(1)基态Cu原子价层电子的排布图为
(2)滤渣的主要成分是
(3)“酸浸”中加入MnO2的作用是
(4)“调pH”的范围是
(5)“还原”前Cu元素以[Cu(NH3)4](OH)2的形式存在,水合肼被氧化的化学方程式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】钠及其化合物的生产、应用,是化工生产与研究的重要组成部分。
(1) 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。回答下列问题:
并检验其纯度的实验流程如图所示。回答下列问题:

①生成 的化学方程式是
的化学方程式是_______ 。
② 样品加水溶解的化学方程式为
样品加水溶解的化学方程式为_______ ,样液中加入 后产生
后产生 ,说明
,说明 与水反应的过程中生成了
与水反应的过程中生成了_______ (填化学式)。
③滤液中加入 溶液产生白色沉淀,说明
溶液产生白色沉淀,说明 样品中含有碳酸钠杂质,生成白色沉淀的离子方程式为
样品中含有碳酸钠杂质,生成白色沉淀的离子方程式为_______ 。
(2)工业上以侯氏制碱法为基础生产焦亚硫酸钠( ,能溶于水)的工艺流程如图:
,能溶于水)的工艺流程如图:
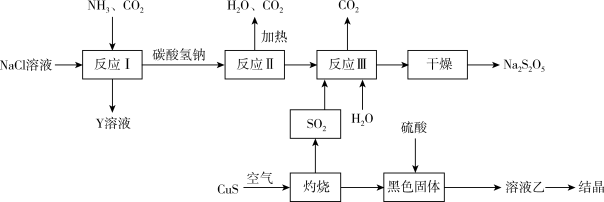
①反应Ⅱ的化学方程式为_______ 。
②关于该流程,下列说法正确的是_______ (填字母)
A.反应Ⅰ属于氧化还原反应 B.该流程中, 可以循环使用
可以循环使用
C.反应Ⅰ中应先通入 ,再通入
,再通入 D.溶液乙通过蒸发浓缩、冷却结晶可得硫酸铜晶体
D.溶液乙通过蒸发浓缩、冷却结晶可得硫酸铜晶体
(3) 在空气中灼烧的化学方程式为
在空气中灼烧的化学方程式为_______ 。
(1)
 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。回答下列问题:
并检验其纯度的实验流程如图所示。回答下列问题:
①生成
 的化学方程式是
的化学方程式是②
 样品加水溶解的化学方程式为
样品加水溶解的化学方程式为 后产生
后产生 ,说明
,说明 与水反应的过程中生成了
与水反应的过程中生成了③滤液中加入
 溶液产生白色沉淀,说明
溶液产生白色沉淀,说明 样品中含有碳酸钠杂质,生成白色沉淀的离子方程式为
样品中含有碳酸钠杂质,生成白色沉淀的离子方程式为(2)工业上以侯氏制碱法为基础生产焦亚硫酸钠(
 ,能溶于水)的工艺流程如图:
,能溶于水)的工艺流程如图:
①反应Ⅱ的化学方程式为
②关于该流程,下列说法正确的是
A.反应Ⅰ属于氧化还原反应 B.该流程中,
 可以循环使用
可以循环使用C.反应Ⅰ中应先通入
 ,再通入
,再通入 D.溶液乙通过蒸发浓缩、冷却结晶可得硫酸铜晶体
D.溶液乙通过蒸发浓缩、冷却结晶可得硫酸铜晶体(3)
 在空气中灼烧的化学方程式为
在空气中灼烧的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】氯化亚铜(CuCl)常用作有机合成工业中的催化剂,在空气中迅速被氧化成绿色;见光则分解,变成褐色。如图是工业上用制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程:
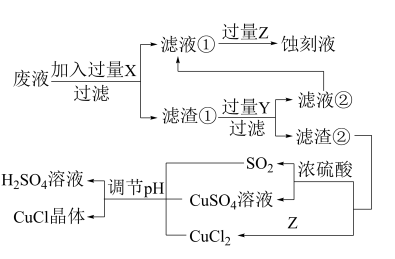
根据以上信息回答下列问题:
(1)生产过程中X的化学式为________ 。
(2)写出产生CuCl的化学方程式:_______________________________ 。
(3)在CuCl的生成过程中理论上不需要补充SO2气体,结合化学方程式和必要的文字说明理由_____________________________________________________ ;
实际生产中SO2要适当过量,原因可能是_______________________________ (答一点即可)。
(4)实验探究pH对CuCl产率的影响如下表所示:
析出CuCl晶体最佳pH为________ ,当pH较大时CuCl产率变低,原因是______________________ 。调节pH时,________ (填“能”或“不能”)用相同pH的硝酸代替硫酸,理由__________________ 。
(5)氯化亚铜的定量分析:
①称取样品0.25 g和过量的FeCl3溶液于锥形瓶中,充分溶解。
②用0.10 mol·L-1硫酸铈标准溶液滴定。已知:CuCl+FeCl3=CuCl2+FeCl2、Fe2++Ce4+=Fe3++Ce3+。三次平行实验结果如下(平行实验结果相差不能超过1%):
则样品中CuCl的纯度为________ (结果保留三位有效数字)。

根据以上信息回答下列问题:
(1)生产过程中X的化学式为
(2)写出产生CuCl的化学方程式:
(3)在CuCl的生成过程中理论上不需要补充SO2气体,结合化学方程式和必要的文字说明理由
实际生产中SO2要适当过量,原因可能是
(4)实验探究pH对CuCl产率的影响如下表所示:
| pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| CuCl产率/% | 70 | 90 | 82 | 78 | 75 | 72 | 70 |
析出CuCl晶体最佳pH为
(5)氯化亚铜的定量分析:
①称取样品0.25 g和过量的FeCl3溶液于锥形瓶中,充分溶解。
②用0.10 mol·L-1硫酸铈标准溶液滴定。已知:CuCl+FeCl3=CuCl2+FeCl2、Fe2++Ce4+=Fe3++Ce3+。三次平行实验结果如下(平行实验结果相差不能超过1%):
| 平行实验次数 | 1 | 2 | 3 |
| 0.25 g样品消耗硫酸铈 标准溶液的体积/mL | 24.35 | 24.05 | 23.95 |
则样品中CuCl的纯度为
您最近一年使用:0次



