如图所示,把试管放入盛有25℃饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5mL稀盐酸。
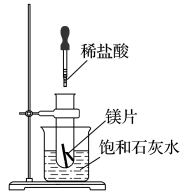
回答下列问题:
(1)实验中观察到的现象是________________ 。
(2)产生上述现象的原因是________________ 。
(3)写出有关反应的离子方程式____________ 。
(4)由实验推知,MgCl2溶液和H2的总能量________ (填“大于”、“小于”或“等于”)镁片和盐酸的总能量。

回答下列问题:
(1)实验中观察到的现象是
(2)产生上述现象的原因是
(3)写出有关反应的离子方程式
(4)由实验推知,MgCl2溶液和H2的总能量
2010·全国·一模 查看更多[41]
5.3.1 化学变化中的能量变化(第1课时)-【帮课堂】高一化学同步精品讲义(沪科版2020必修第二册)陕西省宜君县高级中学2021-2022学年高二上学期第一次月考化学(理)试题云南省易门一中2020-2021学年高一6月份月考化学试题福建省建瓯市芝华中学2020-2021学年高一下学期期中考试化学试题(已下线)6.1.1 化学反应与热能(练好题)(基础过关)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)(人教版2019)必修第二册 第六章 化学反应与能量 第一节 化学反应与能量变化(已下线)1.1.1 化学反应的反应热 内能变化 练习——【高中新教材同步备课】鲁科版高中化学选择性必修1云南省玉溪市峨山彝族自治县第一中学2019-2020学年高一下学期期中考试化学试题青海省海东市第二中学2019-2020学年高一下学期期中考试化学试题陕西省渭南市三贤中学2020年高一下学期期中考试化学试题吉林省延边市长白山第一高级中学2019-2020学年高一下学期验收考试化学试题2020年春高一化学新人教版第二册课后同步:6.1.1 化学反应与热能6.1.1 化学反应与热能——2020年春高一新人教版第二册化学一课一练2020年春季苏教版高中化学必修2专题二《化学反应与能量转化》测试卷2019——2020学年人教版必修2 第二章 化学反应与能量人教版高中化学必修二第二单元《化学反应与能量》测试卷(已下线)2019年3月12日 《每日一题》 必修2 放热反应与吸热反应的实验探究上海市2017-2018学年高一化学第一学期反应原理综合测试题云南省昆明市官渡区第一中学2018-2019学年高一下学期期中考试化学试题广西蒙山县第一中学2018-2019学年高一下学期第二次月考化学试题【校级联考】江苏省常州“教学研究合作联盟”2018-2019学年高二下学期期中考试化学试题人教版高二化学选修四专题:化学反应与能量变化同步练习题宁夏青铜峡市高级中学2017-2018学年高一下学期期中考试化学试题江西省南康中学2017-2018学年高一下学期第一次月考化学试题(已下线)2011-2012年吉林省长春外国语学校高二上学期第一次月考化学试卷(已下线)2010-2011学年湖南省醴陵二中、醴陵四中高一下学期期中联考化学试卷2015-2016学年广西南宁二十六中高一下学期期中考试化学试卷2015-2016学年宁夏育才中学高一下期中化学试卷2015-2016学年安徽省合肥中科大附中高二下期中理科化学试卷(已下线)2010年新疆哈巴河县高级中学高二上学期第一次月考化学试题2015-2016学年江西省玉山一中高一下第一次月考化学试卷22015-2016学年青海省西宁四中高二上学期期末化学试卷(已下线)高考第一轮复习化学反应与能量变化单元测试(已下线)2013-2014宁夏大学附属中学高一下学期期中考试化学试卷(已下线)2011-2012学年贵州省盘县二中高一下学期期中考试化学试卷(已下线)2012-2013学年山西省太原五中高二8月月考化学试卷(已下线)2012-2013学年安徽省舒城晓天中学高二上学期第一次月考化学试卷(已下线)2011-2012学年浙江临海市白云高级中学高二下学期期中考试化学卷(已下线)2011-2012学年浙江省杭州市西湖高级中学高一5月月考化学试卷(已下线)2011-2012年甘肃天水一中高一下学期第一学段考试文科化学试卷吉林省实验中学2016-2017学年高一下学期期中考试(文)化学试题
更新时间:2020-01-30 11:53:33
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】化学反应中不仅有物质变化而且伴随着能量变化,请回答下列问题。
(1)以下实验中属于吸热反应的是_______ (填序号)。
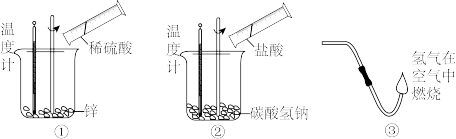
(2)利用铝与氧化铁在高温条件下,放出大量热可以焊接钢轨,发生反应的化学方程式为_______ ,图中,可表示铝与氧化铁的反应的是_______ (填字母)。
A. B.
B.
C. D.
D.
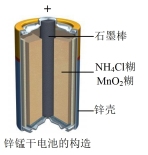
(3)锌锰干电池是应用最普遍的电池之一(如图所示),锌锰干电池属于_______ (填“一次电池”或“二次电池”),锌锰电池的正极材料是_______ ,负极发生的电极反应式为_______ 。若反应消耗19.5g负极材料,则电池中转移电子的数目为_______ 。
(1)以下实验中属于吸热反应的是

(2)利用铝与氧化铁在高温条件下,放出大量热可以焊接钢轨,发生反应的化学方程式为
A.
 B.
B.
C.
 D.
D.
(3)锌锰干电池是应用最普遍的电池之一(如图所示),锌锰干电池属于

您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】人们可以从不同的角度、不同的层面来认识物质的变化。请以2H2+O2 2H2O为例,谈谈你对化学变化的认识
2H2O为例,谈谈你对化学变化的认识____ 。
 2H2O为例,谈谈你对化学变化的认识
2H2O为例,谈谈你对化学变化的认识
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐3】反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示:
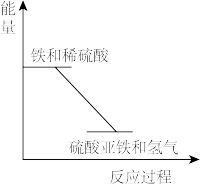
(1)该反应为_____ 反应(填“吸热”或“放热”).
(2)若要使该反应的反应速率加快,下列措施可行的是_____ (填字母).
a.改铁片为铁粉
b.改稀硫酸为98%的浓硫酸
c.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为_____ 极(填“正”或“负”).该极上发生的电极反应式为_____ ,外电路中电子由_____ 极(填“正”或“负”,下同)向_____ 极移动。

(1)该反应为
(2)若要使该反应的反应速率加快,下列措施可行的是
a.改铁片为铁粉
b.改稀硫酸为98%的浓硫酸
c.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)指出下列变化能量是怎样转化的:学校燃烧煤煮饭_________ ,给手机的电池充电_________ 。
(2)磷元素有多种性质不同的单质,红磷(结构复杂用“P”表示)和白磷(P4)是磷的两种同素异形体,充分燃烧之后的产物都是五氧化二磷。在25 ℃、101 kPa下,31 g白磷完全转化为红磷,放出11 kJ的热量,根据以上事实回答下列问题:
①红磷转化为白磷属于_________ 反应(填“放热”或“吸热”)。
②二者更稳定的是_________ 。(填“白磷”或“红磷”)。
(3)拆开1 mol H—H键、1 mol I—I、1 mol H—I键需要吸收的能量为436kJ、151k J、299k J。则氢气和碘生成1 mol HI需要_________ (填“放出”或“吸收”)_________ k J的热量。
(1)指出下列变化能量是怎样转化的:学校燃烧煤煮饭
(2)磷元素有多种性质不同的单质,红磷(结构复杂用“P”表示)和白磷(P4)是磷的两种同素异形体,充分燃烧之后的产物都是五氧化二磷。在25 ℃、101 kPa下,31 g白磷完全转化为红磷,放出11 kJ的热量,根据以上事实回答下列问题:
①红磷转化为白磷属于
②二者更稳定的是
(3)拆开1 mol H—H键、1 mol I—I、1 mol H—I键需要吸收的能量为436kJ、151k J、299k J。则氢气和碘生成1 mol HI需要
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】在寒冷的冬季,我们可以通过取暖器、电热炉,暖宝宝等来取暖。请查阅资料,设计一个通过化学反应产生热量的暖手袋的制作方案______ 。
您最近半年使用:0次
【推荐3】研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如下:

(1)反应I中,主要能量转化形式为_______ 能转化为_______ 能。
(2)S在元素周期表中的位于第_______ 周期第_______ 族。
(3)下列事实能说明硫的非金属性比碳强的是_______(填标号)。
(4)反应II中检验生成的二氧化硫的方法是_______ 。
(5)反应I:2H2SO4(1)=2SO2(g)+2H2O(g)+O2(g) △H1=+551 kJ·mol-1
反应III:S(s)+O2(g=SO2(g) △H3=-297 kJ·mol-1
反应II的热化学方程式:_______ 。
(6)通过反应III也可以不经过热能转化过程而直接获取电能,化学上将实现这一直接转化的装置称为_______ 。
(7)若将反应I、II和III相加,会得到什么结果?说明什么?谈谈你的体会。_________

(1)反应I中,主要能量转化形式为
(2)S在元素周期表中的位于第
(3)下列事实能说明硫的非金属性比碳强的是_______(填标号)。
| A.H2SO3的酸性比H2CO3的酸性强 | B.在硫与碳的化合物CS2中S显负价 |
| C.硫的单质的硬度比金刚石低 | D.S的导电性比石墨的弱 |
(5)反应I:2H2SO4(1)=2SO2(g)+2H2O(g)+O2(g) △H1=+551 kJ·mol-1
反应III:S(s)+O2(g=SO2(g) △H3=-297 kJ·mol-1
反应II的热化学方程式:
(6)通过反应III也可以不经过热能转化过程而直接获取电能,化学上将实现这一直接转化的装置称为
(7)若将反应I、II和III相加,会得到什么结果?说明什么?谈谈你的体会。
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】氢能源是一种有广阔发展前景的新型能源。回答下列问题:
(1)氢气是一种热值高、环境友好型燃料。等物质的量的氢气完全燃烧生成液态水与生成气态水相比,生成液态水时放出热量___________ (填“多”“少”或“相等”)。
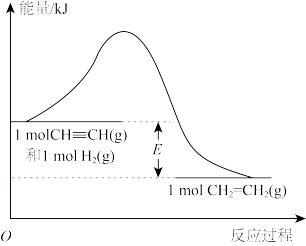
(2)乙炔( )与
)与 选择性反应制乙烯的反应原理为
选择性反应制乙烯的反应原理为 ,该反应过程中的能量变化如图所示。则该反应为
,该反应过程中的能量变化如图所示。则该反应为________ (填“放热”或“吸热”)反应;乙烯的电子式为_____________________ 。
(3)氢氧酸性燃料电池的工作原理示意图如图所示。
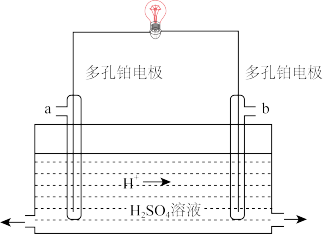
①a口应通入_________ (填“ ”或“
”或“ ”)。
”)。
②正极的电极反应式为_____________________ 。
③工作时,负极附近溶液的酸性___________ (填“增强”“减弱”或“不变”)。
④工作时,导线中流过 电子的电量时,理论上消耗标准状况下
电子的电量时,理论上消耗标准状况下 的体积为
的体积为__________ 。
(1)氢气是一种热值高、环境友好型燃料。等物质的量的氢气完全燃烧生成液态水与生成气态水相比,生成液态水时放出热量
(2)乙炔(
 )与
)与 选择性反应制乙烯的反应原理为
选择性反应制乙烯的反应原理为 ,该反应过程中的能量变化如图所示。则该反应为
,该反应过程中的能量变化如图所示。则该反应为
(3)氢氧酸性燃料电池的工作原理示意图如图所示。

①a口应通入
 ”或“
”或“ ”)。
”)。②正极的电极反应式为
③工作时,负极附近溶液的酸性
④工作时,导线中流过
 电子的电量时,理论上消耗标准状况下
电子的电量时,理论上消耗标准状况下 的体积为
的体积为
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1)已知:2mol氢气与足量氧气充分燃烧生成液态水时放出572kJ热量。
①反应2H2(g)+O2(g)=2H2O(g),生成物能量总和__ (填“大于”“小于”或“等于”)反应物能量总和。
②写出氢气燃烧生成液态水的热化学反应方程式:__ 。
③若H-H键、O=O键和H-O键的键能分别为E1、E2和E3,反应2H2(g)+O2(g)=2H2O(g) △H,则△H=___ (用含E1、E2、E3的式子表示),且△H1__ (填“大于”“小于”或“等于”)-572kJ/mol。
(2)FeS2焙烧产生的SO2可用于制硫酸。
已知25°C、101kPa时,2SO2(g)+O2(g) 2SO3(g) △H1=-197kJ/mol
2SO3(g) △H1=-197kJ/mol
H2O(g)=H2O(l) △H2=-44kJ/mol;
2SO2(g)+O2(g)+2H2O(g)==2H2SO4(1)△H3=-545kJ/mol;
则SO3(g)与H2O(l)反应生成H2SO4(l)的热化学方程式是__ 。
(1)已知:2mol氢气与足量氧气充分燃烧生成液态水时放出572kJ热量。
①反应2H2(g)+O2(g)=2H2O(g),生成物能量总和
②写出氢气燃烧生成液态水的热化学反应方程式:
③若H-H键、O=O键和H-O键的键能分别为E1、E2和E3,反应2H2(g)+O2(g)=2H2O(g) △H,则△H=
(2)FeS2焙烧产生的SO2可用于制硫酸。
已知25°C、101kPa时,2SO2(g)+O2(g)
 2SO3(g) △H1=-197kJ/mol
2SO3(g) △H1=-197kJ/molH2O(g)=H2O(l) △H2=-44kJ/mol;
2SO2(g)+O2(g)+2H2O(g)==2H2SO4(1)△H3=-545kJ/mol;
则SO3(g)与H2O(l)反应生成H2SO4(l)的热化学方程式是
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐3】一定温度下,在体积为0.5L的恒容密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色) N2O4(g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
N2O4(g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
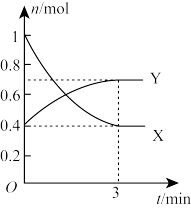
(1)曲线____ (填“X”或“Y”)表示N2O4的物质的量随时间的变化曲线。
(2)在0~3min内,用NO2表示的反应速率为____ 。
(3)若在一保温容器中加入一定量NO2,反应一段时间后,混合气体温度升高,说明2molNO2(g)的能量比1molN2O4(g)的能量____ (填“高”或“低”)。
(4)反应达到平衡后,若降低温度,混合气体的颜色变浅,相对于降温前v(正)____ (填“增大”“减小”或“不变”,下同),v(逆)____ 。
(5)氮氧化物是重要的大气污染物,如图是监测NO含量的传感器工作原理示意图。NiO电极发生___ (填“氧化”或“还原”)反应,Pt电极上的电极反应式为____ 。

 N2O4(g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
N2O4(g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
(1)曲线
(2)在0~3min内,用NO2表示的反应速率为
(3)若在一保温容器中加入一定量NO2,反应一段时间后,混合气体温度升高,说明2molNO2(g)的能量比1molN2O4(g)的能量
(4)反应达到平衡后,若降低温度,混合气体的颜色变浅,相对于降温前v(正)
(5)氮氧化物是重要的大气污染物,如图是监测NO含量的传感器工作原理示意图。NiO电极发生

您最近半年使用:0次



