反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示:
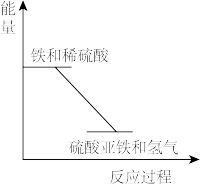
(1)该反应为_____ 反应(填“吸热”或“放热”).
(2)若要使该反应的反应速率加快,下列措施可行的是_____ (填字母).
a.改铁片为铁粉
b.改稀硫酸为98%的浓硫酸
c.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为_____ 极(填“正”或“负”).该极上发生的电极反应式为_____ ,外电路中电子由_____ 极(填“正”或“负”,下同)向_____ 极移动。

(1)该反应为
(2)若要使该反应的反应速率加快,下列措施可行的是
a.改铁片为铁粉
b.改稀硫酸为98%的浓硫酸
c.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为
更新时间:2020-09-14 21:44:38
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】2SO2+O2 2SO3△H=-akJmol-1,反应过程的能量变化如图所示。已知1molSO2完全转化为1molSO3放热99kJ。请回答:
2SO3△H=-akJmol-1,反应过程的能量变化如图所示。已知1molSO2完全转化为1molSO3放热99kJ。请回答:
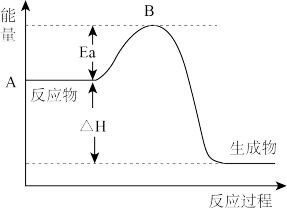
(1)a=___ 。升高温度,该反应中SO2的转化率变___ (填“大”或“小”)。
(2)Ea的大小对该反应的△H___ (填“有”或“无”)影响。该反应常用V2O5作催化剂,加入V2O5会使图中B点__ (填“升高”、“降低”或“不变”)。
(3)已知在一定条件下SO3(g)也可分解生成SO2(g)和O2(g),试写出该反应的热化学方程式:___ 。
 2SO3△H=-akJmol-1,反应过程的能量变化如图所示。已知1molSO2完全转化为1molSO3放热99kJ。请回答:
2SO3△H=-akJmol-1,反应过程的能量变化如图所示。已知1molSO2完全转化为1molSO3放热99kJ。请回答:
(1)a=
(2)Ea的大小对该反应的△H
(3)已知在一定条件下SO3(g)也可分解生成SO2(g)和O2(g),试写出该反应的热化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】铝热反应有广泛的用途,实验装置如图所示。
(1)铝热反应是________ (填“吸热”或“放热”)反应,其能量变化可用下图中的_______ (填序号)表示。
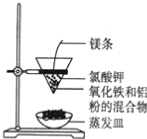
(2)该铝热反应的化学方程式是______________________________________________ 。
(3)任写出铝热反应在实际生产中的一种用途__________________________________ 。
(1)铝热反应是
反应物的总能量高 | 生成物的总能量高 |
|
|
生成物的总能量低 | 反应物的总能量低 |

(2)该铝热反应的化学方程式是
(3)任写出铝热反应在实际生产中的一种用途
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】反应热 焓变
(1)反应热:在等温条件下,化学反应体系向环境_______ 或从环境_______ 的热量,称为化学反应的热效应,简称反应热.
(2)内能:是体系内物质的各种_______ 的总和,受温度,压强和物质聚集状态等影响.
(3)焓变:在等压条件下进行的化学反应,反应热_______ 反应的焓变.用符号 表示,单位:
表示,单位:_______ .放热反应的
_______ 0,吸热反应的
_______ 0.
(4)化学反应中能量变化的主要原因:_______ .
(1)反应热:在等温条件下,化学反应体系向环境
(2)内能:是体系内物质的各种
(3)焓变:在等压条件下进行的化学反应,反应热
 表示,单位:
表示,单位:

(4)化学反应中能量变化的主要原因:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】甲同学用等质量的锌粉先后与1mol·L-1盐酸及相同体积、未知浓度的盐酸反应,记录相关数据,并作出这两个反应过程中放出气体的体积随反应时间的变化曲线图(如图所示)。

(1)如果请你做这个实验,你测量该反应所放气体的体积的方法是___ 。
(2)根据图示可判断,该同学所用的盐酸的浓度比1 mol/L___ (填“大”或“小”)。理由是___ 。
(3)乙同学为控制反应速率,防止因反应过快而难以测量氢气体积,想事先在盐酸中加入等体积的下列溶液以减慢反应速率。你认为在以下试剂中,不可行的是___ 。
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(4)丙同学用1mol·L-1硫酸代替上述实验中的1mol·L-1盐酸,请问二者的反应速率是否相同___ 。理由是___ 。

(1)如果请你做这个实验,你测量该反应所放气体的体积的方法是
(2)根据图示可判断,该同学所用的盐酸的浓度比1 mol/L
(3)乙同学为控制反应速率,防止因反应过快而难以测量氢气体积,想事先在盐酸中加入等体积的下列溶液以减慢反应速率。你认为在以下试剂中,不可行的是
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(4)丙同学用1mol·L-1硫酸代替上述实验中的1mol·L-1盐酸,请问二者的反应速率是否相同
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】一定条件下,在 密闭容器中发生反应:
密闭容器中发生反应: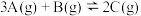 。开始时加入
。开始时加入 、
、 、
、 ,在
,在 末测得
末测得 的物质的量是
的物质的量是 。
。
(1)用 的浓度变化表示反应的平均速率:
的浓度变化表示反应的平均速率:
_______ 。
(2)在 末,
末, 的浓度为
的浓度为_______ 。
(3)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”):
①升高温度,化学反应速率_______ ;
②充入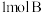 ,化学反应速率
,化学反应速率_______ ;
③将容器的体积变为 ,化学反应速率
,化学反应速率_______ 。
 密闭容器中发生反应:
密闭容器中发生反应: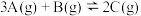 。开始时加入
。开始时加入 、
、 、
、 ,在
,在 末测得
末测得 的物质的量是
的物质的量是 。
。(1)用
 的浓度变化表示反应的平均速率:
的浓度变化表示反应的平均速率:
(2)在
 末,
末, 的浓度为
的浓度为(3)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”):
①升高温度,化学反应速率
②充入
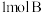 ,化学反应速率
,化学反应速率③将容器的体积变为
 ,化学反应速率
,化学反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】一定条件下CO2会和H2反应合成CH3OH。方程式为:CO2(g)+3H2(g)  CH3OH(g)+H2O(g) 。现向2L恒容密闭容器中加入2 mol CO2、6 mol H2,在恒温下发生反应。10s后反应达到平衡,此时容器内CH3OH的浓度为0.5mol·L-1,请回答以下问题:
CH3OH(g)+H2O(g) 。现向2L恒容密闭容器中加入2 mol CO2、6 mol H2,在恒温下发生反应。10s后反应达到平衡,此时容器内CH3OH的浓度为0.5mol·L-1,请回答以下问题:
(1)前10s内的平均反应速率v(H2O)=___________ ;平衡时c(H2)=___________ 。
(2)其它条件不变的情况下,在10s时往容器中再加入一定量H2,此时该反应正向速率将___________ (填“增大”或“减小”或“不变”)。
(3)下列叙述能说明原反应达到平衡状态的是___________ 。
a.单位时间内消耗n mol CH3OH的同时生成n mol CO2
b.1mol CO2生成的同时有3mol H-H键断裂
c.CO2和H2的浓度保持不变
d.容器内压强保持不变
e.CO2和H2的物质的量之比保持不变
(4)甲醇(CH3OH)性质类似乙醇,请写出甲醇与乙酸形成乙酸甲酯的反应方程式:___________
 CH3OH(g)+H2O(g) 。现向2L恒容密闭容器中加入2 mol CO2、6 mol H2,在恒温下发生反应。10s后反应达到平衡,此时容器内CH3OH的浓度为0.5mol·L-1,请回答以下问题:
CH3OH(g)+H2O(g) 。现向2L恒容密闭容器中加入2 mol CO2、6 mol H2,在恒温下发生反应。10s后反应达到平衡,此时容器内CH3OH的浓度为0.5mol·L-1,请回答以下问题:(1)前10s内的平均反应速率v(H2O)=
(2)其它条件不变的情况下,在10s时往容器中再加入一定量H2,此时该反应正向速率将
(3)下列叙述能说明原反应达到平衡状态的是
a.单位时间内消耗n mol CH3OH的同时生成n mol CO2
b.1mol CO2生成的同时有3mol H-H键断裂
c.CO2和H2的浓度保持不变
d.容器内压强保持不变
e.CO2和H2的物质的量之比保持不变
(4)甲醇(CH3OH)性质类似乙醇,请写出甲醇与乙酸形成乙酸甲酯的反应方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】氢气与氮气反应生成氨气是可逆反应,研究发现降低温度有利于平衡向生成氨气的方向移动,但是实际生产中,这个反应是在较高温度下进行的,主要原因是____
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】简要回答下列问题。
(1)NO暴露在空气中,出现红棕色的原因是________ 。
(2)将食品置于低温条件下,常常可以保存更长时间的原因是________ 。
(3)盛有浓硫酸的容器敞口放置一段时间后,硫酸浓度变小的原因是________ 。
(4)推广使用新能源汽车的目的是________ 。
(1)NO暴露在空气中,出现红棕色的原因是
(2)将食品置于低温条件下,常常可以保存更长时间的原因是
(3)盛有浓硫酸的容器敞口放置一段时间后,硫酸浓度变小的原因是
(4)推广使用新能源汽车的目的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】将物质的量均为3mol的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(s) xC(g)+2D(g),经5min后反应达到平衡,此时测得C的浓度为0.5mol·L-1,D的平均反应速率是0.1mol/(L·min),按要求填空:
xC(g)+2D(g),经5min后反应达到平衡,此时测得C的浓度为0.5mol·L-1,D的平均反应速率是0.1mol/(L·min),按要求填空:
(1)A的平均反应速率为___________
(2)x的值为___________
(3)平衡后A的物质的量浓度为___________
(4)下列措施能明显加快反应速率的是___________
A.升高温度 B.将产物及时分离
C.向密闭容器中充入一定的惰性气体 D.将密闭容器的体积变为1L
 xC(g)+2D(g),经5min后反应达到平衡,此时测得C的浓度为0.5mol·L-1,D的平均反应速率是0.1mol/(L·min),按要求填空:
xC(g)+2D(g),经5min后反应达到平衡,此时测得C的浓度为0.5mol·L-1,D的平均反应速率是0.1mol/(L·min),按要求填空:(1)A的平均反应速率为
(2)x的值为
(3)平衡后A的物质的量浓度为
(4)下列措施能明显加快反应速率的是
A.升高温度 B.将产物及时分离
C.向密闭容器中充入一定的惰性气体 D.将密闭容器的体积变为1L
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)含硫的物质与人们的生活密切相关。已知硫元素常见的化合价有-1、0、+4、+6四种,其不同价态的物质间可相互转化。完成下列填空:
①硫离子的结构示意图为:_______ ,二氧化硫中S 的化合价为_______ 。
②二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是硫酸。
以下是二氧化硫形成酸雨的两种途径:

请写出(1)的化学方程式:_______ 。
③你认为减少酸雨产生的途径可采用的措施是_______ (填字母序号)
A.少用煤作燃料 B.把工厂烟囱造高 C.燃料脱硫 D.在已酸化的土壤中加石灰 E.开发新能源
④硫酸盐的种类很多,且应用广泛,医疗上常用_______ (写化学式)作X射线透视肠胃的内服药剂,生活用水可以用_______ (写化学式)作净水剂。
⑤写出在加热条件下,木炭与浓硫酸反应的化学方程式:_______ 。
⑥检验SO2中是否混有CO2气体,可采用的方法是_______ (填字母序号)
A. 通过品红溶液 B. 先通过NaOH溶液,再通过澄清石灰水
C. 通过澄清石灰水 D. 先通过KMnO4酸性溶液,再通过澄清石灰水
(2)化学电池已成为人类生产生活的重要能量来源之一,化学电池是根据原电池原理制成的。依据如下装置图,回答下列问题:

①若X为Zn,Y为硫酸铜溶液,溶液中的Cu2+移向_______ (填“Cu”或“X”)电极,当电路中转移0.2mole-时,电解质溶液质量增加_______ g。
②若用如图装置,依据反应Fe+2Fe3+=3Fe2+设计原电池,则电极X应为_______ (填化学式),电解质溶液Y的溶质为_______ (填化学式),铜极的电极反应式为_______ 。
(1)含硫的物质与人们的生活密切相关。已知硫元素常见的化合价有-1、0、+4、+6四种,其不同价态的物质间可相互转化。完成下列填空:
①硫离子的结构示意图为:
②二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是硫酸。
以下是二氧化硫形成酸雨的两种途径:

请写出(1)的化学方程式:
③你认为减少酸雨产生的途径可采用的措施是
A.少用煤作燃料 B.把工厂烟囱造高 C.燃料脱硫 D.在已酸化的土壤中加石灰 E.开发新能源
④硫酸盐的种类很多,且应用广泛,医疗上常用
⑤写出在加热条件下,木炭与浓硫酸反应的化学方程式:
⑥检验SO2中是否混有CO2气体,可采用的方法是
A. 通过品红溶液 B. 先通过NaOH溶液,再通过澄清石灰水
C. 通过澄清石灰水 D. 先通过KMnO4酸性溶液,再通过澄清石灰水
(2)化学电池已成为人类生产生活的重要能量来源之一,化学电池是根据原电池原理制成的。依据如下装置图,回答下列问题:

①若X为Zn,Y为硫酸铜溶液,溶液中的Cu2+移向
②若用如图装置,依据反应Fe+2Fe3+=3Fe2+设计原电池,则电极X应为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在由铜锌组成的原电池(电解质是稀硫酸)中,有位同学在铜电极收集到了12 g的气体:
(1)铜锌原电池的正、负极的电极反应:正极:___________ 负极:___________
(2)铜电极产生12 g气体的过程中有___________ g的锌溶解。
(3)铜电极产生12 g气体的过程中有___________ mol的电子发生了转移。
(1)铜锌原电池的正、负极的电极反应:正极:
(2)铜电极产生12 g气体的过程中有
(3)铜电极产生12 g气体的过程中有
您最近一年使用:0次





