(1)通常用小苏打的饱和溶液除去CO2中的HCl,反应的化学方程式为_____ ,不能用苏打溶液的原因是____ (用化学方程式表示)。
(2)在NaBr与NaI的混合液中通入过量的Cl2。把溶液蒸干后灼烧最后残留的物质是____ 。
(2)在NaBr与NaI的混合液中通入过量的Cl2。把溶液蒸干后灼烧最后残留的物质是
更新时间:2020-02-01 17:50:05
|
相似题推荐
【推荐1】FeBr2溶液中通入过量Cl2:_______
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】卤族元素包括氯、溴、碘等元素,其中溴和碘在陆地上含量极少,主要存在于海水中。
(1)氯气有毒,一旦泄漏会造成对空气的严重污染。工业上常用浓氨水检验氯气管是否漏气。(已知Cl2可将NH3氧化成N2)写出有关的化学方程式_________ 。
(2)亚氯酸钠(NaClO2)是一种漂白剂。已知NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量_____ (填相同或不相同),解释其原因是_____ 。
(3)从海水中提取溴,一般要经过浓缩、氧化和提取三个步骤。氧化时常用氯气做氧化剂,写出有关的离子方程式__________ 。
(4)海带提碘时,由于碘的量较少,在灼烧、溶解之后得到的溶液用硝酸银溶液很难检验。设计一个检验浓液中是否含有碘离子的方法_____ 。
(1)氯气有毒,一旦泄漏会造成对空气的严重污染。工业上常用浓氨水检验氯气管是否漏气。(已知Cl2可将NH3氧化成N2)写出有关的化学方程式
(2)亚氯酸钠(NaClO2)是一种漂白剂。已知NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量
(3)从海水中提取溴,一般要经过浓缩、氧化和提取三个步骤。氧化时常用氯气做氧化剂,写出有关的离子方程式
(4)海带提碘时,由于碘的量较少,在灼烧、溶解之后得到的溶液用硝酸银溶液很难检验。设计一个检验浓液中是否含有碘离子的方法
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】I. 是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用,请回答下列问题。
是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用,请回答下列问题。
(1) 属于
属于_____________ (填:氧化物,碱,盐)。
(2)浸泡衣物时加入“84”消毒液在空气中放置一段时间漂白效果更好,原因用离子方程式表示为:______________ 。(已知酸性: -)
-)
(3)若将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,则会产生黄绿色的有毒气体,其反应的离子方程式是_______ 。
II.Cl2是一种有毒气体,如果泄漏会造成严重的危害。
(4)已知: ,化工厂可用浓氨水来检验Cl2是否泄漏。该反应中被氧化和未被氧化的
,化工厂可用浓氨水来检验Cl2是否泄漏。该反应中被氧化和未被氧化的 的物质的量比
的物质的量比_______ 。
(5)喷射石灰乳等碱性物质可以减轻少量Cl2泄漏造成的危害。Cl2和石灰乳反应的化学方程式是:_____ 。
 是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用,请回答下列问题。
是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用,请回答下列问题。(1)
 属于
属于(2)浸泡衣物时加入“84”消毒液在空气中放置一段时间漂白效果更好,原因用离子方程式表示为:
 -)
-)(3)若将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,则会产生黄绿色的有毒气体,其反应的离子方程式是
II.Cl2是一种有毒气体,如果泄漏会造成严重的危害。
(4)已知:
 ,化工厂可用浓氨水来检验Cl2是否泄漏。该反应中被氧化和未被氧化的
,化工厂可用浓氨水来检验Cl2是否泄漏。该反应中被氧化和未被氧化的 的物质的量比
的物质的量比(5)喷射石灰乳等碱性物质可以减轻少量Cl2泄漏造成的危害。Cl2和石灰乳反应的化学方程式是:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】历史上海藻提碘中得到一种红棕色液体,由于性质相似,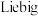 误认为是
误认为是 ,从而错过了一种新元素的发现。该元素是
,从而错过了一种新元素的发现。该元素是_______ 。
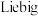 误认为是
误认为是 ,从而错过了一种新元素的发现。该元素是
,从而错过了一种新元素的发现。该元素是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)向橙色的溴水中加入足量的镁粉,充分振荡后过滤,溶液呈现______ 色,原因用化学方程式表示为_____________________________________ 。
(2)若向(1)中滤液加入适量的氯水后,溶液呈______ 色,原因用离子方程式表示为________ 。
(3)若向(1)中滤液加入适量的硝酸银溶液,溶液中有______ 生成,原因用离子方程式表示_____ 。
(2)若向(1)中滤液加入适量的氯水后,溶液呈
(3)若向(1)中滤液加入适量的硝酸银溶液,溶液中有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】按要求回答下列问题:
(1)已知氧化性:Cl2>Br2>Fe3+。向200mLcmol·L-1FeBr2溶液中逐渐通入Cl2,其中n(Fe2+)、n(Br-)随通入Cl2的物质的量[n(Cl2)]变化如图所示:

①曲线①为___________ ,c=___________ ;
②n(Cl2)=0.35 mol时,溶液中c(Fe3+)___________ c(Br-) (填“>”、“<”或“=”);
③n(Cl2)=0.45 mol时,总的离子方程式为___________ 。
(2)实验测得Fe2(SO4)3、CuSO4的混合溶液中,n(Fe3+): n(Cu2+)=1:2,n(Fe3+)=0.1mol/L。则c(SO )为
)为___________ mol/L。
(3)70%的硫酸与等体积的水混合后,所得溶液的质量分数___________ 35%。
(1)已知氧化性:Cl2>Br2>Fe3+。向200mLcmol·L-1FeBr2溶液中逐渐通入Cl2,其中n(Fe2+)、n(Br-)随通入Cl2的物质的量[n(Cl2)]变化如图所示:

①曲线①为
②n(Cl2)=0.35 mol时,溶液中c(Fe3+)
③n(Cl2)=0.45 mol时,总的离子方程式为
(2)实验测得Fe2(SO4)3、CuSO4的混合溶液中,n(Fe3+): n(Cu2+)=1:2,n(Fe3+)=0.1mol/L。则c(SO
 )为
)为(3)70%的硫酸与等体积的水混合后,所得溶液的质量分数
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】A、B、C三种物质均含有同一种元素,它们之间存在如图所示的转化关系:
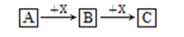
(1)若A、B、C均属于盐类且为厨房中的常见物质,则B为_________ ,列举其在生活中的一种用途________ 。
(2)若A、C均属于盐类,且A常用作净水剂,B为白色胶状不溶物,A与过量氨水反应的离子方程式为_____________________________________ 。
(3)若A为一种无色气体单质,X为一种黑色固体单质,则C为_________ ,B与Na2O2反应方程式____________________________ 。
(4)若A为一种金属单质,X为一种无色气体单质,C为淡黄色粉末,将A投入CuSO4溶液中的离子方程式_____________ 。
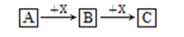
(1)若A、B、C均属于盐类且为厨房中的常见物质,则B为
(2)若A、C均属于盐类,且A常用作净水剂,B为白色胶状不溶物,A与过量氨水反应的离子方程式为
(3)若A为一种无色气体单质,X为一种黑色固体单质,则C为
(4)若A为一种金属单质,X为一种无色气体单质,C为淡黄色粉末,将A投入CuSO4溶液中的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1) ①写出小苏打的化学式:___________ ;
②写出光导纤维主要成分的化学式___________ 。
(2)高温下铁与水蒸气反应的化学方程式___________ 。
(3)下面是同学们熟悉的物质:
①O2 ②NaOH ③酒精 ④HClO ⑤Na2O2 ⑥NH4Cl ⑦CO2 ⑧Ne
这些物质中,属于非电解质的是___________ (填序号,下同),含有离子键的是___________ ,不含化学键的有___________ 写出 NaOH 的电子式___________ ,写出 HClO 的结构式___________
②写出光导纤维主要成分的化学式
(2)高温下铁与水蒸气反应的化学方程式
(3)下面是同学们熟悉的物质:
①O2 ②NaOH ③酒精 ④HClO ⑤Na2O2 ⑥NH4Cl ⑦CO2 ⑧Ne
这些物质中,属于非电解质的是
您最近一年使用:0次



