镁的化合物在化工生产和药物合成上有重要用途。某兴趣小组以一种工业废渣(主要成分为MgCO3、MgSiO3和少量Fe的氧化物)为原料制备MgCO3·3H2O。实验过程如下:
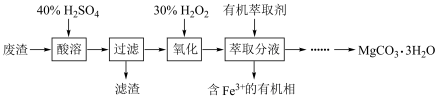
(1)滤渣的成分为_________________ (填化学式),过滤装置在使用一段时间后需用NaOH溶液清洗,用化学方程式表示其清洗原理:______________ 。
(2)加入H2O2一段时间后,溶液中有气泡出现并放热,分析产生气泡的原因:____________ (用文字表达)。
(3)萃取分液中要用到分液漏斗,分液漏斗在使用前须洗干净并____________________ 。萃取分液的目的是______________ (填字母)。
A.除去水溶液中的铁离子
B.增加镁离子在水中的溶解度
C.富集铁元素,可以回收利用
(4)萃取后得到的水溶液制备MgCO3·3H2O的实验操作:边搅拌边向溶液中滴加Na2CO3溶液至有大量沉淀生成,静置后,进行操作:______________________________ ,确定沉淀完全后,再过滤、__________________ 、__________________ ,得到MgCO3·3H2O。

(1)滤渣的成分为
(2)加入H2O2一段时间后,溶液中有气泡出现并放热,分析产生气泡的原因:
(3)萃取分液中要用到分液漏斗,分液漏斗在使用前须洗干净并
A.除去水溶液中的铁离子
B.增加镁离子在水中的溶解度
C.富集铁元素,可以回收利用
(4)萃取后得到的水溶液制备MgCO3·3H2O的实验操作:边搅拌边向溶液中滴加Na2CO3溶液至有大量沉淀生成,静置后,进行操作:
更新时间:2020-02-11 16:03:06
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】二苯甲烷( 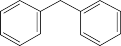 )有定香能力,可作香叶油的代用品,用于配制香水。在一定温度下,二苯甲烷可通过苯和氯化苄(
)有定香能力,可作香叶油的代用品,用于配制香水。在一定温度下,二苯甲烷可通过苯和氯化苄(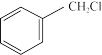 )在AlCl3催化下合成。已知:
)在AlCl3催化下合成。已知:
按以下步骤制备二苯甲烷,回答相关问题:
(1)如图所示,向三颈烧瓶中加入50 mL苯、40 mL氯化苄和适量AlCl3,开启搅拌器,控制温度为80 ℃左右,反应4小时。
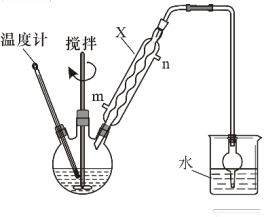
①仪器X的名称为_______ ,所起的主要作用是_______ ,其进水口是_______ (填“m”或“n”)。
②该合成反应的化学方程式为_______ 。
③反应时所用苯过量的目的是_______ 。
(2)反应结束后,停止加热,冷却三颈烧瓶至室温,依次用水、稀碱液、水对粗产品进行洗涤、分液,再进行干燥,最后采用操作a分离出二苯甲烷。
①第一次水洗的目的是_______ ,操作a的名称是_______ 。
②若分离所得的二苯甲烷为50.4 g,则其产率为_______ 。
 )有定香能力,可作香叶油的代用品,用于配制香水。在一定温度下,二苯甲烷可通过苯和氯化苄(
)有定香能力,可作香叶油的代用品,用于配制香水。在一定温度下,二苯甲烷可通过苯和氯化苄( )在AlCl3催化下合成。已知:
)在AlCl3催化下合成。已知:| 名称 | 相对分子质量 | 密度(g/cm3) | 溶解性 | 沸点/℃ |
| 苯 | 78 | 0.87 | 不溶于水,易溶于有机溶剂 | 80.1 |
| 氯化苄 | 126.5 | 1.10 | 不溶于水,可溶于苯 | 179 |
| 二苯甲烷 | 168 | 1.34 | 不溶于水,可溶于苯 | 265 |
(1)如图所示,向三颈烧瓶中加入50 mL苯、40 mL氯化苄和适量AlCl3,开启搅拌器,控制温度为80 ℃左右,反应4小时。

①仪器X的名称为
②该合成反应的化学方程式为
③反应时所用苯过量的目的是
(2)反应结束后,停止加热,冷却三颈烧瓶至室温,依次用水、稀碱液、水对粗产品进行洗涤、分液,再进行干燥,最后采用操作a分离出二苯甲烷。
①第一次水洗的目的是
②若分离所得的二苯甲烷为50.4 g,则其产率为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某兴趣小组设计如图实验装置制备次磷酸钠( )。
)。
已知:①白磷( )在空气中可自燃,与过量烧碱溶液混合,80~90℃时反应生成
)在空气中可自燃,与过量烧碱溶液混合,80~90℃时反应生成 和
和 。
。
② 是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成
是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成 。
。
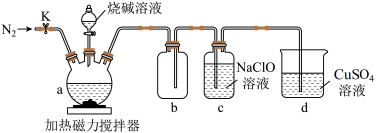
(1)仪器a的名称是___________ 。a中发生反应的化学方程式是___________ 。
(2)仪器b组成的装置的作用是___________ ,检查装置气密性后,应先打开K通入 一段时间,目的是
一段时间,目的是___________ 。
(3)下列有关说法正确的是___________。
(4)①仪器c中充分反应后生成 和NaCl,经过一系列操作可获得固体
和NaCl,经过一系列操作可获得固体 。相关物质的溶解度(S)如下:
。相关物质的溶解度(S)如下:
从下列选项a-g中选择合理的仪器或操作,补全如下步骤。
取仪器c中溶液,用蒸发皿___________ →用___________ (趁热过滤)→用烧杯(冷却结晶)→用漏斗(过滤得到 )→
)→___________ →干燥 粗品。
粗品。
选项:a.溶解 b.过滤 c.洗涤 d.普通三角漏斗 e.保温漏斗
f.蒸发浓缩至有大量晶体析出 g.蒸发浓缩至溶液表面出现晶膜
②写出c中发生反应的离子方程式___________ 。
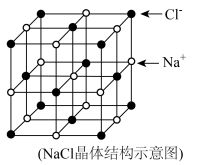
(5)NaCl晶胞结构如图,设距离最近的 间的距离为apm,
间的距离为apm, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为___________  。(列出计算式即可)
。(列出计算式即可)
 )。
)。已知:①白磷(
 )在空气中可自燃,与过量烧碱溶液混合,80~90℃时反应生成
)在空气中可自燃,与过量烧碱溶液混合,80~90℃时反应生成 和
和 。
。②
 是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成
是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成 。
。
(1)仪器a的名称是
(2)仪器b组成的装置的作用是
 一段时间,目的是
一段时间,目的是(3)下列有关说法正确的是___________。
A.次磷酸( )是三元酸 )是三元酸 |
| B.为加快反应速率,投料前应先在通风橱内将白磷碾成薄片状 |
C.反应结束后应继续通入 一段时间,可提高 一段时间,可提高 产率 产率 |
| D.d中所盛硫酸铜溶液可用酸性高锰酸钾溶液代替 |
(4)①仪器c中充分反应后生成
 和NaCl,经过一系列操作可获得固体
和NaCl,经过一系列操作可获得固体 。相关物质的溶解度(S)如下:
。相关物质的溶解度(S)如下: | S(25℃) | S(100℃) | |
| NaCl | 37 | 39 |
 | 100 | 667 |
取仪器c中溶液,用蒸发皿
 )→
)→ 粗品。
粗品。选项:a.溶解 b.过滤 c.洗涤 d.普通三角漏斗 e.保温漏斗
f.蒸发浓缩至有大量晶体析出 g.蒸发浓缩至溶液表面出现晶膜
②写出c中发生反应的离子方程式
(5)NaCl晶胞结构如图,设距离最近的
 间的距离为apm,
间的距离为apm, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为 。(列出计算式即可)
。(列出计算式即可)
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】试回答下列中学化学实验室中常见仪器的有关问题:
(1)在仪器①分液漏斗、②试剂瓶、③集气瓶、④滴瓶、⑤滴定管、⑥容量瓶、⑦量筒、⑧托盘天平中,标有“0”刻度的是(填序号,下同)___________ ;标有使用温度的仪器是___________ 。
(2)“磨砂”是增加玻璃仪器密封性的一种处理工艺。在仪器①试管、②分液漏斗、③细口试剂瓶、④广口试剂瓶、⑤集气瓶、⑥滴瓶、⑦酸式滴定管、⑧碱式滴定管中,用到“磨砂”的有___________ 。
(3)在仪器①漏斗、②容量瓶、③蒸馏烧瓶、④分液漏斗、⑤烧杯、⑥蒸发皿中,可用于粗盐提纯实验的有_______ ;可用于分离两种沸点接近且互不相溶的液态混合物实验的有_______ 。
(1)在仪器①分液漏斗、②试剂瓶、③集气瓶、④滴瓶、⑤滴定管、⑥容量瓶、⑦量筒、⑧托盘天平中,标有“0”刻度的是(填序号,下同)
(2)“磨砂”是增加玻璃仪器密封性的一种处理工艺。在仪器①试管、②分液漏斗、③细口试剂瓶、④广口试剂瓶、⑤集气瓶、⑥滴瓶、⑦酸式滴定管、⑧碱式滴定管中,用到“磨砂”的有
(3)在仪器①漏斗、②容量瓶、③蒸馏烧瓶、④分液漏斗、⑤烧杯、⑥蒸发皿中,可用于粗盐提纯实验的有
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】从铜电解液(主要含 、Ni2+、
、Ni2+、 、
、 、
、 、Zn2+等)中提纯得到粗硫酸镍晶体,为了进一步纯化并回收胆矾晶体,某课题小组设计了如图流程:
、Zn2+等)中提纯得到粗硫酸镍晶体,为了进一步纯化并回收胆矾晶体,某课题小组设计了如图流程:

已知:相关离子浓度为0.1mol/L时,形成氢氧化物沉淀的pH范围如下:
(1)为加快“水浸”时的浸出率,可采取的措施有_______ (任写一点)。
(2)为了使“溶液1”中的反应充分进行,需要通入稍过量的H2S,写出Fe3+与H2S发生反应的离子方程式:_______ 。
(3)请结合离子方程式解释向“溶液2”中加入Ni(OH)2的原因_______ 。
(4)“操作X”为在_______ (填仪器名称)中加热至_______ ,冷却结晶、过滤、洗涤、干燥后得到结晶水合物晶体。
(5)若“溶液3”中Ca2+的浓度为0.001mol/L,取等体积的NiF2溶液与该溶液混合,要使反应结束时c(Ca2+)<10-5mol/L,则所加NiF2溶液的浓度至少为_______ mol/L。[已知室温下Ksp(CaF2)=4×10-11]
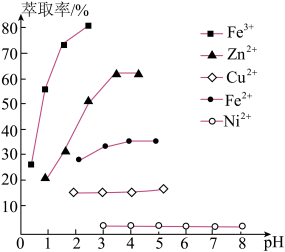
(6)室温下选择萃取剂P204(二乙基已基磷酸,用HR表示),其萃取原理为nHR+Mn+⇌MRn+nH+,试剂a为_______ (填化学式)。溶液pH对几种离子的萃取率的影响如图,则萃取锌时,应控制pH的范围为3~4,请解释原因:_______ 。
 、Ni2+、
、Ni2+、 、
、 、
、 、Zn2+等)中提纯得到粗硫酸镍晶体,为了进一步纯化并回收胆矾晶体,某课题小组设计了如图流程:
、Zn2+等)中提纯得到粗硫酸镍晶体,为了进一步纯化并回收胆矾晶体,某课题小组设计了如图流程:
已知:相关离子浓度为0.1mol/L时,形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Cu2+ | Fe2+ | Fe3+ | Ca2+ | Zn2+ | Ni2+ |
| 开始沉淀的pH | 4.2 | 6.3 | 1.5 | 11.8 | 6.2 | 6.9 |
| 沉淀完全的uH | 6.7 | 8.3 | 2.8 | 13.8 | 8.2 | 8.9 |
(2)为了使“溶液1”中的反应充分进行,需要通入稍过量的H2S,写出Fe3+与H2S发生反应的离子方程式:
(3)请结合离子方程式解释向“溶液2”中加入Ni(OH)2的原因
(4)“操作X”为在
(5)若“溶液3”中Ca2+的浓度为0.001mol/L,取等体积的NiF2溶液与该溶液混合,要使反应结束时c(Ca2+)<10-5mol/L,则所加NiF2溶液的浓度至少为
(6)室温下选择萃取剂P204(二乙基已基磷酸,用HR表示),其萃取原理为nHR+Mn+⇌MRn+nH+,试剂a为

您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】连二亚硫酸钠( )俗称保险粉,广泛用于纺织、医药、选矿、造纸工业。某实验小组拟用甲酸钠、烧碱、二氧化硫制备连二亚硫酸钠并测定其纯度。
)俗称保险粉,广泛用于纺织、医药、选矿、造纸工业。某实验小组拟用甲酸钠、烧碱、二氧化硫制备连二亚硫酸钠并测定其纯度。
查阅资料:连二亚硫酸钠是一种白色粉末,易溶于水,难溶于乙醇;加热到80℃以上分解并出二氧化硫气体;在空气中能被氧化,是一种强还原剂。
Ⅰ. 的制备
的制备 时选用上图所示装置中的
时选用上图所示装置中的________ (填标号)。选用以下试剂中的________ (填标号)。
A.铜粉 B. 固体 C.98%浓硫酸 D.70%浓硫酸 E.10%稀硫酸
固体 C.98%浓硫酸 D.70%浓硫酸 E.10%稀硫酸
Ⅱ. 的制备
的制备
制用如图所示实验装置(加热、搅拌及夹持装置省略)制备 ,实验步骤如下:
,实验步骤如下: 一段时间;
一段时间;
ii.然后持续通入 ,保持水浴温度75℃左右,反应20min;
,保持水浴温度75℃左右,反应20min;
iii.停止加热,冷却至50℃;
iv.拆卸装置,将d中的混合物进行过滤、洗涤,得到粗产品。
(2)步骤Ⅰ中先通入 的目的是
的目的是________ (答出两点)。
(3)装置d中发生的主要反应的化学方程式为________ 。
(4)步骤iv中“洗涤”时,洗涤剂为________ (填“水”或“乙醇”),进一步提纯 的方法为
的方法为________ 。
Ⅲ.产品纯度的测定
称取纯化后的产品mg溶于水,加入足量 溶液后配成250mL待测液,量取25.00mL待测液于锥形瓶中,滴入2~3滴指示剂亚甲基蓝溶液,用
溶液后配成250mL待测液,量取25.00mL待测液于锥形瓶中,滴入2~3滴指示剂亚甲基蓝溶液,用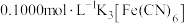 标准溶液进行滴定{已知滴定过程中
标准溶液进行滴定{已知滴定过程中 转化为
转化为 ,
, 转化为
转化为 ,杂质不参与反应},达到滴定终点时消耗标准溶液VmL。
,杂质不参与反应},达到滴定终点时消耗标准溶液VmL。
(5)滴定过程中发生反应的离子方程式为________ 。
(6)产品中 的质量分数为
的质量分数为________ 。
(7)下列情况会造成测定结果偏小的是________ (填标号)。
A.盛放待测液的锥形瓶内残留少量蒸馏水
B.未用 标准液润洗酸式滴定管
标准液润洗酸式滴定管
C.滴定终点时俯视读数
 )俗称保险粉,广泛用于纺织、医药、选矿、造纸工业。某实验小组拟用甲酸钠、烧碱、二氧化硫制备连二亚硫酸钠并测定其纯度。
)俗称保险粉,广泛用于纺织、医药、选矿、造纸工业。某实验小组拟用甲酸钠、烧碱、二氧化硫制备连二亚硫酸钠并测定其纯度。查阅资料:连二亚硫酸钠是一种白色粉末,易溶于水,难溶于乙醇;加热到80℃以上分解并出二氧化硫气体;在空气中能被氧化,是一种强还原剂。
Ⅰ.
 的制备
的制备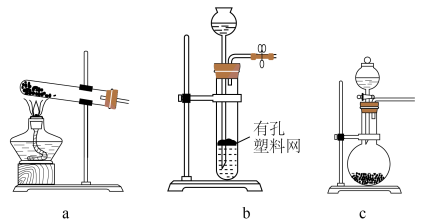
 时选用上图所示装置中的
时选用上图所示装置中的A.铜粉 B.
 固体 C.98%浓硫酸 D.70%浓硫酸 E.10%稀硫酸
固体 C.98%浓硫酸 D.70%浓硫酸 E.10%稀硫酸Ⅱ.
 的制备
的制备制用如图所示实验装置(加热、搅拌及夹持装置省略)制备
 ,实验步骤如下:
,实验步骤如下: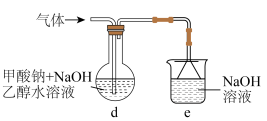
 一段时间;
一段时间;ii.然后持续通入
 ,保持水浴温度75℃左右,反应20min;
,保持水浴温度75℃左右,反应20min;iii.停止加热,冷却至50℃;
iv.拆卸装置,将d中的混合物进行过滤、洗涤,得到粗产品。
(2)步骤Ⅰ中先通入
 的目的是
的目的是(3)装置d中发生的主要反应的化学方程式为
(4)步骤iv中“洗涤”时,洗涤剂为
 的方法为
的方法为Ⅲ.产品纯度的测定
称取纯化后的产品mg溶于水,加入足量
 溶液后配成250mL待测液,量取25.00mL待测液于锥形瓶中,滴入2~3滴指示剂亚甲基蓝溶液,用
溶液后配成250mL待测液,量取25.00mL待测液于锥形瓶中,滴入2~3滴指示剂亚甲基蓝溶液,用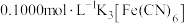 标准溶液进行滴定{已知滴定过程中
标准溶液进行滴定{已知滴定过程中 转化为
转化为 ,
, 转化为
转化为 ,杂质不参与反应},达到滴定终点时消耗标准溶液VmL。
,杂质不参与反应},达到滴定终点时消耗标准溶液VmL。(5)滴定过程中发生反应的离子方程式为
(6)产品中
 的质量分数为
的质量分数为(7)下列情况会造成测定结果偏小的是
A.盛放待测液的锥形瓶内残留少量蒸馏水
B.未用
 标准液润洗酸式滴定管
标准液润洗酸式滴定管C.滴定终点时俯视读数
您最近半年使用:0次
【推荐3】废旧锂离子电池的回收利用意义重大,其正极废料的主要成分是LiCoO2、铝、炭黑及其他微量杂质,回收利用的流程如下:
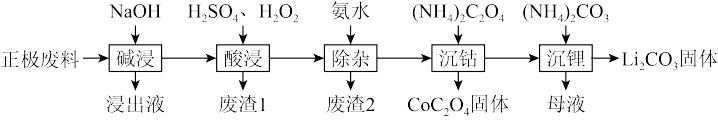
(1)“碱浸”步骤中铝溶解的离子方程式为_______ ,“废渣1”的主要成分为_______ 。
(2)LiCoO2中Co的化合价为_______ ,“酸浸”步骤中LiCoO2固体溶解的化学方程式为_______ ,反应中H2O2的作用为_______ 。
(3)“酸浸”后的溶液中含有少量Fe3+、Al3+、Cu2+,离子的沉淀率随pH的变化如图所示。“除杂”步骤中加入氨水调节溶液的pH约为_______ ,理由是_______ 。
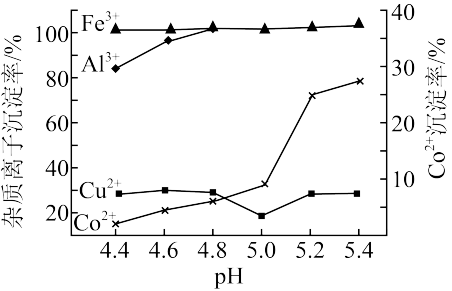
(4)母液中溶质的主要成分是_______ ,生成Li2CO3固体的离子方程式为_______ 。

(1)“碱浸”步骤中铝溶解的离子方程式为
(2)LiCoO2中Co的化合价为
(3)“酸浸”后的溶液中含有少量Fe3+、Al3+、Cu2+,离子的沉淀率随pH的变化如图所示。“除杂”步骤中加入氨水调节溶液的pH约为

(4)母液中溶质的主要成分是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】我国科学家屠呦呦因成功从黄花蒿中提取抗疟药物青蒿素而获得2015年诺贝尔奖。从黄花蒿中提取青蒿素的流程如下:
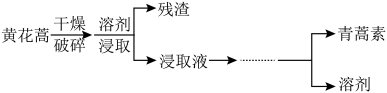
已知:青蒿素为白色针状晶体,易溶于乙醇、乙醚、苯和汽油等有机溶剂,不溶于水,熔点为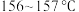 ,沸点为
,沸点为 ,热稳定性差。屠呦呦团队经历了使用不同溶剂和不同温度的探究过程,实验结果如下:
,热稳定性差。屠呦呦团队经历了使用不同溶剂和不同温度的探究过程,实验结果如下:
(1)对黄花蒿进行破碎的目的是___________ ;用水作溶剂,提取无效的原因可能是___________ 。
(2)研究发现,青蒿素分子中的某个基团对热不稳定。分析用乙醚作溶剂,提取效率高于乙醇的原因是___________ 。
(3)从青蒿(粉末)中提取青蒿素的方法以萃取原理为基础,乙醚浸提法的具体操作如下:
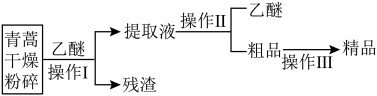
①乙醚浸提法涉及到的操作中,不会用到的装置是___________ 。
A.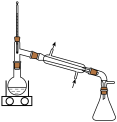 B.
B.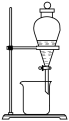 C.
C.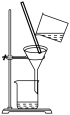 D.
D.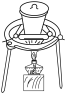
②操作Ⅲ的主要过程可能是___________ 。
A.加水溶解,蒸发浓缩、冷却结晶 B.加 的乙醇,浓缩、结晶、过滤
的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液 D.加入乙醇后,再加入苯或汽油进行萃取
(4)某科研小组通过控制其他实验条件不变,来研究原料的粒度、提取时间和提取温度对青蒿素提取速率的影响,其结果如下图所示:

由上图可知控制其他实验条件不变,采用的最佳粒度、时间和温度为___________ 。
(5)由上可知,在提取青蒿素的过程中,应充分考虑物质的___________ 等性质(写出两点即可)。

已知:青蒿素为白色针状晶体,易溶于乙醇、乙醚、苯和汽油等有机溶剂,不溶于水,熔点为
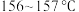 ,沸点为
,沸点为 ,热稳定性差。屠呦呦团队经历了使用不同溶剂和不同温度的探究过程,实验结果如下:
,热稳定性差。屠呦呦团队经历了使用不同溶剂和不同温度的探究过程,实验结果如下:| 溶剂 | 水 | 乙醇 | 乙醚 |
沸点/ | 100 | 78 | 35 |
| 提取效率 | 几乎为0 |  |  |
(2)研究发现,青蒿素分子中的某个基团对热不稳定。分析用乙醚作溶剂,提取效率高于乙醇的原因是
(3)从青蒿(粉末)中提取青蒿素的方法以萃取原理为基础,乙醚浸提法的具体操作如下:

①乙醚浸提法涉及到的操作中,不会用到的装置是
A.
 B.
B. C.
C. D.
D.
②操作Ⅲ的主要过程可能是
A.加水溶解,蒸发浓缩、冷却结晶 B.加
 的乙醇,浓缩、结晶、过滤
的乙醇,浓缩、结晶、过滤C.加入乙醚进行萃取分液 D.加入乙醇后,再加入苯或汽油进行萃取
(4)某科研小组通过控制其他实验条件不变,来研究原料的粒度、提取时间和提取温度对青蒿素提取速率的影响,其结果如下图所示:

由上图可知控制其他实验条件不变,采用的最佳粒度、时间和温度为
(5)由上可知,在提取青蒿素的过程中,应充分考虑物质的
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】[Co(NH3)5Cl]Cl2是一种重要的Co(III)配合物,在实验室中制备流程如图所示:
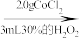

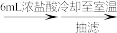

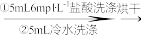

总的实验原理:2CoCl2+2NH4Cl+H2O2+8NH3=2[Co(NH3)5H2O]Cl3 △H<0;[Co(NH3)5H2O]Cl3中的H2O被Cl-取代生成目标产物[Co(NH3)5Cl]Cl2。
回答下列问题:
(1)结合实验原理可知,浓氨水为制备过程主要提供_______ (填微粒符号,下同),使用NH4Cl为制备过程主要提供_______ 。
(2)加入6 mL浓盐酸后,要及时将锥形瓶用胶塞封闭,否则目标产物中将混有大量副产物[Co(NH3)5H2O]Cl3,试分析用胶塞封闭的目的:_______ 。
(3)3 mL 30%的H2O2应采用缓慢滴加的方式,若一次性加入产生的不良后果是_______ 。
(4)“抽滤”在如图装置中进行,利用抽气泵将装置内的空气不断抽出,可使装置内的压强小于外界大气压,试分析抽滤较普通过滤的优点有_______ (任写一点)。
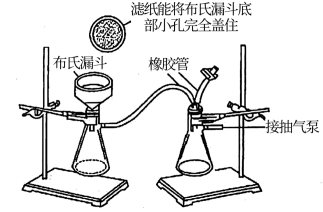
(5)“沉淀”用温度更低的冷水洗涤的优点是_______ 。
(6)已知水溶液中:[Co(NH3)5H2O]Cl3=[Co(NH3)5H2O]3++3Cl-;[Co(NH3)5Cl]Cl2=[Co(NH3)5C]2++2Cl-;不考虑[Co(NH3)5Cl]2+=[Co(NH3)5]3++Cl-。试设计区分[Co(NH3)5H2O]Cl3晶体和[Co(NH3)5C]Cl2晶体的实验方案:_______ (所用试剂:AgNO3溶液)。

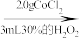

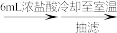

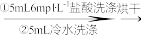

总的实验原理:2CoCl2+2NH4Cl+H2O2+8NH3=2[Co(NH3)5H2O]Cl3 △H<0;[Co(NH3)5H2O]Cl3中的H2O被Cl-取代生成目标产物[Co(NH3)5Cl]Cl2。
回答下列问题:
(1)结合实验原理可知,浓氨水为制备过程主要提供
(2)加入6 mL浓盐酸后,要及时将锥形瓶用胶塞封闭,否则目标产物中将混有大量副产物[Co(NH3)5H2O]Cl3,试分析用胶塞封闭的目的:
(3)3 mL 30%的H2O2应采用缓慢滴加的方式,若一次性加入产生的不良后果是
(4)“抽滤”在如图装置中进行,利用抽气泵将装置内的空气不断抽出,可使装置内的压强小于外界大气压,试分析抽滤较普通过滤的优点有

(5)“沉淀”用温度更低的冷水洗涤的优点是
(6)已知水溶液中:[Co(NH3)5H2O]Cl3=[Co(NH3)5H2O]3++3Cl-;[Co(NH3)5Cl]Cl2=[Co(NH3)5C]2++2Cl-;不考虑[Co(NH3)5Cl]2+=[Co(NH3)5]3++Cl-。试设计区分[Co(NH3)5H2O]Cl3晶体和[Co(NH3)5C]Cl2晶体的实验方案:
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某探究学习小组在实验室中,模拟并改进侯氏制碱法制备 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如下图:
,实验流程如下图:
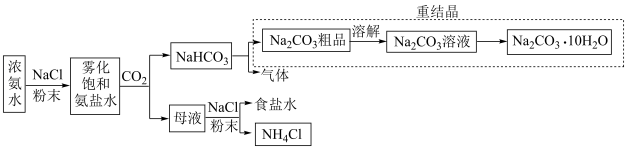
I.根据图中信息回答下列问题:
(1)生成 的总反应化学方程式为
的总反应化学方程式为___________ 。
(2)实验小组使用雾化饱和氨盐水吸收 ,优点是
,优点是___________ 。
Ⅱ.制得的纯碱粗品中常含有少量 。该小组拟测定纯碱样品
。该小组拟测定纯碱样品 的质量分数。
的质量分数。
(3)设计实验方案检验粗品中 的存在:取少量样品于试管中,加水溶解,
的存在:取少量样品于试管中,加水溶解,___________ ,若有白色沉淀生成,则证明样品中含有 。
。
(4)产品分析:把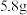 含有少量
含有少量 杂质的
杂质的 样品与足量稀硫酸反应后,产生的气体先通过足量浓硫酸,再通过足量
样品与足量稀硫酸反应后,产生的气体先通过足量浓硫酸,再通过足量 ,
, 增重
增重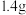 。则产品纯度为
。则产品纯度为___________ (用百分数表示,保留到小数点后1位)。
(5)对产品以重结晶法进行提纯,提纯过程中从溶液中得到 晶体的实验操作为
晶体的实验操作为_____ 、_______ 、过滤。
 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如下图:
,实验流程如下图:
I.根据图中信息回答下列问题:
(1)生成
 的总反应化学方程式为
的总反应化学方程式为(2)实验小组使用雾化饱和氨盐水吸收
 ,优点是
,优点是Ⅱ.制得的纯碱粗品中常含有少量
 。该小组拟测定纯碱样品
。该小组拟测定纯碱样品 的质量分数。
的质量分数。(3)设计实验方案检验粗品中
 的存在:取少量样品于试管中,加水溶解,
的存在:取少量样品于试管中,加水溶解, 。
。(4)产品分析:把
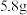 含有少量
含有少量 杂质的
杂质的 样品与足量稀硫酸反应后,产生的气体先通过足量浓硫酸,再通过足量
样品与足量稀硫酸反应后,产生的气体先通过足量浓硫酸,再通过足量 ,
, 增重
增重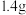 。则产品纯度为
。则产品纯度为(5)对产品以重结晶法进行提纯,提纯过程中从溶液中得到
 晶体的实验操作为
晶体的实验操作为
您最近半年使用:0次



