已知某温度下纯水中的c(H+)=2×10-7mol/L,对此下列说法正确的是( )
| A.若向水中加入少量盐酸,则水的电离度减小 |
| B.该温度低于25℃ |
| C.此温度下水的离子积为常温下的两倍 |
| D.据此无法求算水中c(OH-) |
更新时间:2020-02-12 09:57:48
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列图示与对应的叙述相符的是
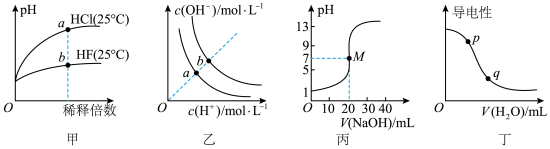

A.由图甲可知,a点 的数值比b点 的数值比b点 的数值大 的数值大 |
B.图乙表示不同温度下水溶液中 和 和 的浓度变化曲线,图中a点对应温度高于b点 的浓度变化曲线,图中a点对应温度高于b点 |
C.图丙表示 溶液滴定 溶液滴定 溶液的滴定曲线,M点水的电离程度最大 溶液的滴定曲线,M点水的电离程度最大 |
| D.图丁表示向醋酸稀溶液中加水时溶液的导电性变化,图中p点醋酸的电离程度大于q点 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】在某温度下,水的离子积常数为1×10-12,该温度下等体积的①pH=0的H2SO4溶液、②0.05 mol·L-1的Ba(OH)2溶液、③pH=10的Na2S溶液、④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比(①∶②∶③∶④)是
| A.1∶10∶1010∶107 | B.1∶5∶5×109∶5×106 |
| C.1∶20∶1010∶107 | D.1∶10∶102∶107 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】已知NaHSO4在水中的电离方程式为:NaHSO4 = Na+ + H+ + SO42—。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确 的是( )
| A.该温度高于25℃ |
| B.由水电离出来的H+的浓度是1.0×10-10mol·L-1 |
| C.NaHSO4晶体的加入抑制了水的电离 |
| D.该温度下加入等体积pH为12的NaOH溶液可使该溶液恰好呈中性 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】水是生命之源,下列关于水的说法正确的是
| A.水是非电解质 |
| B.pH=6.8的纯水呈中性 |
| C.降低温度,水的Kw增大 |
| D.在100℃,纯水的pH<7,因此显酸性 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列操作中,能使电离平衡 H2O H++OH-,向右移动且溶液呈酸性的是( )
H++OH-,向右移动且溶液呈酸性的是( )
 H++OH-,向右移动且溶液呈酸性的是( )
H++OH-,向右移动且溶液呈酸性的是( )| A.向水中加入NaHSO3溶液 | B.向水中加入 NH4Cl 溶液 |
| C.向水中加入CH3COONa 溶液 | D.将水加热到 100℃,使 pH=6 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】其它条件不变,增大反应体系的压强,下列数据会明显增大的是( )
| A.二氧化硫与氧气反应生成三氧化硫气体的化学反应速率v |
| B.醋酸的电离度α |
| C.合成氨的化学平衡常数K |
| D.水的离子积常数Kw |
您最近一年使用:0次

 、Ba2+、
、Ba2+、 、I-
、I- 、
、

 、
、
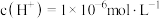 ,
,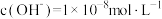
 ,其中
,其中
 HCl溶液和
HCl溶液和 溶液的pH均等于1
溶液的pH均等于1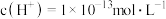 时,此溶液一定是酸溶液
时,此溶液一定是酸溶液



