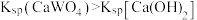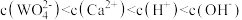下列实验操作与预期实验目的或所得实验结论一致的是
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向含有少量 的 的 溶液中加入足量 溶液中加入足量 粉末,搅拌一段时间后过滤 粉末,搅拌一段时间后过滤 | 除去 溶液中少量 溶液中少量 |
| B | 向某溶液中加入 溶液生成白色沉淀,继续加稀硝酸沉淀不消失 溶液生成白色沉淀,继续加稀硝酸沉淀不消失 | 证明溶液中含 |
| C | 向某溶液中加入稀盐酸,放出无色无味气体,将气体通入澄清石灰水,石灰水变浑浊 | 证明该溶液中存在 |
| D | 向 溶液中滴加少量酸性 溶液中滴加少量酸性 溶液, 溶液, 溶液褪色 溶液褪色 | 证明 具有氧化性 具有氧化性 |
| A.A | B.B | C.C | D.D |
更新时间:2020-02-13 21:52:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列是对某溶液进行离子检测的方法和结论,其中正确的是
| A.先加入适量的硝酸酸化,再加入BaCl2溶液,产生白色沉淀,则溶液中一定含有大量的SO42- |
| B.加入足量的CaCl2溶液,产生白色溶液,则溶液中一定含有大量的CO32- |
| C.加入NaOH溶液后加热产生有刺激性气味的气体,则溶液中一定含有大量的NH4+ |
| D.先加入适量的盐酸酸化,再加入AgNO3溶液,产生白色沉淀,则溶液中一定含有大量的Cl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】有一瓶可能部分被氧化的Na2SO3溶液,某同学取少量此溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀。下述有关此实验的结论正确的是( )
| A.Na2SO3已部分被空气中的氧气氧化 |
| B.加入 Ba(NO3)2溶液后,生成的沉淀中一定含有BaSO4 |
| C.加足量硝酸后的白色沉淀一定是BaSO4 |
| D.此实验能确定Na2SO3是否部分被氧化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验操作及现象与对应结论匹配的是
| 选项 | 实验操作及现象 | 结论 |
| A | 取一定量NaSO4样品,溶解后加入BaCl2溶液,产生白色沉淀。加入浓HNO3,仍有沉淀。 | 此样品中含有 |
| B | 相同温度下,分别测定相同浓度的NaNO2和CH3COONa溶液pH,NaNO2溶液的pH 约为8,CH3COONa溶液的pH约为9 | 相同温度下Ka(HNO2)<Ka(CH3COOH) |
| C | 向硫酸铜溶液中滴加浓盐酸至过量,溶液由蓝色变为绿色 | [Cu(H2O)4]2+转化为[CuCl4]2- |
| D | 将Zn(OH)2固体粉末加入过量NaOH溶液中,充分搅拌,溶解得到无色溶液。 | Zn(OH)2既体现碱性又体现酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验的现与对应结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向 溶液中加入 溶液中加入 溶液 溶液 | 有白色沉淀生成 |  结合 结合 的能力比 的能力比 弱 弱 |
| B | 用pH试纸测定NaCl和NaF溶液的pH | 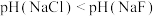 | F元素的非金属性强于Cl |
| C | 将 样品溶于稀 样品溶于稀 后,滴加KSCN溶液 后,滴加KSCN溶液 | 溶液显红色 |  晶体已氧化变质 晶体已氧化变质 |
| D | 向久置的 溶液中加入足量 溶液中加入足量 溶液,再加入足量稀盐酸 溶液,再加入足量稀盐酸 | 先出现白色沉淀后部分溶解 | 部分 氧化变质 氧化变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验中,各实验操作对应的现象以及结论均正确且具有因果关系的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将一片鲜花花瓣放入盛有干燥氯气的集气瓶中 | 鲜花花瓣未变色 | 干燥的氯气没有漂白性 |
| B | 向某溶液中滴入几滴K3[Fe(CN)6]溶液 | 有蓝色沉淀生成 | 该溶液中含有Fe3+ |
| C | 测定等浓度的Na2C2O4的溶液和Na2CO3溶液的pH | Na2CO3溶液的pH较大 | 酸性:H2C2O4>H2CO3 |
| D | 常温下,向含等浓度Mg2+和Cu2+的溶液中逐滴加入NaOH溶液 | 先生成蓝色沉淀 | 常温下,Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】高纯三氯氧磷 是集成电路、太阳能电池生产的掺杂剂。实验室可通过以下实验步骤测定三氯氧磷产品中氯元素的含量,并计算产品的纯度[已知:常温下,
是集成电路、太阳能电池生产的掺杂剂。实验室可通过以下实验步骤测定三氯氧磷产品中氯元素的含量,并计算产品的纯度[已知:常温下,
 ,
, ,
, 呈白色]。
呈白色]。
①取 产品置于盛
产品置于盛 蒸馏水的水解瓶中,摇动至完全水解,将水解液配成
蒸馏水的水解瓶中,摇动至完全水解,将水解液配成 溶液并预处理排除含磷粒子的影响。
溶液并预处理排除含磷粒子的影响。
②取 溶液于锥形瓶中,向其中加入
溶液于锥形瓶中,向其中加入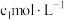 的
的 标准溶液
标准溶液 ,使
,使 完全沉淀,再加入
完全沉淀,再加入 硝基苯,振荡,使沉淀表面被有机物覆盖;然后加入几滴
硝基苯,振荡,使沉淀表面被有机物覆盖;然后加入几滴 溶液作指示剂,用
溶液作指示剂,用
 标准溶液滴定过量
标准溶液滴定过量 至终点,所用体积为
至终点,所用体积为 。
。
假设杂质不参加反应,则下列说法正确的是
 是集成电路、太阳能电池生产的掺杂剂。实验室可通过以下实验步骤测定三氯氧磷产品中氯元素的含量,并计算产品的纯度[已知:常温下,
是集成电路、太阳能电池生产的掺杂剂。实验室可通过以下实验步骤测定三氯氧磷产品中氯元素的含量,并计算产品的纯度[已知:常温下,
 ,
, ,
, 呈白色]。
呈白色]。①取
 产品置于盛
产品置于盛 蒸馏水的水解瓶中,摇动至完全水解,将水解液配成
蒸馏水的水解瓶中,摇动至完全水解,将水解液配成 溶液并预处理排除含磷粒子的影响。
溶液并预处理排除含磷粒子的影响。②取
 溶液于锥形瓶中,向其中加入
溶液于锥形瓶中,向其中加入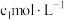 的
的 标准溶液
标准溶液 ,使
,使 完全沉淀,再加入
完全沉淀,再加入 硝基苯,振荡,使沉淀表面被有机物覆盖;然后加入几滴
硝基苯,振荡,使沉淀表面被有机物覆盖;然后加入几滴 溶液作指示剂,用
溶液作指示剂,用
 标准溶液滴定过量
标准溶液滴定过量 至终点,所用体积为
至终点,所用体积为 。
。假设杂质不参加反应,则下列说法正确的是
A.配制好的 标准溶液可盛放在棕色广口试剂瓶中 标准溶液可盛放在棕色广口试剂瓶中 |
| B.实验过程中可用甲苯代替硝基苯进行实验 |
| C.滴定终点时锥形瓶中有血红色沉淀生成 |
D.实验过程中若忘记加入硝基苯,会导致所测 的含量偏低 的含量偏低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
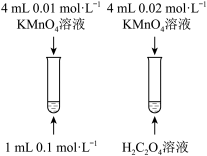
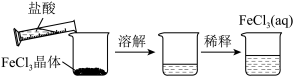
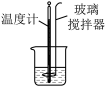
【推荐2】下图所示的实验,可以达到实验目的的是
A.探究浓度对化学反应速率的影响 (两个试管中均是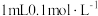 的 的 ) ) | B.验证 溶解度大于 溶解度大于 |
 | 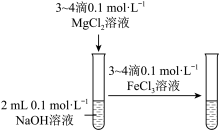 |
C.配制 溶液 溶液 | D.测定中和反应的反应热 |
 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于某无色溶液中离子检验的操作、现象与结论对应正确的是
| 检验操作 | 现象 | 结论 | |
| A | 加入盐酸酸化的氯化钡 | 产生白色沉淀 | 一定有 SO42- |
| B | 加入氯水与四氯化碳 | 有机层呈紫色 | 一定有 I- |
| C | 加入足量稀盐酸 | 产生无色气体 | 一定有 CO32- |
| D | 加入硝酸银 | 产生白色沉淀 | 一定有 Cl- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某溶液中可能含有I-、Cl-、Fe3+、SO32-,向该溶液中加溴水,溶液无色。因此可知原溶液中

| A.肯定不含I- | B.肯定不含Cl- |
| C.肯定含Fe3+ | D.肯定不含有SO32- |
您最近一年使用:0次

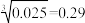 )。下列分析正确的是
)。下列分析正确的是