聚合氯化铝晶体的化学式为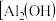
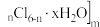 ,它是一种高效无机水处理剂,它的制备原理是调节增大
,它是一种高效无机水处理剂,它的制备原理是调节增大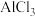 溶液的pH,通过促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣--铝灰,它主要含
溶液的pH,通过促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣--铝灰,它主要含 、Al,还有
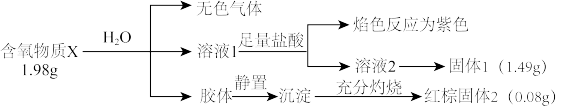
、Al,还有 等杂质。聚合氯化铝生产的工艺流程如下:
等杂质。聚合氯化铝生产的工艺流程如下:
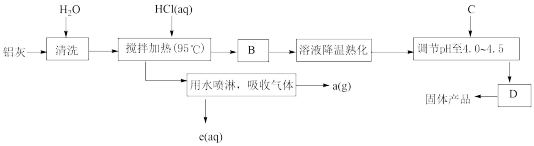
(1)搅拌加热操作过程中发生反应的离子方程式为:______ 。
(2)生产过程中B和D的操作名称分别是______ 和______ 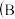 和D均为简单操作
和D均为简单操作 。
。
(3)反应中副产品a是______ 。
(4)生产过程中可循环使用的物质是______  用化学式表示
用化学式表示 。
。
(5)调节pH至 的目的是
的目的是______ 。
(6)实验室要测定水处理剂产品中n和x的值。为使测定结果更准确,需得到的晶体较纯净。生产过程C物质可选用下列物质中的______ 。
A.氢氧化钠 铝
铝 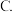 氨水
氨水  氧化铝
氧化铝 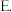 偏铝酸钠
偏铝酸钠
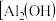
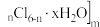 ,它是一种高效无机水处理剂,它的制备原理是调节增大
,它是一种高效无机水处理剂,它的制备原理是调节增大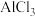 溶液的pH,通过促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣--铝灰,它主要含
溶液的pH,通过促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣--铝灰,它主要含 、Al,还有
、Al,还有 等杂质。聚合氯化铝生产的工艺流程如下:
等杂质。聚合氯化铝生产的工艺流程如下:
(1)搅拌加热操作过程中发生反应的离子方程式为:
(2)生产过程中B和D的操作名称分别是
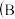 和D均为简单操作
和D均为简单操作 。
。(3)反应中副产品a是
(4)生产过程中可循环使用的物质是
 用化学式表示
用化学式表示 。
。(5)调节pH至
 的目的是
的目的是(6)实验室要测定水处理剂产品中n和x的值。为使测定结果更准确,需得到的晶体较纯净。生产过程C物质可选用下列物质中的
A.氢氧化钠
 铝
铝  氨水
氨水  氧化铝
氧化铝  偏铝酸钠
偏铝酸钠
更新时间:2020-02-17 10:51:16
|
相似题推荐
【推荐1】Ⅰ.由硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、Al2O3和SiO2)得到绿矾(FeSO4·7H2O),然后制取透明氧化铁颜料的流程如下:

已知:①透明氧化铁又称纳米氧化铁,粒子直径微小(10~90 nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
②Fe3+能将FeS2中的硫元素氧化为+6价。
回答下列问题:
(1)FeS2的电子式为_______ 。
(2)“滤渣”中的主要成分是_______ 。
(3)流程中“ ”环节的目的是
”环节的目的是_______ 。
(4)“还原”过程中涉及的离子方程式为_______ 。
(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到均匀、色泽纯正的氢氧化铁,而且还可以_______ 。
(6)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁红的含量。已知Fe(SCN)3的吸光度A(对特定波长光的吸收程度)与Fe3+标准溶液浓度的关系如图所示:

称取3.47 g透明氧化铁,用稀硫酸溶解并定容至1 L,准确移取该溶液10.00 mL,加入足量KSCN溶液,再用蒸馏水定容至100 mL。测得溶液吸光度A=0.8,则透明氧化铁中氧化铁红的质量分数为_______ %(保留小数点后一位)。
Ⅱ.重晶石(BaSO4)作为原料制备金属钡及其他含钡化合物的方法如下图:

完成下列填空:
(7)Ba在元素周期表中的位置为_______ ,最外层电子的电子云形状是_______ 。图中涉及的第二周期元素电负性由大到小的顺序是_______ (用元素符号表示),可以判断其中两种元素非金属性强弱的反应是_______ (选填流程中的反应编号)。
(8)配平BaS与稀硝酸反应的化学方程式:_______
_______BaS+_______HNO3=_______Ba(NO3)2+_______S+_______NO↑+_______H2O

已知:①透明氧化铁又称纳米氧化铁,粒子直径微小(10~90 nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
②Fe3+能将FeS2中的硫元素氧化为+6价。
回答下列问题:
(1)FeS2的电子式为
(2)“滤渣”中的主要成分是
(3)流程中“
 ”环节的目的是
”环节的目的是(4)“还原”过程中涉及的离子方程式为
(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到均匀、色泽纯正的氢氧化铁,而且还可以
(6)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁红的含量。已知Fe(SCN)3的吸光度A(对特定波长光的吸收程度)与Fe3+标准溶液浓度的关系如图所示:

称取3.47 g透明氧化铁,用稀硫酸溶解并定容至1 L,准确移取该溶液10.00 mL,加入足量KSCN溶液,再用蒸馏水定容至100 mL。测得溶液吸光度A=0.8,则透明氧化铁中氧化铁红的质量分数为
Ⅱ.重晶石(BaSO4)作为原料制备金属钡及其他含钡化合物的方法如下图:

完成下列填空:
(7)Ba在元素周期表中的位置为
(8)配平BaS与稀硝酸反应的化学方程式:
_______BaS+_______HNO3=_______Ba(NO3)2+_______S+_______NO↑+_______H2O
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】某锂离子电池正极由钴酸锂( )、铝箔、石墨等组成。某研究小组利用该锂离子电池正极材料回收制备
)、铝箔、石墨等组成。某研究小组利用该锂离子电池正极材料回收制备 ,同时回收锂,流程如下:
,同时回收锂,流程如下:
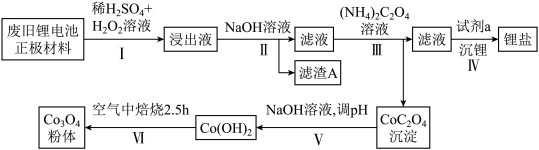
已知:i.锂离子电池充电时负极反应式为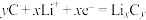 ,锂离子电池正极充放电过程中发生
,锂离子电池正极充放电过程中发生 与
与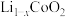 之间的转化。
之间的转化。
ii.某些物质的溶解度(s)如下表所示:
请回答下列问题:
(1)过程I浸出液产生气泡,钴酸锂发生反应的化学方程式为_______ ,在取出正极材料之前需要先将废旧电池“放电处理”,其目的是_______ (答出两点)。
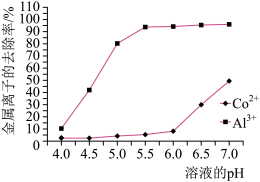
(2)过程Ⅱ中,不同pH下金属离子的去除效果如图所示。该过程加碱调节pH的范围是_______ ,其理由是_______ 。
(3)过程Ⅳ中操作方法为:向滤液中加入稍过量的_______ ,充分搅拌,_______ ,用热水洗涤后干燥。
(4)过程V中,常温下 开始转化为
开始转化为 的pH为
的pH为_______ 。(已知: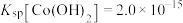 ,
,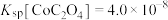 )
)
 )、铝箔、石墨等组成。某研究小组利用该锂离子电池正极材料回收制备
)、铝箔、石墨等组成。某研究小组利用该锂离子电池正极材料回收制备 ,同时回收锂,流程如下:
,同时回收锂,流程如下:
已知:i.锂离子电池充电时负极反应式为
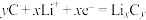 ,锂离子电池正极充放电过程中发生
,锂离子电池正极充放电过程中发生 与
与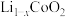 之间的转化。
之间的转化。ii.某些物质的溶解度(s)如下表所示:
| t/℃ | 20 | 40 | 60 | 80 |
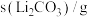 | 1.33 | 1.17 | 1.01 | 0.85 |
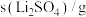 | 34.2 | 32.8 | 31.9 | 30.7 |
请回答下列问题:
(1)过程I浸出液产生气泡,钴酸锂发生反应的化学方程式为
(2)过程Ⅱ中,不同pH下金属离子的去除效果如图所示。该过程加碱调节pH的范围是

(3)过程Ⅳ中操作方法为:向滤液中加入稍过量的
(4)过程V中,常温下
 开始转化为
开始转化为 的pH为
的pH为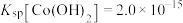 ,
,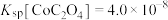 )
)
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】纳米CdSe(硒化镉)可作光学材料。在一定条件下,由Na2SO3和Se反应生成Na2SeSO3(硒代硫酸钠),再由CdCl2形成的配合物与Na2SeSO3反应制得CdSe颗粒,流程图如下:

注①CdCl2能与配位剂L形成配合物[Cd(L)n]Cl2
[Cd(L)n]Cl2=[Cd(L)n]2++2Cl-;[Cd(L)n]2+⇌Cd2++nL
②纳米颗粒通常指平均粒径为1nm-100nm的粒子。请回答:


(1)图1加热回流装置中,仪器a的名称为_____ ,进水口为_____ (填1或2)。
(2)研究表明,由Na2SeSO3制取CdSe分两步进行,已知第二步反应为:HSe-与[Cd(L)n]2+反应生成CdSe,请完成第一步反应的离子方程式_____ 。
(3)CdSe纳米颗粒的大小影响其发光性质,某研究小组在一定配位剂浓度下,探究了避光加热步骤中反应时间和温度对纳米颗粒平均粒径的影响,如图2所示,同时探究了某温度下配位剂浓度对纳米颗粒平均粒径的影响,如图3所示。下列说法正确的是_____(填写序号)
(4)已知Se可由SO2通入亚硒酸溶液制得,若以H2SeO3溶液为主要原料制取高纯硒单质,请补充完整实验方案:_____ ,得高纯硒单质。(可能使用的试剂:亚硫酸钠固体、10%硫酸溶液、70%硫酸溶液、BaCl2溶液、1mol·L-1NaOH溶液)
(5)实验室常用氧化还原滴定法测定某样品中Se的质量分数,步骤如下:
I.取0.8400g样品充分磨碎,加酸煮沸配成H2SeO3溶液,将溶液完全转移到250mL容量瓶中后定容。
II.准确量取25.00mL待测液于锥形瓶中,加入0.0200mol·L-1KMnO4标准溶液25.00mL,向锥形瓶中再加入25.00mL0.06mol·L-1Fe2+溶液,加入磷酸后再用0.0200mol·L-1KMnO4滴定,消耗KMnO4溶液10.00mL。
已知:Se的最高价含氧酸氧化Fe2+较慢,在该滴定过程可忽略此反应。计算硒的质量分数_____ (写出计算过程)。

注①CdCl2能与配位剂L形成配合物[Cd(L)n]Cl2
[Cd(L)n]Cl2=[Cd(L)n]2++2Cl-;[Cd(L)n]2+⇌Cd2++nL
②纳米颗粒通常指平均粒径为1nm-100nm的粒子。请回答:


(1)图1加热回流装置中,仪器a的名称为
(2)研究表明,由Na2SeSO3制取CdSe分两步进行,已知第二步反应为:HSe-与[Cd(L)n]2+反应生成CdSe,请完成第一步反应的离子方程式
(3)CdSe纳米颗粒的大小影响其发光性质,某研究小组在一定配位剂浓度下,探究了避光加热步骤中反应时间和温度对纳米颗粒平均粒径的影响,如图2所示,同时探究了某温度下配位剂浓度对纳米颗粒平均粒径的影响,如图3所示。下列说法正确的是_____(填写序号)
| A.改变反应温度和反应时间,可以得到不同发光性质的CdSe纳米颗粒 |
| B.在图2所示的两种温度下,只有60℃反应条件下可得到2.7nm的CdSe颗粒 |
| C.若要在60℃得到3.0nm的CdSe纳米颗粒,可尝试降低配位剂浓度的方法 |
| D.在其他条件不变时,若要得到较大的CdSe颗粒,可采用降低温度的方法 |
(5)实验室常用氧化还原滴定法测定某样品中Se的质量分数,步骤如下:
I.取0.8400g样品充分磨碎,加酸煮沸配成H2SeO3溶液,将溶液完全转移到250mL容量瓶中后定容。
II.准确量取25.00mL待测液于锥形瓶中,加入0.0200mol·L-1KMnO4标准溶液25.00mL,向锥形瓶中再加入25.00mL0.06mol·L-1Fe2+溶液,加入磷酸后再用0.0200mol·L-1KMnO4滴定,消耗KMnO4溶液10.00mL。
已知:Se的最高价含氧酸氧化Fe2+较慢,在该滴定过程可忽略此反应。计算硒的质量分数
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】以炼锌厂的烟道灰(主要成分为ZnO,另含少量Fe2O3、CuO、SiO2、MnO等)为原料可生产草酸锌晶体(ZnC2O4·2H2O)。
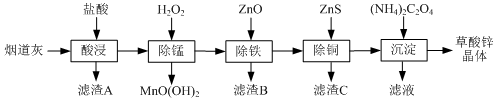
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
请问答下列问题:
(1)滤渣A的主要成分为________ ,滤渣B的主要成分为________ 。
(2)除锰过程中产生MnO(OH)2沉淀的离子方程式为____________________ 。
(3)①除铁(部分Cu2+可能被除去)时加入ZnO控制反应液pH的范围为________ 。
②上述流程中除铁与除铜的顺序不能颠倒,否则除铁率会减小,其原因是__________ 。
(4)沉淀后要获得干燥纯净草酸锌晶体,需进行的操作是_____________ 。
(5)将草酸锌晶体加热分解可得到一种纳米材料。加热过程中固体残留率随温度的变化如下图所示,300 ℃~460 ℃范围内,发生反应的化学方程式为_______ 。


有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 4.2 | 5.4 |
| 沉淀完全的pH | 3.3 | 9.7 | 6.7 | 8.2 |
请问答下列问题:
(1)滤渣A的主要成分为
(2)除锰过程中产生MnO(OH)2沉淀的离子方程式为
(3)①除铁(部分Cu2+可能被除去)时加入ZnO控制反应液pH的范围为
②上述流程中除铁与除铜的顺序不能颠倒,否则除铁率会减小,其原因是
(4)沉淀后要获得干燥纯净草酸锌晶体,需进行的操作是
(5)将草酸锌晶体加热分解可得到一种纳米材料。加热过程中固体残留率随温度的变化如下图所示,300 ℃~460 ℃范围内,发生反应的化学方程式为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】从铜转炉烟灰(主要成分ZnO还有Pb、Cu、Cd、As、Cl、F等元素)中回收锌、铜、铅等元素进行资源综合利用,具有重要意义。以铜转炉烟灰制备重要化工原料活性氧化锌的工艺流程如图所示。

已知:活性炭净化主要是除去有机杂质。
请回答以下问题:
(1)若浸出液中锌元素以[Zn(NH3)4]2+形式存在,则浸取时ZnO发生反应的离子方程式为___ 。
(2)在反应温度为50℃,反应时间为lh时,测定各元素的浸出率与氯化铵溶液浓度的关系如图,结合流程图分析,氯化铵适宜的浓度为___ mol·L-1。

(3)若浸出液中c(AsO43-)=6.0×10-3mol•L-1,现将8.0×10-3mol•L-1FeC13溶液与浸出液等体积混合生成砷酸铁沉淀。若该温度时Ksp(FeAsO4)=2.0×10-22,则反应后溶液中c(AsO43-)=___ mol•L-1。
(4)滤渣II的主要成分为___ ;除杂3是置换除杂过程,则此过程主要除去的金属有___ (填化学式)。
(5)沉锌得到的物质为Zn(NH3)2C12,请写出水解转化的化学方程式___ 。
(6)该流程中可以循环使用的物质的电子式为___ 。
(7)取mg活性氧化锌样品,预处理后配成待测液,加入指示剂3、4滴,再加入适量六亚甲基四胺,用amol•L-1EDTA标准液进行滴定,消耗标准液VmL。已知:与1.0mLEDTA标准液[c(EDTA)=1.000mol•L-1]相当的以克表示的氧化锌质量为0.08139,则样品中氧化锌的质量分数为___ (用代数式表示)。

已知:活性炭净化主要是除去有机杂质。
请回答以下问题:
(1)若浸出液中锌元素以[Zn(NH3)4]2+形式存在,则浸取时ZnO发生反应的离子方程式为
(2)在反应温度为50℃,反应时间为lh时,测定各元素的浸出率与氯化铵溶液浓度的关系如图,结合流程图分析,氯化铵适宜的浓度为

(3)若浸出液中c(AsO43-)=6.0×10-3mol•L-1,现将8.0×10-3mol•L-1FeC13溶液与浸出液等体积混合生成砷酸铁沉淀。若该温度时Ksp(FeAsO4)=2.0×10-22,则反应后溶液中c(AsO43-)=
(4)滤渣II的主要成分为
(5)沉锌得到的物质为Zn(NH3)2C12,请写出水解转化的化学方程式
(6)该流程中可以循环使用的物质的电子式为
(7)取mg活性氧化锌样品,预处理后配成待测液,加入指示剂3、4滴,再加入适量六亚甲基四胺,用amol•L-1EDTA标准液进行滴定,消耗标准液VmL。已知:与1.0mLEDTA标准液[c(EDTA)=1.000mol•L-1]相当的以克表示的氧化锌质量为0.08139,则样品中氧化锌的质量分数为
您最近一年使用:0次