某元素的最高价氧化物的分子式RO2,其中含R 27.27% 。对此元素的叙述不正确的是( )
| A.该元素为碳 |
| B.该元素的气态氢化物含H 25% |
| C.RO2为极性分子 |
| D.RO2与水反应能生成酸 |
更新时间:2020-02-12 18:31:27
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】随着原子序数的递增,八种短周期元素(x~h)原子半径的相对大小、最高正价或最低负价的变化如下图所示。下列说法错误的是


| A.h形成的最高价含氧酸的酸性比y形成的最高价含氧酸的酸性强,由此可以推出非金属性:h>y |
| B.d元素常见离子的半径大于f元素常见离子的半径 |
C.x、z元素组成ZX3共价化合物,其电子式可以表示为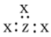 |
| D.g的最高价氧化物对应的水化物可以和f的单质、氧化物和氢氧化物反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
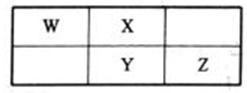
【推荐2】X、Y、Z、 W、R为原子序数依次增大的前20号主族元素,且分属于四个周期,Y的最外层电子数是电子层数的3倍,Z、W为同周期相邻元素,Y、 W可形成如图所示的离子,下列说法正确的是
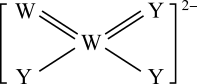

| A.该阴离子中W的化合价为+6 |
| B.简单离子半径: Y<W <R |
| C.最高价氧化物对应水化物酸性Z的比W的强 |
| D.Y与R能形成原子个数比为1:1或1:2等多种离子化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】短周期元素M、W、X、Y、Z的原子序数依次增大,质子数之和为37。M和W形成的某种化合物可作制冷剂,Y和Z能形成ZY2型离子化合物。下列有关叙述不正确的是( )
| A.Y元素没有正价 |
| B.M、W元素组成的化合物中一定只含极性共价键 |
| C.W、X、Y三种元素的简单氢化物稳定性:Y>X>W |
| D.X和Z形成的化合物ZX2中,阳离子和阴离子的数目之比为1:1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】A、B、D、E为原子序数依次递增的四种元素,简单离子A2–和E+相差一个电子层,B、D为同周期元素,B为金属元素,其基态原子最外层成对电子是未成对电子的2倍,D元素的原子最外层有一个未成对电子。下列有关元素及其化合物的说法错误的是
| A.简单离子半径:B﹤D |
| B.E与D形成的化合物晶体的熔点高于B与D形成的化合物晶体的熔点 |
| C.B、D、E的最高价氧化物对应的水化物之间能发生反应的化学方程式有4个 |
| D.DA2可用于自来水的消毒,其消毒效果(以每摩尔物质得到的电子数表示)相当于D2的2.5倍 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列数值表示有关元素的质子数,其所表示的各原子组中能以离子键相互结合成稳定化合物的是
| A.10和9 | B.6和16 | C.11和17 | D.14与8 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.CaCl2中既有离子键又有共价键,所以属于离子化合物 |
| B.H2O汽化成水蒸气、分解为H2和O2,都需要破坏共价键 |
| C.C4H10的两种同分异构体因为分子间作用力大小不同,因而沸点不同 |
| D.CH3COOH和CH3COOCH3互为同系物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】联氨(NH2-NH2)是一种绿色无污染的还原剂,NH2-NH2分子可能有以下两种不同的构象,沿N-N键轴方向的投影如图所示。下列说法错误的是
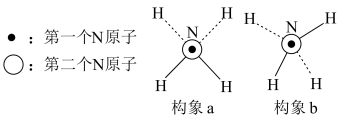

| A.NH2-NH2中N原子杂化方式为sp3 |
| B.实验测得NH2-NH2分子的极性很大,则其结构为构象b |
| C.NH2-NH2的沸点高于CH3-CH3的沸点 |
| D.NH2-NH2中的键角∠N-N-H小于H2O2中的键角∠O-O-H |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在半导体生产或灭火剂的使用中,会向空气逸散气体,如 、
、 与
与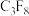 ,它们虽是微量的,有些却是强温室气体,下列有关推测正确的是
,它们虽是微量的,有些却是强温室气体,下列有关推测正确的是
 、
、 与
与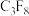 ,它们虽是微量的,有些却是强温室气体,下列有关推测正确的是
,它们虽是微量的,有些却是强温室气体,下列有关推测正确的是A. 属于非极性分子 属于非极性分子 |
B. 属于手性分子 属于手性分子 |
C.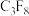 的三个碳原子在同一条直线上 的三个碳原子在同一条直线上 |
D.由价层电子对互斥理论可确定 分子中N原了是 分子中N原了是 杂化,分子呈平面三角形 杂化,分子呈平面三角形 |
您最近一年使用:0次


 与
与
 与NaOH
与NaOH 与
与

 分子的极性小于
分子的极性小于
 易溶于
易溶于 ,可从
,可从 中的氢键数量比
中的氢键数量比 少,可推断
少,可推断

