按要求填空:
(1)FeO·Cr2O3+NaNO3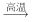 Na2CrO4+ Fe2O3+ CO2↑+NaNO2,上述反应配平后,FeO·Cr2O3与NaNO3的系数比为
Na2CrO4+ Fe2O3+ CO2↑+NaNO2,上述反应配平后,FeO·Cr2O3与NaNO3的系数比为________ ,该反应的氧化产物为_____________ ,该步骤不能使陶瓷容器,用反应式说明:_________ 。
(2)完成下列反应_____ MnO4—+H2O2+___=Mn2++__+H2O。
(3)Na2CO3溶液中通入足量Cl2,写出其离子反应方程式:_______________ 。
(4)将0.03mol Fe3O4完全溶解在200ml3. 00mol/L硫酸中,然后加入20.00ml K2Cr2O7溶液,
恰好使Fe2+全部转化为Fe3+,且Cr2O72—中的铬全部转化为Cr3+,则, K2Cr2O7的物质的量浓度是________ 。
(5)用离子反应方程式表示泡沫灭火器的反应原理:__________________ 。
(1)FeO·Cr2O3+NaNO3
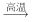 Na2CrO4+ Fe2O3+ CO2↑+NaNO2,上述反应配平后,FeO·Cr2O3与NaNO3的系数比为
Na2CrO4+ Fe2O3+ CO2↑+NaNO2,上述反应配平后,FeO·Cr2O3与NaNO3的系数比为(2)完成下列反应
(3)Na2CO3溶液中通入足量Cl2,写出其离子反应方程式:
(4)将0.03mol Fe3O4完全溶解在200ml3. 00mol/L硫酸中,然后加入20.00ml K2Cr2O7溶液,
恰好使Fe2+全部转化为Fe3+,且Cr2O72—中的铬全部转化为Cr3+,则, K2Cr2O7的物质的量浓度是
(5)用离子反应方程式表示泡沫灭火器的反应原理:
更新时间:2020-02-23 09:25:01
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】为了防止枪支生锈,常将枪支的钢铁零件放在NaNO2和NaOH的混合溶液中进行化学处理使钢铁零件表面生成Fe3O4的致密的保护层——“发蓝”。其过程可用下列化学方程式表示:
①3Fe+NaNO2+5NaOH===3Na2FeO2+H2O+NH3↑
②____Na2FeO2+____NaNO2+____H2O→____Na2Fe2O4+____NH3↑+____NaOH
③Na2FeO2+Na2Fe2O4+2H2O Fe3O4+4NaOH
Fe3O4+4NaOH
请回答下列问题:
(1)配平化学方程式②,各物质前的化学计量数依次为________ 。
(2)上述反应①中还原剂为________ ,被还原的是________ 。若有1 mol Na2FeO2生成,则反应①中有________ mol电子发生转移。
(3)关于“发蓝”的过程,下列说法正确的是________ (填字母)。
A.该过程不会产生污染
B.反应③生成的四氧化三铁具有抗腐蚀作用
C.反应①②③均是氧化还原反应
D.反应①②中的氧化剂均为NaNO2
(4)当混合溶液中NaOH浓度过大,“发蓝”的厚度会变小,其原因是___________________ 。
①3Fe+NaNO2+5NaOH===3Na2FeO2+H2O+NH3↑
②____Na2FeO2+____NaNO2+____H2O→____Na2Fe2O4+____NH3↑+____NaOH
③Na2FeO2+Na2Fe2O4+2H2O
 Fe3O4+4NaOH
Fe3O4+4NaOH请回答下列问题:
(1)配平化学方程式②,各物质前的化学计量数依次为
(2)上述反应①中还原剂为
(3)关于“发蓝”的过程,下列说法正确的是
A.该过程不会产生污染
B.反应③生成的四氧化三铁具有抗腐蚀作用
C.反应①②③均是氧化还原反应
D.反应①②中的氧化剂均为NaNO2
(4)当混合溶液中NaOH浓度过大,“发蓝”的厚度会变小,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:______KClO3+______HCl(浓)===______KCl+______ClO2↑+______Cl2↑+______H2O
(1) 请配平上述化学方程式____________________________________ 。
(2) 浓盐酸在反应中显示出来的性质是__________ (填编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3) 产生0.1 mol Cl2,则转移的电子的物质的量为__________ mol。
(4) 氧化剂是__________ ,氧化产物是__________ 。
(1) 请配平上述化学方程式
(2) 浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3) 产生0.1 mol Cl2,则转移的电子的物质的量为
(4) 氧化剂是
您最近一年使用:0次
【推荐3】Cu2S与一定浓度的HNO3反应,反应除了生成Cu(NO3)2、CuSO4和水以外,还有可能生成NO2或NO。回答下列问题:
(1)当NO2和NO的物质的量之比为1:1时,实际参加反应的Cu2S与HNO3的物质的量之比为___ 。
(2)若反应按上题发生,则被氧化的元素是____ 。
(3)若反应的还原产物只有NO2,且生成的物质的量为5mol,则电子转移的物质的量为__________ 。
(4)当反应的还原产物既有NO又有NO2时,Cu2S与HNO3反应的物质的量有多种系数比,原因是___ 。
(1)当NO2和NO的物质的量之比为1:1时,实际参加反应的Cu2S与HNO3的物质的量之比为
(2)若反应按上题发生,则被氧化的元素是
(3)若反应的还原产物只有NO2,且生成的物质的量为5mol,则电子转移的物质的量为
(4)当反应的还原产物既有NO又有NO2时,Cu2S与HNO3反应的物质的量有多种系数比,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)联氨 又称联肼,N2H4,无色液体
又称联肼,N2H4,无色液体 是一种应用广泛的化工原料,可用作火箭燃料。
是一种应用广泛的化工原料,可用作火箭燃料。
①联氨电子式为______ ,其中氮的化合价为______ 。
②联氨为二元弱碱,在水中的电离方程式与氨相似。写出联氨的第一步电离方程式_______________ ,联氨与硫酸形成的酸式盐的化学式为______ 。
(2)在100mLFeBr2溶液中通入标准状况下2.24LCl2,溶液中有 的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为
的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为______  结果保留两位小数
结果保留两位小数 。
。
(3)三氟化氮(NF3)是一种无色无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式______ ,反应中生成0.2molHNO3,转移的电子数目为______ 。
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是______ 。
 又称联肼,N2H4,无色液体
又称联肼,N2H4,无色液体 是一种应用广泛的化工原料,可用作火箭燃料。
是一种应用广泛的化工原料,可用作火箭燃料。①联氨电子式为
②联氨为二元弱碱,在水中的电离方程式与氨相似。写出联氨的第一步电离方程式
(2)在100mLFeBr2溶液中通入标准状况下2.24LCl2,溶液中有
 的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为
的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为 结果保留两位小数
结果保留两位小数 。
。(3)三氟化氮(NF3)是一种无色无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填空
(1)在S2-、Fe2+、Fe、Mg2+、H2S、I-、H+中,既有氧化性又有还原性的是________ 。
(2)实验室可用以下反应制备氯气:KClO3+6HCl(浓)= KCl+ 3Cl2↑+3H2O。反应中有1 mol电子转移时制得氯气44g,则反应物可能的组合是_______________
A.K35ClO3+6H35Cl B.K35ClO3+6H37Cl
C.K37ClO3+6H35Cl D.K37ClO3+6H37Cl
(3)将57.6 g的Cu片加入50 mL 18 mol/L的H2SO4溶液中并加热,被还原的H2SO4的物质的量为_________ (填“>”、“=”、“<”)0.45 mol
(4)火箭发射时以肼(N2H4)为燃料,也可以用一氧化氮作氧化剂,在此反应过程中若转移2 mol电子,则消耗燃料肼的质量为_______ 。
(5)已知溶液中含有以下离子: 、
、 、
、 、
、 、
、 、CH3COO-、Na+当加入足量Na2O2固体后,离子浓度几乎保持不变的是
、CH3COO-、Na+当加入足量Na2O2固体后,离子浓度几乎保持不变的是___________ 。
(1)在S2-、Fe2+、Fe、Mg2+、H2S、I-、H+中,既有氧化性又有还原性的是
(2)实验室可用以下反应制备氯气:KClO3+6HCl(浓)= KCl+ 3Cl2↑+3H2O。反应中有1 mol电子转移时制得氯气44g,则反应物可能的组合是
A.K35ClO3+6H35Cl B.K35ClO3+6H37Cl
C.K37ClO3+6H35Cl D.K37ClO3+6H37Cl
(3)将57.6 g的Cu片加入50 mL 18 mol/L的H2SO4溶液中并加热,被还原的H2SO4的物质的量为
(4)火箭发射时以肼(N2H4)为燃料,也可以用一氧化氮作氧化剂,在此反应过程中若转移2 mol电子,则消耗燃料肼的质量为
(5)已知溶液中含有以下离子:
 、
、 、
、 、
、 、
、 、CH3COO-、Na+当加入足量Na2O2固体后,离子浓度几乎保持不变的是
、CH3COO-、Na+当加入足量Na2O2固体后,离子浓度几乎保持不变的是
您最近一年使用:0次



